多廿烷醇(policosanol),是由C20 到C34 等多种饱和一元脂肪醇组成的混合物,主要从甘蔗蜡、蜂蜡、米糠中获得,从甘蔗蜡提取的多廿烷醇中,二十八烷醇的含量最高,占比约为60%~70%[1-2]。自古巴学者报道多廿烷醇可降血脂以来,许多学者指出,多廿烷醇能显著降低血浆总胆固醇(total cholesterol,TC)和低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)的水平,同时还能升高高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)的水平,具有显著的降脂效用,而且具有良好的耐受性和极高的安全性[3-8]。此外,多廿烷醇还能预防和治疗动脉血栓、血管内皮功能不良、动脉粥样硬化、间歇性跛行等诸多心血管疾病[9-11]。然而,也有研究者报道了动物实验和临床试验中的阴性结果[12-16],这引起了人们对多廿烷醇降脂功能的质疑。
血脂异常是造成心血管疾病的主要因素之一,合理应用他汀类药物可以降低胆固醇水平[17-18],但是许多患者在接受了较大剂量他汀治疗后,胆固醇水平仍不能得到有效控制[19];而且他汀类药物会对部分患者造成肝脏功能和骨骼肌损害,甚至有诱发骨骼肌溶解导致患者死亡的危险,此外还有致血糖异常和诱导糖尿病的风险[20]。近年来,胆固醇吸收抑制剂依折麦布作为一种新型调酯药物,在治疗高胆固醇血症中发挥的作用正日益受到关注[21-22]。受此启发,结合先前的研究,本文探讨了多廿烷醇对肠道胆固醇吸收的影响,进一步说明其降脂作用效果,并尝试分析其降脂机制。
1 材料方法
1.1 实验动物
5 周龄~6 周龄、7 周龄~8 周龄SPF 级健康SD 雄性大鼠、5 周龄~6 周龄KM 雄性小鼠:中山大学实验动物中心,喂食基础饲料或高脂饲料(配方:蔗糖20%、猪油15%、胆固醇1.2%、胆酸钠0.2%、酪蛋白10%、磷酸氢钙0.6%、石粉0.4%、预混料0.4%、基础饲料52.2%),所有动物实验均按中山大学实验动物管理和使用委员会以及中山大学实验动物伦理委员会的实验指导原则进行。
1.2 药品与试剂
胆固醇标准品、辛伐他汀阳性对照药:大连美仑生物技术有限公司;甲醇(色谱级)、正己烷(色谱级):天津市科密欧化学试剂有限公司;无水乙醇(分析纯)、异丙醇(色谱级):广州化学试剂厂;吐温80:sigma 公司;多廿烷醇:广东省科学院生物工程研究所。由于多廿烷醇极不溶于水,在配制时,先按照配制体积的10%加入无水乙醇,沸水浴加热1 min 使其充分溶解,后加入吐温80 一滴,充分摇匀,加水至总体积,漩涡振荡15 min,再超声30 min,即得多廿烷醇溶液,同时配制不加多廿烷醇的上述溶液作为溶媒剂(10%乙醇)。
1.3 多廿烷醇对喂食高脂饲料7 d 小鼠胆固醇吸收的影响
39 只雄性KM 小鼠,22 g~28 g,分成正常对照组、模型对照组、溶媒组、多廿烷醇低、中、高剂量组,其中前3 组每组6 只,后3 组每组7 只,正常对照组喂食常规饲料,其他组连续喂食高脂饲料7 d。第8 天,正常对照组和模型对照组用生理盐水灌胃,溶媒组用溶媒剂灌胃,多廿烷醇低、中、高3 组的给药剂量分别为10、20 mg/kg 和100 mg/kg,灌胃体积均为0.2 mL/10 g。于6、12、18、24 h 收集每组粪便测定胆固醇含量,收集粪便过程中动物正常喂食。实验结束后,取血测定总胆固醇(total cholesterol,TC)和甘油三酯(triglyceride,TG)指标。
1.4 多廿烷醇对喂食高脂饲料10 d 大鼠胆固醇吸收的影响
雄性SD 大鼠36 只,150 g~180 g,随机分成6 组,每组6 只,包括正常对照组、模型对照组、溶媒组和多廿烷醇低、中、高剂量组。除正常对照组用基础饲料喂养外,其余5 组均用高脂饲料喂养,其他条件均一致,饲养10 d。第11 天正常对照组和模型对照组用生理盐水灌胃,溶媒组用溶媒剂灌胃,多廿烷醇低、中、高3 个剂量组的给药剂量分别为10、20 mg/kg 和50 mg/kg,灌胃体积均为1 mL/100g。给药结束后,以6 h 为单位,收集各组大鼠24 h 粪便测定胆固醇,给药后24 h 动物不再喂食饲料,实验结束时取血测定TC、TG 指标。
1.5 多廿烷醇对喂食高脂饲料30 d 大鼠胆固醇吸收的影响
雄性SD 大鼠30 只,180 g~220 g,随机分为6 组,每组5 只,具体的分组、饲养及给药情况与1.4 一致,在高脂饮食时同时进行灌胃给药并持续30 d。每天称重,记录体重变化。给药期间,每7 d 收集一次每组大鼠一昼夜(24 h)的粪便测定胆固醇含量,共收集4 周。实验结束后,均按50 mg/kg 剂量腹腔注射2%戊巴比妥钠麻醉大鼠,下腔静脉取血,所有血液于常温(25 ℃)放置20 min,而后3 000 r/min 离心15 min,得新鲜无溶血血清,测定TC、TG、HDL-C、LDL-C 等血脂指标。
1.6 相关指标测定
参照曹晓钢等的方法处理粪便[23],具体为将所收集到的粪便进行干燥处理,并用研钵将粪便充分碾磨混匀后,准确称取200 mg 于15 mL 离心管中,加入10 mL 甲醇超声30 min,1 500 r/min 离心15 min,取上清,0.45 μm 有机滤膜过滤,滤液作为供试品溶液,采用高压液相色谱法(high performance liquid chromatography,HPLC)测定胆固醇浓度,具体条件如下[23]:色谱条件,色谱柱ODS-C18(250 mm×4.6 mm,5 μm),流动相为甲醇∶异丙醇(80 ∶20,体积比),检测波长210 nm,流速1.0 mL/min,柱温35 ℃,进样量为10 μL。
采用全自动血脂测试仪对血清TC、TG、HDL-C 和LDL-C 进行测定。大鼠实验的血脂测定由广州金域医学检验中心完成。
2 结果与分析
2.1 HPLC 测定结果
胆固醇标准品HPLC 色谱图及样品色谱图见图1。胆固醇定量标准曲线见图2。

图1 胆固醇标准品HPLC 色谱图及样品色谱图
Fig.1 HPLC chromatogram of cholesterol standard and sample
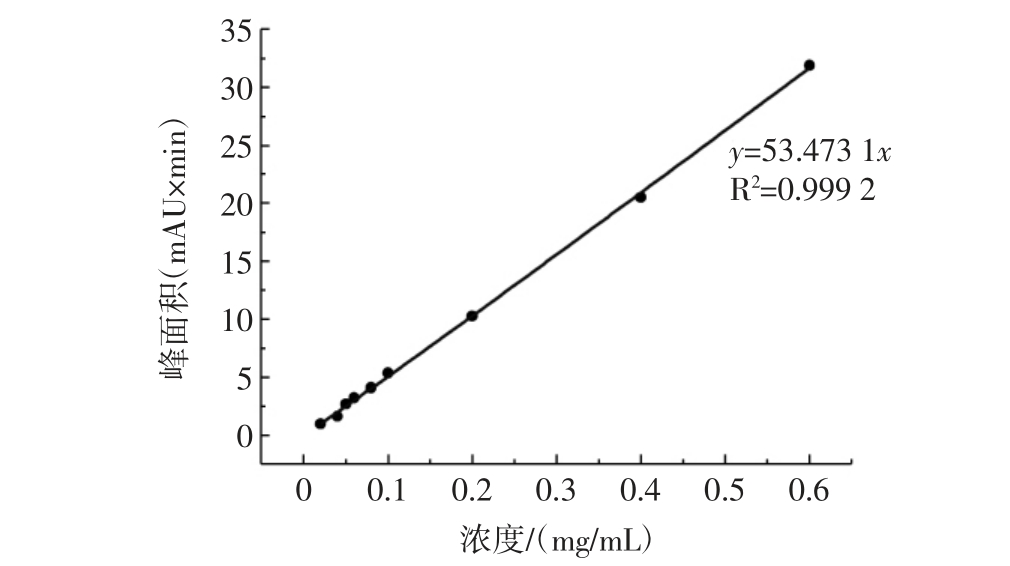
图2 胆固醇定量标准曲线
Fig.2 Quantitative standard curve of cholesterol
在HPLC 测定条件下,对胆固醇标准品进行色谱分析(图1 A),得到此色谱条件下的胆固醇保留时间在10.5 min 左右,再对样品进行色谱分析(图1 B),可以看到目标物质与胆固醇标准品的出峰时间一致,且与非目标物质的分离度良好,证明该条件适合试验样品的分析,能达到测定要求,再对一系列浓度梯度的胆固醇标准品分析之后制得标准曲线(图2)。
此外,在此HPLC 条件下,进行以下试验:取某一样品,每4 h 进样1 次,共进样5 次,进行稳定性试验;选取0.04 mg/mL 标准品溶液,连续进样5 次,进行精密度试验;准确称取大鼠同一份粪便5 份,连续进样5次,进行重复性试验;取5 份浓度已知的样品,分别加入等体积0.06 mg/mL 胆固醇标准品溶液,陆续进样,进行加样回收率测定试验。胆固醇HPLC 测定的稳定性、精密度和重复性试验结果见表1,大鼠粪便中胆固醇加样回收率测定结果见表2。
表1 胆固醇HPLC 测定的稳定性、精密度和重复性试验结果
Table 1 The HPLC experimental results of stability,precision and reproducibility of cholesterol

项目 峰面积/(mAU×min) 相对标准偏差/%稳定性试验 4.66±0.04 0.98精密度试验 1.71±0.09 0.51重复性试验 4.72±0.05 1.09
表2 大鼠粪便中胆固醇加样回收率测定结果
Table 2 The results of recovery rate test of cholesterol in rat feces

序号 测得浓度/(mg/mL)相对标准偏差/%1 0.061 0.065 0.93 0.94 1.09 2 0.061 094 3 0.061 0.94 4 0.061 0.94 5 0.062 0.95(mg/mL) 回收率/% 平均回收率/%实际浓度/
从稳定性试验、精密度试验和重复性试验(表1)以及加样回收率试验(表2)得到的相对标准偏差来看,仪器性能良好,试验数据具有很强的可信度。
2.2 多廿烷醇单次给药对喂食高脂饲料7 d 小鼠胆固醇吸收的影响
正常喂养的小鼠粪便中含一定量的胆固醇,这与动物胆固醇的代谢机理是一致的。正常情况下,肠道内胆固醇75%来源于胆汁,25%源自食物[21],动物粪便胆固醇一方面来自饲料中未被吸收的部分,但主要由未被吸收的肠道内胆汁产生。多廿烷醇对喂食高脂饲料7 d 小鼠粪便胆固醇及血脂的影响见表3。
结果显示,小鼠经过7 d 高脂饲料喂养,粪便胆固醇浓度成10 倍以上增加,而血液中TC 和TG 含量分别增加了83%和34%,说明粪便胆固醇的增加主要源于高脂饲料中未被吸收的胆固醇,体现了机体物质代谢平衡的机制。模型对照组与正常对照组比较,血脂TC、TG 均有显著增加,说明高脂饲料对动物脂肪代谢影响较大。溶媒剂(10%乙醇)在灌胃的12 h 内促进胆固醇吸收,因此使粪便中胆固醇浓度明显减少,6 h 和12 h的粪便胆固醇含量仅为模型对照组的49%和54%,随着乙醇代谢完毕,该数值逐渐升高至与模型对照组相近。与模型对照组相比,一次灌胃多廿烷醇3 个剂量均在12 h 内增加了胆固醇的排出量,使粪便胆固醇浓度升高,其中6 h 的粪便胆固醇含量分别提升46%(P-10)、35%(P-20)和42%(P-100),12 h 后也有13%~24%的增长率。与模型对照组和溶媒组比较,多廿烷醇对血液中TC 含量未有明显影响,但中、高剂量组血液中TG 含量显著降低,表现出一定的降脂作用。
表3 多廿烷醇对喂食高脂饲料7 d 小鼠粪便胆固醇及血脂的影响
Table 3 The effect of policosanol on fecal cholesterol and blood lipid in mice fed high-fat diet for 7 days

注:P-10、P-20 和P-100 分别表示小鼠实验多廿烷醇低、中、高剂量组。粪便是一组动物在笼中一起收集,为一个测定值。血脂指标表示为平均值±标准差,n=6。与正常对照组比较,**P<0.05 表示差异显著;与溶媒组比较,##P<0.05 表示差异显著。
组别 粪便胆固醇含量/(mg/g 粪便)TC/(mmol/L) TG/(mmol/L)6 h 12 h 18 h 24 h正常对照组3.84 3.91 2.73 2.71 5.23±0.93 0.98±0.11模型对照组40.80 48.06 57.20 57.67 9.59±1.25** 1.31±0.38**溶媒组 19.99 25.74 50.54 53.37 9.74±1.27 1.05±0.28 P-10 59.68 59.66 55.80 54.78 10.8±1.89 1.53±0.64 P-20 55.00 54.13 55.09 56.67 10.4±1.66 0.83±0.37##P-100 57.84 54.08 49.11 50.48 9.35±0.92 0.60±0.20##
2.3 多廿烷醇单次给药对喂食高脂饲料10 d 大鼠胆固醇吸收的影响
多廿烷醇对喂食高脂饲料10 d 大鼠粪便胆固醇及血脂的影响见表4。
正常大鼠粪便中同样含有一定量的胆固醇(表4),这与小鼠一致。尽管粪便收集是一组一起收集,只有一个测定值,但这个测定值是一组6 只动物产生的,也反映一定的实验规律。在利用高脂饲料喂食10 d后,进行灌胃给药,然后禁食来研究药物进入体内后对于体内代谢和排出胆固醇的情况。实验结果证明了多廿烷醇在一定程度上能够抑制机体对于胆固醇的吸收,促进了机体胆固醇的排泄。无论是正常对照组,还是高脂饲料喂食的模型对照组,在开始禁食的18 h内,粪便胆固醇含量都是明显降低的,这与胆固醇停止摄入有关。24 h 的粪便胆固醇浓度均有升高,而高脂饲料喂养的动物更明显,说明高脂饲料喂养导致体内胆固醇水平升高,排泄到肠道的也增多。对于高脂饲料喂食10 d 的大鼠,多廿烷醇3 个剂量组使粪便胆固醇浓度增加,抑制了食物中胆固醇的吸收;与溶媒组相比较,在24 h 时,P-10、P-20 和P-50 的胆固醇浓度分别升高了60%、81%和123%,这说明多廿烷醇也促进了体内胆固醇的排出。本实验结果说明,多廿烷醇能明显抑制机体消化系统对胆固醇的吸收,也增加了机体对胆固醇的排泄。多廿烷醇高剂量组的TC 和TG水平比模型对照组和溶媒组显著降低,尤其TG 已达到正常水平,可能是其对胆固醇代谢调节的结果。
表4 多廿烷醇对喂食高脂饲料10 d 大鼠粪便胆固醇及血脂的影响
Table 4 The effect of policosanol on fecal cholesterol and blood lipid in rats fed high-fat diet for 10 days
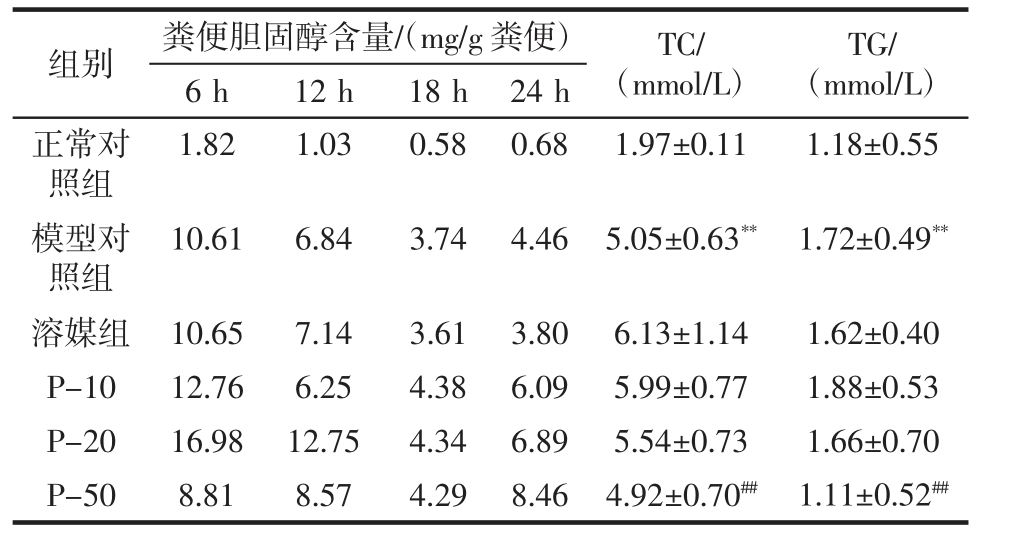
注:P-10、P-20 和P-50 分别表示大鼠实验多廿烷醇低、中、高剂量组。粪便是一组动物在笼中一起收集,只有一个测定值。血脂指标表示为平均值±标准差,n=6。与正常对照组比较,**P<0.05 表示差异显著;与溶媒组比较,##P<0.05 表示差异显著。
组别 粪便胆固醇含量/(mg/g 粪便) TC/(mmol/L)TG/(mmol/L)6 h 12 h 18 h 24 h正常对照组1.82 1.03 0.58 0.68 1.97±0.11 1.18±0.55模型对照组10.61 6.84 3.74 4.46 5.05±0.63** 1.72±0.49**溶媒组 10.65 7.14 3.61 3.80 6.13±1.14 1.62±0.40 P-10 12.76 6.25 4.38 6.09 5.99±0.77 1.88±0.53 P-20 16.98 12.75 4.34 6.89 5.54±0.73 1.66±0.70 P-50 8.81 8.57 4.29 8.46 4.92±0.70## 1.11±0.52##
2.4 多廿烷醇连续给药对喂食高脂饲料30 d 大鼠胆固醇吸收的影响
多廿烷醇连续给药对喂食高脂饲料30 d 大鼠粪便胆固醇含量的影响见表5。
表5 多廿烷醇连续给药对喂食高脂饲料30 d 大鼠粪便胆固醇含量的影响
Table 5 The effect of continuous administration of policosanol on cholesterol content in feces of rats fed with high-fat diet for 30 days

注:P-10、P-20 和P-50 分别表示大鼠实验多廿烷醇低、中、高剂量组。粪便是一组5 只动物在笼中一起收集,本次实验制备3 个平行样品,表示为平均值±标准差,n=3。
组别 24h 粪便胆固醇含量/(mg/g 粪便)第1 周 第2 周 第3 周 第4 周正常对照组 0.51±0.01 0.62±0.07 0.68±0.01 0.70±0.03模型对照组 6.01±0.30 6.68±0.33 7.31±0.25 8.52±0.14溶媒组 9.02±0.46 9.76±0.53 7.79±0.31 9.86±0.44 P-10 8.10±0.12 7.92±0.44 9.33±0.54 8.58±0.83 P-20 9.21±0.53 8.11±0.41 9.38±0.32 8.30±0.30 P-50 8.79±0.15 8.81±0.24 6.44±0.11 7.89±0.51
与2.2 和2.3 实验结果一致,高脂饲料喂养,使动物粪便中胆固醇含量大幅增加,而且随着高脂饲料喂养时间延长,大鼠粪便胆固醇含量也呈增加的趋势,如表5 所示,模型对照组第4 周比第1 周粪便胆固醇含量明显增多,增长量高达42%。结合2.2 和2.3 实验结果,到第4 周时高脂饲料喂养的大鼠粪便胆固醇浓度的增加表明动物排泄到肠道的胆固醇也增加了。溶媒组(10%乙醇)的结果显示整体上每周24 h 粪便胆固醇浓度都比模型对照组高,这说明10%乙醇对动物胆固醇的代谢影响很大,粪便中胆固醇增加是机体胆固醇水平升高的结果。此外,发现多廿烷醇3 个剂量组中,粪便胆固醇含量大多数在溶媒组和模型对照组之间,一方面说明多廿烷醇对高脂饲料喂养动物脂肪代谢有一定调节作用,另一方面也说明多廿烷醇对乙醇影响胆固醇水平的作用有一定影响。
大鼠血脂四项水平见表6。
表6 大鼠血脂四项水平
Table 6 The level of four blood lipids items mmol/L

注:P-10、P-20、P-50 分别表示大鼠实验多廿烷醇低、中、高剂量组。与正常对照组相比:##P<0.05 表示差异显著。
组别 TC TG HDL-C LDL-C正常对照组 1.48±0.15 0.56±0.22 1.29±0.08 0.37±0.10模型对照组 2.64±0.33## 0.67±0.26 1.07±0.15## 1.61±0.22##溶媒组 2.54±0.48 0.76±0.35 1.16±0.13 1.66±0.66 P-10 2.58±0.51 0.89±0.51 1.04±0.04 1.29±0.11 P-20 2.47±0.38 0.78±0.12 1.12±0.12 1.35±0.34 P-50 2.62±0.21 0.90±0.22 1.06±0.04 1.32±0.18
30 d 后取血测定的血脂四项的结果大体上与粪便胆固醇测定结果相符。与正常对照组相比(表6),模型对照组血脂TC 和LDL-C 水平显著升高,分别增加78%和335%,而HDL-C 水平降低了17%,表明高脂饲料影响了机体的脂肪代谢。而溶媒组(10%乙醇)与模型对照组比较,尽管血脂四项水平同样处于异常,但几项指标没有显著性差别,这可能与溶媒组动物有较高的胆固醇排出量有关,但这个机制尚不明确。与溶媒组相比,多廿烷醇3 个剂量组LDL-C 水平有下降,但在目前样本量下没有显著性差别,综合血脂TC 和HDL-C 结果来看,多廿烷醇对脂肪代谢有一定的调节作用。
3 讨论与结论
古巴学者的系列研究证明多廿烷醇具有极好的降脂作用,且没有明显的副作用,被誉为“血管的清道夫”,加之具有来源广、低成本的特点,多廿烷醇已经被作为第五大降脂药物应用于临床。随着研究增加也出现了一些阴性结果,例如,美国[12]和德国[16]进行的随机、双盲、安慰剂对照临床试验,分别以40 例和143例高血脂症患者为研究对象,分成口服多廿烷醇20、40 mg/d 和80 mg/d 剂量和安慰剂8 周~12 周,结果显示,治疗组与对照组间血脂TC、TG 和HDL 水平变化无显著性差异。为了进一步明确多廿烷醇的效果,为临床应用提供明晰的依据,本文从机体的胆固醇代谢入手来探讨多廿烷醇的作用。
动物机体(包括人)血液中胆固醇主要来源于肝脏与外周组织生物合成的内源性胆固醇和食物的肠道吸收外源性胆固醇[21]。机体胆固醇的生物合成与肠道吸收处于一种代偿平衡,生物合成受抑制时,吸收会增加,反之亦然。本文通过高脂饲料分别喂养小鼠7 d、大鼠10 d 和30 d,均显著增加了动物粪便胆固醇排出量,也显著增加了血脂水平。高脂饲料会大大促进食物中脂肪和胆固醇被动物吸收进入机体,导致血液TC 和TG 升高,而血液TC 水平上升后也会增加胆固醇的排出量,因此食物中未被吸收的胆固醇和胆汁排出的胆固醇都会使粪便胆固醇量增加。实验发现,乙醇与高脂饲料同时存在,可促进动物对胆固醇的吸收,也许因为平衡的机制,胆固醇的排出也会增加。
在高脂喂食7 d 小鼠实验和10 d 大鼠实验中,多廿烷醇能显著地增加动物胆固醇的排泄量,既能抑制胆固醇的吸收,也能增加高血脂大鼠对胆固醇的排出,这揭示多廿烷醇能对机体胆固醇的代谢产生影响。高脂喂食30 d,与溶媒组比较,多廿烷醇组胆固醇的排泄量减少,这可能是其通过其他机制降低了血液胆固醇水平,而使机体通过胆汁排泄胆固醇减少。结果表明多廿烷醇能发挥降脂作用,机制之一就是对胆固醇代谢的影响。
综上所述,多廿烷醇具有一定的降脂作用,其降脂作用既可能与抑制胆固醇肠道吸收、调节胆固醇的代谢有关,也可能存在其他机制来降低血脂水平。
[1] KIM J Y,LEE J H,JEONG D Y,et al.Preparation and characterization of aqueous dispersions of dextrin and policosanol composites[J].Carbohydrate Polymers,2015,121:140-146.
[2] WEERAWATANAKORN M,MEEROD K,WONGWAIWECH D,et al.Policosanols:chemistry,occurrence,and health effects[J].Current Pharmacology Reports,2019,5(3):131-149.
[3] POLI A,VISIOLI F.Pharmacology of nutraceuticals with lipid lowering properties[J].High Blood Pressure & Cardiovascular Prevention,2019,26(2):113-118.
[4] BIANCONI V,MANNARINO M R,SAHEBKAR A,et al.Cholesterollowering nutraceuticals affecting vascular function and cardiovascular disease risk[J].Current Cardiology Reports,2018,20(7):53.
[5] ASKARPOUR M,GHAEDI E,ROSHANRAVAN N,et al.Policosanol supplementation significantly improves blood pressure among adults:a systematic review and meta-analysis of randomized controlled trials[J].Complementary Therapies in Medicine,2019,45:89-97.
[6] LEE J Y,CHOI H Y,KANG Y R,et al.Effects of long-term supplementation of policosanol on blood cholesterol/glucose levels and 3-hydroxy-3-methylglutaryl coenzyme a reductase activity in a rat model fed high cholesterol diets[J].Food Science and Biotechnology,2016,25(3):899-904.
[7] SHEN J J,LUO F J,LIN Q L.Policosanol:Extraction and biological functions[J].Journal of Functional Foods,2019,57:351-360.
[8] 郭艺芳.降胆固醇治疗的过去、现状与展望[J].中华高血压杂志,2014,22(11):1001-1003.
[9] CASTAÑO G,FERREIRO R M,FERNÁNDEZ L,et al.A long-term study of policosanol in the treatment of intermittent claudication[J].Angiology,2001,52(2):115-125.
[10] CARBAJAL D, ARRUZAZABALA M L, MÁS R, et al. Effect of policosanol on experimental thrombosis models [J]. Prostaglandins,Leukotrienes and Essential Fatty Acids,1994,50(5):249-251.
[11] ARRUZAZABALA M L, CARBAJAL D, MAS R, et al. Effects of policosanol on platelet aggregation in rats [J].Thrombosis Research,1993,69(3):321-327.
[12] DULIN M F,HATCHER L F,SASSER H C,et al.Policosanol is ineffective in the treatment of hypercholesterolemia: a randomized controlled trial[J].The American Journal of Clinical Nutrition,2006,84(6):1543-1548.
[13] FRANCINI Pesenti F, BELTRAMOLLI D, S Dall'Acqua, et al. Effect of sugar cane policosanol on lipid profile in primary hypercholesterolemia[J].Phytotherapy Research,2008,22(3):318-322.
[14] JONES P J H, KASSIS A N, MARINANGELI C P F. Policosanols lose their lustre as cholesterol-lowering agents [J].Journal of Functional Foods,2009,1(2):236-239.
[15] KASSIS A N,JONES P J H.Lack of cholesterol-lowering efficacy of Cuban sugar cane policosanols in hypercholesterolemic persons[J].The American Journal of Clinical Nutrition, 2006, 84 (5): 1003-1008.
[16] BERTHOLD H K, UNVERDORBEN S, DEGENHARDT R, et al.Effect of policosanol on lipid levels among patients with hypercholesterolemia or combined hyperlipidemia [J]. The Journal of the American Medical Association,2006,295(19):2262.
[17] 吕昂,王海红.他汀类药物个体化差异的研究进展[J].中国乡村医药,2015,22(23):83-86.
[18] 陈爱荣.他汀类降脂药的合理选择应用[J].浙江临床医学,2011,13(8):940-941.
[19] 叶平,王晓娜.从百年胆固醇学说到新型降脂药物[J].中国循环杂志,2016,31(1):1-3.
[20] PREISS D.Risk of incident diabetes with intensive-dose compared with moderate-dose statin therapy[J].The Journal of the American Medical Association,2011,305(24):2556.
[21] 李云建.胆固醇吸收抑制剂——依折麦布[J].医学理论与实践,2012,25(11):1304-1305.
[22] 徐艳玲,张静,周琳.调脂药物-依折麦布的研究进展[J].中国循证心血管医学杂志,2012,4(2):168-169.
[23] 曹晓钢,于刚,叶小利,等.中药提取物抑制胆固醇吸收的研究[J].中成药,2009,31(4):616-618.