黑木耳(Auricularia auricula)作为一种药食同源资源,具有丰富的营养和药用价值[1]。黑木耳多糖(Auricularia auricula polysaccharides,AAP)是黑木耳中重要的活性成分[2],作为天然活性多糖,已被证明具有广泛的生理调节功能,目前研究热点主要集中在黑木耳多糖的抗氧化[3]、抗肿瘤[4-6]、免疫调节[7]及益生作用[8]等方面。
针对黑木耳多糖益生作用的研究,通常以益生菌数量增殖效果为评价指标,而益生菌代谢产物或次级代谢产物对人体健康具有重要作用[9]。黑木耳多糖的肠道益生作用研究通常仅针对正常生理实验动物的肠道菌群种类、数量等指标进行分析[10],未充分考虑特殊生理人群和病理人群的特点。高血脂患者肠道菌群紊乱[11],黑木耳多糖及其复配物是否具有针对该类人群的调节作用有待探究。本研究在提取并鉴定黑木耳多糖的基础上,评价其对乳酸菌蛋白质类代谢产物的影响及其对高血脂人群的肠道益生作用,以期为未来高血脂人群功能性食品开发奠定理论基础。
1 材料与方法
1.1 材料、试剂与实验动物
乳酸链球菌菌株(HW-1):河北科技大学营养与功能性食品研究室保留菌种;黑木耳:中康蔬菜种植有限公司;银耳多糖、山楂黄酮:河北科技大学营养与功能性食品研究室提供,乳酸菌培养用MRS液体或固体培养基[12]。辛伐他汀片:北京万生药业有限责任公司(批号:31801043)。
谷胱甘肽过氧化物酶测试盒、超氧化物歧化酶测试盒、丙二醛测试盒、过氧化氢酶测试盒:南京建成生物科技有限公司。
DNA提取试剂盒:美国Omega生物技术公司;MiSeq测序试剂盒:美国Illumina公司;DNA凝胶回收试剂盒:美国Axygen公司;核酸纯化试剂盒:美国Beckman Coulter公司;文库定量试剂盒:美国KAPA公司。
SPF级雄性 Wistar大鼠,体质量(200±20)g,河北医科大学实验动物中心提供,许可证SCXK(冀)2018-004。
高脂饲料配方:基础饲料78.8%,猪油10%,蛋黄粉10%,胆固醇1%和胆酸盐0.2%。基础饲料由河北医科大学实验动物中心提供。基础饲料配方见表1。
表1 基础饲料配方
Table 1 The formula of basic feed

成分面粉麦片玉米粉豆面含量/%25 25 25 10成分 含量/%鱼粉 8骨粉 4酵母粉 2精盐 1
1.2 仪器与设备
高通量测序仪(PE300):美国Illumina公司;电泳仪(dyy-12):北京市六一仪器厂;凝胶成像系统(Alpha Imager HP):美国Protein Simple公司;生物分析仪(DE13806339):安捷伦科技有限公司;生物大分子分析仪(LabChip GX)、实时定量 PCR 仪(ABI 7500):美国Perkin Elmer公司。
1.3 方法
1.3.1 黑木耳多糖提取与鉴定
1.3.1.1 黑木耳多糖提取
将黑木耳用液氮冷冻法粉碎后过120目筛。采用水提醇沉法,在料液比 1∶60(g/mL)、温度 60 ℃、超声功率180 W的条件下提取20 min,于4 500 r/min离心6 min,收集上清液。重复提取3次,合并提取液干燥备用。用苯酚-硫酸法测定溶液中多糖含量[13]。
1.3.1.2 黑木耳多糖鉴定
参考莫开菊等[14]的方法,采用苯基-3-甲基-5-吡唑啉酮(1-phenyl-3-methyl-5-pyrazolone,PMP)柱前衍生化高效液相色谱(high performance liquid chromatography,HPLC)分析黑木耳多糖的单糖组成。HPLC条件:SHISEIDO C18色谱柱(4.6 mm×250 mm,5 μm),流动相A为0.1 mol/L KH2PO4(pH6.8);流动相B为乙腈;A∶B=82∶18(体积比);流速 1.0 mL/min;柱温 25 ℃;进样量10 μL;波长为245 nm。
1.3.2 黑木耳多糖对乳酸菌代谢产物影响
将对数生长期的乳酸链球菌按5%的接种量,接种到MRS液体培养基中,分别以0%、1%、5%、10%、20%、30%黑木耳多糖处理,37℃恒温培养14 h。每2 h取样并于4 200 r/min条件下离心20 min取上清液,采用考马斯亮蓝法[15]测定蛋白质含量。
1.3.3 黑木耳多糖体内益生作用分析
将36只SPF级Wistar雄性大鼠随机分为4组,分别为空白组(NC)、模型组(HFD)、辛伐他汀组(PCI)和复配物组(HDC),大鼠在自由采食高脂饲料的同时进行黑木耳多糖复配物干预,连续给药5周,具体处理方式见表2。
表2 实验设计方案(n=9)
Table 2 Experimental design scheme(n=9)

组别 饲料及灌胃量NC 普通饲料+1 mL/100 g蒸馏水HFD 高脂饲料+1 mL/100 g蒸馏水PCI高脂饲料+辛伐他汀6.7 mg/(kg·d)HDC高脂饲料+[黑木耳多糖提取物100 mg/(kg·d)+银耳多糖提取物100 mg/(kg·d)+山楂黄酮提取物100 mg/(kg·d)]
1.3.4 检测样品采集
大鼠在末次灌胃12 h后,收集大鼠血清、肝脏和脑等器官,于-80℃保存备用。无菌收集结肠内粪便,置于无菌EP管中,迅速液氮冷却后置于-80℃冰箱保存备用。
1.3.5 抗氧化能力分析
根据试剂盒说明指示,依次对脑、肝脏组织中丙二醛(malondialdehyde,MDA)含量、过氧化氢酶(catalase,CAT)活性、超氧化物歧化酶(superoxide dismutase,SOD)活性和谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)活性进行测定。
1.3.6 Illumina高通量测序
对大鼠粪便样品进行16S rRNA基因V3~V4区域的聚合酶链式反应(polymerase chain reaction,PCR)扩展以及Illumina高通量测序。基于肠道菌群的16S rRNA基因V3~V4区域合成相关引物,进行PCR扩增,其中扩增所使用的引物序列为338F(5′-ACTCCTACGGGAGGCAGCAG-3′)和 806R(5′-GGACTACNNGGG TATCTAAT-3′)[16]。扩增的体系和扩增条件见表3与表4。
表3 16S rRNA基因V3~V4区PCR扩增体系
Table 3 16S rRNA gene V3-V4 region PCR amplification system

试剂成分 体积DNA 样品 X(30 ng)上游引物(5 μmol/L) 1 μL下游引物(5 μmol/L) 1 μL牛血清蛋白(2 ng/μL) 3 μL 2×Taq Plus Master Mix 12.5 μL ddH2O (7.5-X)μL总计 25 μL
表4 PCR扩增条件
Table 4 PCR amplification condition

温度/℃ 时间 循环数94 5 min 94 30 s 55 30 s 72 60 s 72 7 min 4结束 0 0 28 0 0 0
1.3.7 数据统计分析
数据处理采用SPSS20.0进行统计学分析。用单因素方差分析法分析组间差异的显著性,结果采用平均值±标准差表示,P<0.05表示差异具有统计学意义。
2 结果与分析
2.1 黑木耳多糖提取结果
黑木耳多糖提取结果见图1。

图1 黑木耳多糖提取结果
Fig.1 Extraction results of Auricularia auricula polysaccharides
(a)黑木耳颗粒电镜扫描结果;(b)多糖标准曲线。
通过扫描电镜对黑木耳颗粒进行形态学观察,如图1(a)所示,冷冻粉碎处理的黑木耳样品具有较高的粒度级别,并具有良好的粒度均一性。
采用苯酚硫酸法测定多糖,绘制标准曲线,如图1(b)所示。获得回归方程为y=8.626 7x+0.140 3,相关系数R2=0.999 1。
本试验通过冷冻粉碎方法对黑木耳进行前处理,多糖的提取率达10.2%。
2.2 黑木耳多糖鉴定
单糖组成色谱图见图2。

图2 单糖组成色谱图
Fig.2 HPLC chromatogram of PMP derivatives
(a)混合标准单糖PMP衍生物;(b)黑木耳多糖PMP衍生物。
由图2中各峰保留时间和峰面积,对黑木耳多糖的单糖组成进行分析,结果表明,黑木耳多糖中主要以葡萄糖、甘露糖为主,单糖比例葡萄糖∶甘露糖∶木糖∶岩藻糖∶半乳糖∶葡萄糖醛酸为 13.47∶8.64∶2.13∶1.95∶1.69∶1.00。
2.3 黑木耳多糖益生作用研究
黑木耳多糖对乳酸链球菌蛋白质代谢的影响结果如图3所示。

图3 黑木耳多糖对乳酸链球菌蛋白质代谢的影响
Fig.3 Effects of different concentrations of polysaccharides on protein metabolism of lactic acid bacteria
(a)0~14 h蛋白代谢情况;(b)8 h蛋白质代谢情况;*表示差异显著(P<0.05)。
当培养基中多糖含量为30%时,蛋白质含量随时间呈抛物线式变化。在8 h时,培养基中的蛋白质含量达到最大值114.48 mg/L,随后快速下降。多糖浓度0~20%时,乳酸菌的蛋白质代谢无显著变化。
2.4 体内抗氧化能力分析
黑木耳多糖复配物对大鼠血清抗氧化能力的影响见表5。
表5 黑木耳多糖复配物对大鼠血清抗氧化能力的影响
Table 5 Effects of A.auricula polysaccharides complex on serum antioxidant capacity in rats

注:不同小写字母表示差异显著(P<0.05)。
组别 CAT活力/(U/mL)SOD活力/(U/mL)NC 7.85±2.80a 2 243.30±177.36a 11.81±1.34ab486.79±57.82a HFD 3.73±0.34c 2 065.97±195.45ab 12.68±0.89a401.18±24.95b PCI 6.22±1.87abc2 093.10±132.14ab11.94±1.98ab420.06±65.58ab HDC 5.17±0.96bc2 068.52±122.61ab11.81±1.28ab484.02±56.58a GSH-Px活力/(U/mL)MDA含量/(nmol/mL)
黑木耳多糖复配物具有较好的抗氧化能力。由表5可知,与NC组相比,HFD组大鼠血清CAT活力与SOD 活力显著降低(P<0.05),GSH-Px活力降低、MDA含量升高,但不存在显著差异(P>0.05)。与HFD组相比,PCI组与HDC组的GSH-Px活力、SOD活力均有不同程度的升高,MDA含量降低。其中HDC组SOD活力显著高于HFD组(P<0.05)。
黑木耳多糖复配物对大鼠肝脏抗氧化能力的影响见表6。
表6 黑木耳多糖复配物对大鼠肝脏抗氧化能力的影响
Table 6 Effects of A.auricula polysaccharides complex on antioxidant capacity of rat liver

注:不同小写字母表示差异显著(P<0.05)。
组别 CAT活力/(U/mg)SOD活力/(U/mg)NC 60.66±9.57a 253.48±29.55a 1.41±0.37b146.12±34.40a HFD 43.38±4.83b 199.16±0.90c 2.12±0.49a 127.66±9.65a PCI 56.28±6.27ab 218.67±22.17abc1.90±0.24ab145.46±19.16a HDC 48.48±6.42ab 239.59±23.03ab1.73±0.28ab135.89±15.30a GSH-Px活力/(U/mg)MDA含量/(nmol/mg)
由表6可知,与NC组相比,HFD组大鼠肝脏CAT活力和 GSH-Px活力显著降低(P<0.05),MDA 含量显著升高(P<0.05)。与HFD组相比,HDC组GSH-Px活力显著升高。
黑木耳多糖复配物对大鼠脑抗氧化能力的影响见表7。
表7 黑木耳多糖复配物对大鼠脑抗氧化能力的影响
Table 7 Effects of A.auricula polysaccharides complex on antioxidant capacity of rat brain
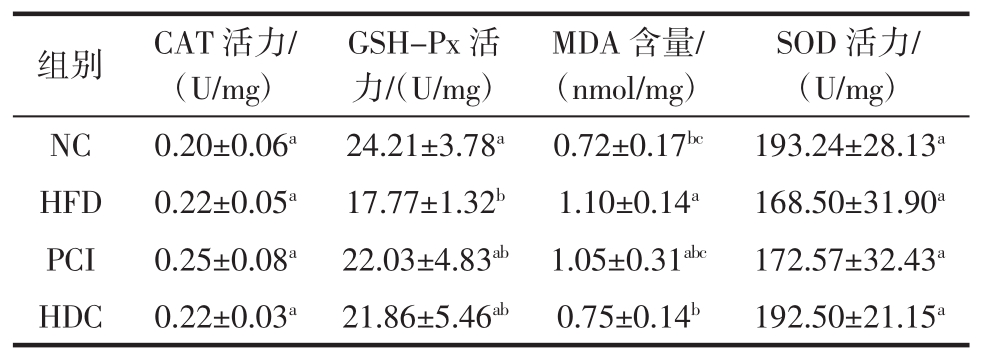
注:不同小写字母表示差异显著(P<0.05)。
组别 CAT活力/(U/mg)SOD活力/(U/mg)NC 0.20±0.06a 24.21±3.78a 0.72±0.17bc 193.24±28.13a HFD 0.22±0.05a 17.77±1.32b 1.10±0.14a 168.50±31.90a PCI 0.25±0.08a 22.03±4.83ab 1.05±0.31abc 172.57±32.43a HDC 0.22±0.03a 21.86±5.46ab 0.75±0.14b 192.50±21.15a GSH-Px活力/(U/mg)MDA含量/(nmol/mg)
由表7可知,与NC组相比,HFD组大鼠脑组织GSH-Px活力显著降低(P<0.05),MDA含量显著升高(P<0.05),SOD活力虽低于NC组,但没有统计学差异(P>0.05)。与HFD组相比,HDC组MDA含量显著降低 P<0.05)。
2.5 大鼠肠道菌群物种丰度及多样性
2.5.1 分类单元聚类分析
分类单元(operational taxonomic units,OTU)交集维恩图见图4。

图4 OTU交集维恩图
Fig.4 Venn diagram of OTU
试验以OTU相似性为97%对11个样本进行了OTU 分析,其中 NC 组(NC1~NC2),HFD 组(HFD1~HFD3)、PCI组(PCI1~PCI3)、HDC 组(HDC1~HDC3)。图4可以看出,4组OTU 分别为 626、692、673、656个。共有的为527个。
2.5.2 Alpha多样性分析
图5为大鼠肠道菌群Alpha多样性曲线。

图5 大鼠肠道微生物的Alpha多样性曲线
Fig.5 Alpha diversity curve of intestinal microorganisms in rats
(a)稀释曲线;(b)Shannon曲线;(c)Specaccum物种积累曲线。
由图5(a)可以看出,随着抽样数量的增加,测得的OTU数量先增大,后趋于平缓。说明已经获得环境中绝大多数细菌序列,物种不会随着测序数量的增加产生明显的变化。从图5(b)可知,曲线逐渐趋于平缓状态,尽管增加抽样数量可以提高OTU数量,但是不会改变物种多样性。从图5(c)可以看出,随着样本量的增大,OTU数量从快速增加到趋于稳定,此时肠道菌群数量不再增多,所以此时的数据量可以用于后续实验。
图6和表8为各个样品Alpha多样性分析。
表8 肠道微生物Alpha多样性分析
Table 8 Alpha diversity of gut micrabiota

注:不同小写字母表示差异显著(P<0.05)。
组别 chao1指数 物种丰富度指数Shannon指数NC 594.65±11.50a 536.50±12.02a41.46±0.67a 5.89±0.09b HFD 645.60±31.94a 595.33±37.29a43.20±2.29a 6.89±0.39a PCI 600.13±29.72a 547.93±46.32a 41.14±3.06a 6.37±0.54ab HDC 626.77±27.09a 540.33±44.84a40.57±2.43a 5.95±0.47b PD_whole_tree指数

图6 Alpha多样性指数
Fig.6 Alpha diversity index
从图6和表8可以看出,HFD组大鼠的肠道菌群chao1指数最大,即肠道菌群丰度最高,但不存在显著性差异;HFD组大鼠肠道菌群Shannon指数显著高于NC、HDC组(P<0.05);即HFD组大鼠肠道微生态多样性明显高于NC、HDC组,原因可能是高脂饮食改变了肠道生态,有害菌过度繁殖,使肠道菌群多样性增加[17]。HDC组大鼠肠道菌群的丰富度以及多样性更接近于NC组。
2.5.3 Beta多样性分析
Beta多样性分析可以反映不同样本之间的菌群组成差异。图7为4组大鼠肠道菌群的组成,图中的点表示个体菌群,点与点之间的距离反映菌群之间的序列相似度。

图7 基于PLS-DA的4组大鼠肠道菌群组成分析
Fig.7 Composition of intestinal flora of four groups of rats based on PLS-DA
从图7中可以看出,HFD组大鼠的肠道菌群构成与NC组差别较大。PCI组与HDC组大鼠的肠道菌群构成与NC组相近,其中HDC组更接近正常大鼠。说明该复配物对肠道菌群具有正向调节作用。
2.6 大鼠肠道菌群结构分析
2.6.1 门水平差异分析
大鼠肠道菌群结构在门水平的差异见图8。

图8 大鼠肠道菌群结构在门水平的差异
Fig.8 Microbial community structure at the phylum level
由图8可知,在门水平上,大鼠肠道中最多的是厚壁菌门,其次是拟杆菌门。HDC组大鼠肠道内的放线菌门(16.41±1.81)%显著高于 HFD 组(8.6±1.72)%(P<0.05)。HDC组拟杆菌门丰度较NC组和HFD组有下降的趋势,但不存在显著性差异。
2.6.2 属水平差异分析
大鼠肠道菌群结构在属水平的差异见图9。

图9 大鼠肠道菌群结构在属水平的差异
Fig.9 Microbial community structure at the genus lev
由图9可知,在属水平上,NC组大鼠肠道中菌属相对丰度由高到低为 Lactobacillus、Romboutsi、Rumino-coccaceae UCG-014、Ruminococcus1、Ruminococcaceae NK4A214_group等。HFD 组(10.7±4.23)%、PCI组(4.40±1.11)%的乳酸菌相对丰度较 NC组(37.71±0.63)%均极显著降低(P<0.01);与HFD相比,HDC组Alistipes、螺杆菌、脱硫弧菌属含量分别降低0.10%、0.34%、0.50%,Dorea、志贺氏菌含量均降低0.11%;双歧杆菌、乳酸菌、乳球菌含量分别增加3.06%、9.12%、0.04%。
3 讨论与结论
本实验提取黑木耳多糖的单糖组成与庄伟等[7]的研究结果基本相符。结合已有的研究,黑木耳多糖的单糖组成与黑木耳来源相关,不同品种的黑木耳的单糖组成不同[18]。黑木耳多糖作为益生元,可有效促进乳酸菌的增殖[19]。薛依婷等[20]研究发现黑木耳多糖促进了酸乳中保加利亚乳杆菌、嗜热链球菌、干酪乳杆菌的繁殖,并提高了酸乳中游离脂肪酸和胞外多糖的含量。Zhang等[21]研究发现黑木耳多糖的干预逆转了高脂血症大鼠中乳酸杆菌和Oscillibacter丰度下降的趋势。本实验将不同浓度的黑木耳多糖与乳酸菌共培养,培养过程中发现,当乳酸菌与30%黑木耳多糖共培养至8 h时,采用考马斯亮蓝法测定溶液中蛋白质浓度(114.48 mg/L)与空白组相比明显提高。考马斯亮蓝法(Bradford法)测定溶液中的蛋白质含量,其工作原理为染料考马斯亮蓝G-250与蛋白质中的碱性氨基酸或芳香族氨基酸结合,在595 nm波长下有最大光吸收[22]。因此推测,随着培养时间的延长,黑木耳多糖提高乳酸菌蛋白酶类的代谢水平,促进溶液中蛋白质的降解,使得特征氨基酸充分暴露出来并与染料结合,进而提高了其吸光度。
高脂饮食可以调节大鼠肠道菌群结构,从而对机体的健康产生影响。本研究中发现,高脂饮食大鼠肠道菌群与空白组相比产生了明显的差异,肠道中的有害菌增加,如志贺氏菌、螺杆菌、β-变形菌纲、伯克霍尔德氏菌目、梭菌属、粪球菌属等;有益菌的相对丰度降低,如乳酸杆菌、双歧杆菌等。将黑木耳多糖与银耳多糖和山楂黄酮复配后,对高脂饮食大鼠进行干预,观察到大鼠的肠道菌群结构发生变化,其结构向正常大鼠的肠道菌群结构转变,有害菌减少,乳酸菌等有益菌的增多。这与Zhang等[21]的研究结果一致。其原因可能是黑木耳多糖影响了乳酸菌的蛋白质水解系统,增强了胞外蛋白酶活性,促进了蛋白质水解为多肽。多肽通过乳酸菌的多肽转运系统进入细胞,促进了乳酸菌的代谢水平。乳酸菌进一步抑制肠道有害菌,改善肠道菌群结构,并调节宿主代谢[23-25]。另一方面,在蛋白质水解过程中还可以产生其它分子,如与乳酸菌益生作用相关的生物活性肽[26]。
综上所述,黑木耳多糖对乳酸菌的代谢产物具有一定的调节作用,并且黑木耳多糖复配物对高脂饮食造成的肠道菌群紊乱具有调节恢复作用,同时可以在一定程度上增强机体的抗氧化能力。
[1] LUO Y C,CHEN G,LI B,et al.Evaluation of antioxidative and hypolipidemic properties of a novel functional diet formulation of Auricularia auricula and hawthorn[J].Innovative Food Science&Emerging Technologies,2009,10(2):215-221.
[2] 王献友,陈培云,吴广臣,等.黑木耳多糖提取及其药理活性的研究进展[J].南方农业学报,2012,43(5):683-687.WANG Xianyou,CHEN Peiyun,WU Guangchen,et al.Advances on polysaccharide extraction from Auricularia auricula and its pharmacological activity[J].Journal of Southern Agriculture,2012,43(5):683-687.
[3] 罗敬文,司风玲,顾子玄,等.3种木耳多糖的抗氧化活性与抑菌能力比较分析[J].食品科学,2018,39(19):64-69.LUO Jingwen,SI Fengling,GU Zixuan,et al.Antioxidant and antimicrobial activities of polysaccharides from three species of Auricularia[J].Food Science,2018,39(19):64-69.
[4]SONG G L,DU Q Z.Structure characterization and antitumor activity of an α β -glucan polysaccharide from Auricularia polytricha[J].Food Research International,2012,45(1):381-387.
[5]CHAKRABORTY I,SEN I K,MONDAL S,et al.Bioactive polysaccharides from natural sources:A review on the antitumor and immunomodulating activities[J].Biocatalysis and Agricultural Biotechnology,2019,22:101425.
[6] LIU L Q,LI M Z,YU M L,et al.Natural polysaccharides exhibit anti-tumor activity by targeting gut microbiota[J].International Journal of Biological Macromolecules,2019,121:743-751.
[7] 庄伟,屈咪,赵迪,等.黑木耳多糖的结构组成及其免疫活性研究[J].食品科技,2020,45(2):205-210.ZHUANG Wei,QU Mi,ZHAO Di,et al.Structual composition and immunomodulatory activities of polysaccharides from Auricularia auricula[J].Food Science and Technology,2020,45(2):205-210.
[8] 刘雪姬,陈庆森,闫亚丽.高脂饮食对小鼠肠道菌群的影响[J].食品科学,2011,32(23):306-311.LIU Xueji,CHEN Qingsen,YAN Yali.Effect of high fat diet on intestinal flora in mice[J].Food Science,2011,32(23):306-311.
[9] 刘荣瑜,王昊,张子依,等.多糖与肠道菌群相互作用的研究进展[J/OL].食品科学,2021:1-15(2021-02-05)[2021-03-10].http://kns.cnki.net/kcms/detail/11.2206.TS.20210205.1625.043.html.LIU Rongyu,WANG Hao,ZHANG Ziyi,et al.Progress on interaction of polysaccharides with intestinal flora[J/OL].Food Science,2021:1-15(2021-02-05)[2021-03-10].http://kns.cnki.net/kcms/detail/11.2206.TS.20210205.1625.043.html.
[10]ZHAO R Q,CHENG N H,NAKATA P A,et al.Consumption of polysaccharides from Auricularia auricula modulates the intestinal microbiota in mice[J].Food Research International,2019,123:383-392.
[11]LI Y Q,MA Q T,WANG J K,et al.Relationship between hyperlipidemia and the gut microbiome of rats,characterized using highthroughput sequencing[J].Journal of Traditional Chinese Medical Sciences,2020,7(2):154-161.
[12]田建军.高效降胆固醇乳酸菌的筛选及其在发酵乳中的应用[D].呼和浩特:内蒙古农业大学,2006.TIAN Jianjun.Screening of Lactobacillus for efficient cholesteroldegrading and its application in fermented milk[D].Hohhot:Inner Mongolia Agricultural University,2006.
[13]张一帆,张智,魏志艳,等.四种方法提取灵芝粗多糖的得率比较试验[J].食用菌,2010,32(6):58-60.ZHANG Yifan,ZHANG Zhi,WEI Zhiyan,et al.Comparative experiment on the yield of crude polysaccharides from Ganoderma lucidum by four methods[J].Edible Fungi,2010,32(6):58-60.
[14]莫开菊,赵娜,朱照武,等.葛仙米多糖的单糖组成分析[J].食品科学,2015,36(18):89-92.MO Kaiju,ZHAO Na,ZHU Zhaowu,et al.Analysis of monosaccharide composition of polysaccharide from Nostoc sphaeroides kützing[J].Food Science,2015,36(18):89-92.
[15]王孝平,邢树礼.考马斯亮蓝法测定蛋白含量的研究[J].天津化工,2009,23(3):40-42.WANG Xiaoping,XING Shuli.Determination of protein quantitation using the method of coomassie brilliant blue[J].Tianjin Chemical Industry,2009,23(3):40-42.
[16]吕锡斌,吴耀领,郝飞,等.高通量测序技术分析酱香型白酒下造沙轮次的微生物多样性[J].酿酒科技,2019(3):52-58,64.LÜ Xibin,WU Yaoling,HAO Fei,et al.Analysis of microbial diversity in the 1st and 2nd fermentation cycle of Jiangxiang baijiu based on high throughput sequencing technology[J].Liquor-Making Science&Technology,2019(3):52-58,64.
[17]陈见容.大豆源甾醇干预对仓鼠肠道菌群及胆固醇代谢影响[D].天津:天津科技大学,2018.CHEN Jianrong.Effect of soybean source of sterols on intestinal flora and cholesterol metabolism in hamsters[D].Tianjin:Tianjin University of Science&Technology,2018.
[18]XU S Q,ZHANG Y J,JIANG K.Antioxidant activity in vitro and in vivo of the polysaccharides from different varieties of Auricularia auricula[J].Food&Function,2016,7(9):3868-3879.
[19]FARAKI A,NOORI N,GANDOMI H,et al.Effect of Auricularia auricula aqueous extract on survival of Lactobacillus acidophilus La-5 and Bifidobacterium bifidum Bb-12 and on sensorial and functional properties of synbiotic yogurt[J].Food Science&Nutrition,2020,8(2):1254-1263.
[20]薛依婷,白红霞,李明杰,等.黑木耳多糖凝固型酸奶发酵工艺优化[J].食品工业科技,2020,41(16):156-162.XUE Yiting,BAI Hongxia,LI Mingjie,et al.Optimization of fermentation process of set yogurt with Auricularia auricula polysaccharide[J].Science and Technology of Food Industry,2020,41(16):156-162.
[21]ZHANG T T,ZHAO W Y,XIE B Z,et al.Effects of Auricularia auricula and its polysaccharide on diet-induced hyperlipidemia rats by modulating gut microbiota[J].Journal of Functional Foods,2020,72:104038.
[22]陈金斌,芮鸿飞,方佳宁,等.糯米蛋白质与黄酒氨基酸的相关性分析[J].酿酒科技,2017(4):51-56.CHEN Jinbin,RUI Hongfei,FANG Jianing,et al.Analysis of the correlations between amino acid content in yellow rice wine and protein content in glutinous rice[J].Liquor-Making Science&Technology,2017(4):51-56.
[23]ZHANG C H,ZHANG M H,WANG S Y,et al.Interactions between gut microbiota,host genetics and diet relevant to development of metabolic syndromes in mice[J].The ISME Journal,2010,4(2):232-241.
[24]KUUGBEE E D,SHANG X Q,GAMALLAT Y,et al.Structural change in microbiota by a probiotic cocktail enhances the gut barrier and reduces cancer via TLR2 signaling in a rat model of colon cancer[J].Digestive Diseases and Sciences,2016,61(10):2908-2920.
[25]COLLADO M C,MERILUOTO J,SALMINEN S.Role of commercial probiotic strains against human pathogen adhesion to intestinal mucus[J].Letters in Applied Microbiology,2007,45(4):454-460.
[26]白凤翎,张柏林,赵宏飞.乳酸菌蛋白代谢研究进展[J].食品科学,2010,31(19):381-384.BAI Fengling,ZHANG Bolin,ZHAO Hongfei.Progress in protein metabolism of lactic acid bacteria[J].Food Science,2010,31(19):381-384.