姜黄色素是从姜科、天南星科中的一些植物根茎中提取的一种天然多酚类化合物,具有明亮的黄色,粉末呈橙黄色结晶状,亦称“郁金黄色素”。它具有β-二酮的庚二烯和两个邻甲基化的酚相连组成的对称分子结构,味稍苦[1],着色力强,毒性小,长时间以来作为一种常用的天然色素被普遍使用于食品、纺织、化妆品等产品上。近年来许多学者研究发现姜黄素具有抗氧化(延缓衰老)[2-4]、抗炎[5]、抗肿瘤[6]、抗突变、抗抑郁、抗病毒、心血管保护、修复脑部损伤、缓解帕金森症状等多种药理和保健作用[7-10],因此姜黄素有望作为功能性色素应用于功能性食品上。但由于姜黄素易受外界因素影响失去其本身的颜色,尤其在室外光照下,姜黄素水溶液极其不稳定,产生降解反应,失去原来的药理作用和颜色,这就限制了姜黄素在液体食品中产业化开发与应用。有研究报道将其制成纳米脂质体后,可显著改善其水溶性,提高生物利用度[11-12],刘延敏等[13]通过熔融速冷及室温冷却的方法,制备了姜黄素的固体分散体,并发现其体外溶出度远远高于纯姜黄素;葛云龙等[14]使用反溶剂法制备的姜黄素纳米粒冻干粉能够改善姜黄素水溶性,提高姜黄素的生物利用度。但鲜见改善其光敏性的研究报道。
改善天然色素稳定性的方法有添加稳定剂[15]、微胶囊化[16]、色素分子结构修饰[17]、改善天然色素加工储存条件[18]等。其中微胶囊技术是提高天然色素稳定性的一种较为有效的方法。周丹红等[19]以阿拉伯胶、β-环糊精、蔗糖(1∶1∶1,质量比)作为复合壁材对苋菜红色素进行微胶囊化处理,提高了该色素的贮存稳定性;韩爱芝等[20]以阿拉伯树胶和β-环糊精为壁材,采用喷雾干燥法包埋花色苷,发现可以降低花色苷对外界条件的敏感性。李宛陶等[21]以灵武长枣枣皮红色素为原料,探讨了常见金属离子对枣皮红色素稳定性的影响,结果发现低浓度的Zn2+有利于枣皮红色素的稳定性。前期试验发现加入0.1%植酸作为抗氧化剂,0.1 g/LZn2+溶液、0.1%的柠檬酸溶液作为稳定剂都有利于改善姜黄素溶液对光的稳定性。本文利用添加稳定剂和微胶囊化联用制备姜黄素纳米颗粒(玉米醇溶蛋白-阿拉伯胶-姜黄素分散体系)来改善姜黄素的光敏性,确定了姜黄素纳米颗粒的最优制备工艺,解决姜黄素应用于液体食品中的褪色问题。
1 材料与方法
1.1 试验材料
1.1.1 材料与试剂
姜黄素粉末(食品级,纯度37.98%):珠海雅富兴源食品工业有限公司;姜黄素标品(一级标准品,纯度98%):上海远慕生物科技公司;玉米醇溶蛋白(食品级):市售;阿拉伯胶(食品级):河南唐古生物科技有限公司;硫酸锌(分析纯):天津市福晨化学试剂厂。
1.1.2 主要仪器与设备
SHE-3000G全波长多功能酶标仪分析仪:上海美谱达仪器有限公司;FD-1E-50冷冻干燥机:上海豫明仪器有限公司;iCAP Q ICP-MS电感耦合等离子体质谱仪、1510酶标仪:美国赛默飞世尔科技有限公司;LS-POP(9)激光粒度分析仪:珠海欧美克仪器有限公司;JB-3数显恒温磁力搅拌器:常州荣华仪器制造有限公司。
1.2 试验方法
1.2.1 姜黄素最大吸收波长及回归方程
最大吸收波长:准确称取0.01 g姜黄素粉末样品于100 mL容量瓶中,用95%乙醇定容,得到浓度为0.1 mg/mL的姜黄素溶液,从中移取500 μL用95%乙醇溶液定容到100 mL,得到浓度为0.5 μg/mL的姜黄素溶液,调节波长,测定在不同波长下姜黄素的吸光值,以波长为横坐标,吸光度为纵坐标,确定姜黄素的最大吸收波长为425 nm。
回归方程:准确称取姜黄素标准品25 mg于50 mL容量瓶中,用95%乙醇定容,分别稀释得到0、15、30、45、60、75 μg/mL 的标准溶液,425 nm 处测定吸光度,以浓度X对吸光度Y进行线性回归。标准曲线的回归方程为Y=0.316 8X+0.634 9,R2=0.997 4,姜黄素浓度在0~75 μg/mL范围内,线性关系良好。
1.2.2 稳定剂锌离子最适作用浓度筛选
姜黄素母液的配制:称取0.175 g姜黄素溶解于280 mL的无水乙醇中,搅拌至姜黄素粉末完全溶解。
不同锌离子浓度储备液的配制:分别称取硫酸锌0.03、0.06、0.09、0.12、0.15、0.18 g 溶解于 100 mL 蒸馏水中,搅拌均匀,配制成 0.3、0.6、0.9、1.2、1.5、1.8 g/L 硫酸锌储备溶液,保存好备用。
锌离子最适浓度筛选试验:将姜黄素母液分装成40 mL的7份样液,在1~7号样液中分别加入10 mL的 0.0、0.3、0.6、0.9、1.2、1.5、1.8 g/L 硫酸锌储备液,搅拌均匀得到硫酸锌浓度分别为 0.00、0.06、0.12、0.18、0.24、0.30、0.36 g/L 的样液,(20±5)℃放置。每隔 12 h在425 nm波长处用酶标仪测定吸光度,平行3次取平均值。
1.2.3 姜黄素纳米颗粒制备操作要点
1.2.3.1 玉米醇溶蛋白-姜黄素储备液的制备
称取1 g玉米醇溶蛋白溶解于50 mL 85%乙醇中,磁力搅拌1 h,离心去除不溶物作为玉米醇溶蛋白液,加入0.108 g姜黄素于玉米醇溶蛋白液中搅拌30 min。
玉米醇溶蛋白特有的两亲性和独特溶解性,能够有效制备纳米颗粒,且复合阿拉伯胶的玉米醇溶蛋白纳米颗粒的稳定性、耐盐耐酸碱性显著提高[22]。试验按玉米醇溶蛋白与阿拉伯胶8∶10的质量比称取阿拉伯胶溶解于150 mL0.4 g/L硫酸锌溶液(水浴加热60℃溶解),搅拌至完全溶解。
1.2.3.2 姜黄素纳米颗粒的制备
将玉米醇溶蛋白-姜黄素储备液缓慢加入阿拉伯胶中搅拌30 min后得(姜黄素-玉米醇溶蛋白-阿拉伯胶)纳米颗粒液,对其旋转蒸发浓缩、冷冻干燥得到姜黄素纳米颗粒。
1.2.4 姜黄素纳米颗粒制备单因素试验
以包埋率为考察指标,分析水相与醇相体积比、壁材比(阿拉伯胶与玉米醇溶蛋白质量比)、芯壁比(姜黄素与玉米醇溶蛋白-阿拉伯胶质量比)对姜黄素纳米颗粒包埋率的影响,确定3个因素的最适作用条件。
水相与醇相体积比:玉米醇溶蛋白1 g、姜黄素0.02 g、阿拉伯胶1 g、85%乙醇50 mL,硫酸锌0.3 g/L(以总体积算),蒸馏水与乙醇体积比为 1.5∶1、2∶1、2.5∶1、3∶1、3.5∶1,按 1.2.3.2 操作制备姜黄素纳米颗粒,确定水相与醇相体积的最适比例。
壁材比(阿拉伯胶与玉米醇溶蛋白质量比)∶玉米醇溶蛋白1 g、姜黄素0.02 g、蒸馏水75 mL、85%乙醇50 mL、硫酸锌0.3 g/L(以总体积算)、阿拉伯胶与玉米醇溶蛋白质量比为 2∶10、4∶10、6∶10、8∶10、10∶10,按1.2.3.2操作制备姜黄素纳米颗粒,确定最适壁材比。
芯壁比(姜黄素与玉米醇溶蛋白-阿拉伯胶质量比):玉米醇溶蛋白1 g、阿拉伯胶1 g、85%乙醇 50 mL、硫酸锌0.3 g/L(以总体积算)、蒸馏水75 mL,姜黄素与玉米醇溶蛋白-阿拉伯胶质量比 5.5∶100、6∶100、6.5∶100、7∶100、7.5:100,按 1.2.3.2 操作制备姜黄素纳米颗粒,确定最适芯壁比。
1.2.5 姜黄素纳米颗粒包埋率的测定
移取1 mL负载姜黄素的纳米颗粒置于有4 mL 95%乙醇溶液的烧杯中,超声15 min萃取获得游离的姜黄素,用0.22 μm尼龙膜过滤,反复萃取3次,合并萃取液。以95%乙醇作为空白对照,在425nm下测定样品的吸光度,使用姜黄素在95%乙醇中的标准曲线方程,计算出游离姜黄素后,按照下式计算包埋率、载药量。

1.2.6 姜黄素纳米颗粒粒径测定
将样品稀释一定的倍数,置于样品池中,使用激光粒度仪测量其粒径。
1.2.7 姜黄素纳米颗粒对光稳定性试验
将样品稀释4倍,(20±5)℃放置,每24 h使用酶标仪测量一次吸光度值,观察微胶囊技术对姜黄素光敏性的影响。以反应时间t为横坐标,以姜黄素的保留率为纵坐标,绘制光解反应图,观察纳米颗粒对姜黄素光敏性的影响。以保留率表示对光的稳定性。
式中:At为室温(20±5)℃下不同时间段测得的样品吸光度;A1为开始时测得的样品吸光度。
1.2.8 多指标综合平衡法
多指标综合平衡法是指在正交试验结果分析中先分别考察每个因素对各指标的影响,然后进行分析比较,确定出最好的水平,从而得到最好的试验方案[23]。
光稳定性评分:1-(A第1天-A第7天)/A第1天;粒径评分:1-粒径,分值越大越好。
1.2.9 数据分析
数据以平均值±标准差表示,正交试验数据使用正交设计助手处理,采用SPSS 22.0 for Windows软件进行方差分析,p<0.05表示有统计学意义,使用GraphPad Prism 7.04、Origin 9作图。
2 结果与分析
2.1 稳定剂锌离子最适作用浓度确定
锌离子最适作用浓度筛选结果见图1。
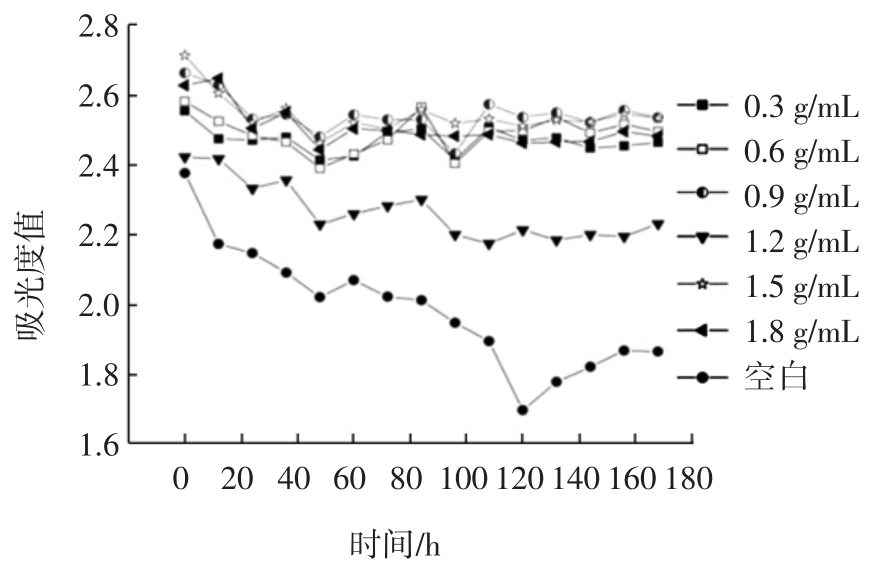
图1 锌离子最适作用浓度筛选
Fig.1 Screening of optimal concentration of Zn2+
由图1可知,不同浓度的锌离子加入姜黄素溶液中在0~48 h内,姜黄素都在褪色,但比不加锌离子的稳定;48 h~60 h,加入不同浓度的锌离子姜黄素溶液的吸光度都增加;60 h后,加入0.3 g/L锌离子的姜黄素溶液斜率最小,且吸光度较为稳定。因此选择锌离子作用浓度为0.3 g/L。
2.2 姜黄素纳米颗粒制备单因素试验
水相与醇相体积比试验结果见图2。
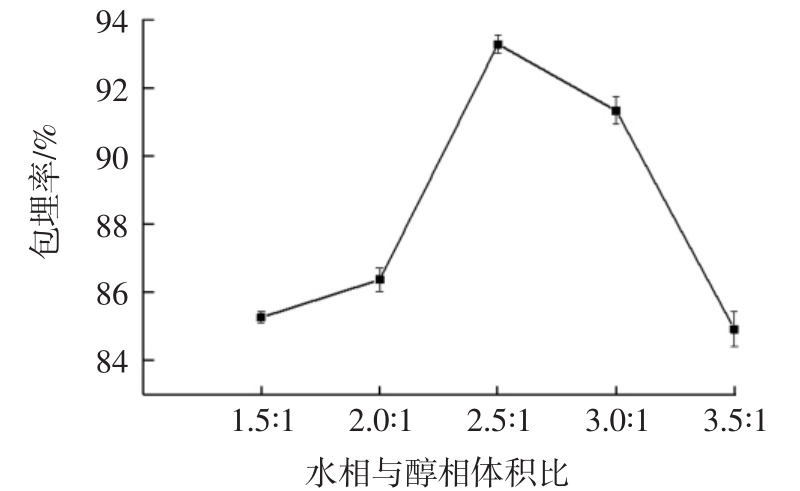
图2 水相与醇相体积比对包埋率的影响
Fig.2 Effect of volume ratio of aqueous phase to ethanol phase on embedding rate
由图2可知,水相与醇相的体积比从1.5∶1到2.5∶1时,包埋率从85.495%上升到93.227%,继续增加到3.5∶1时,包埋率下降至84.900%。可能是随着水相与醇相的体积比增加,醇相的浓度下降,姜黄素溶解达到过饱和状态,在沉积过程中,姜黄素部分析出,导致包埋率下降,因此确定最适水相与醇相体积比为2.5∶1。阿拉伯胶与玉米醇溶蛋白质量比试验结果见图3。
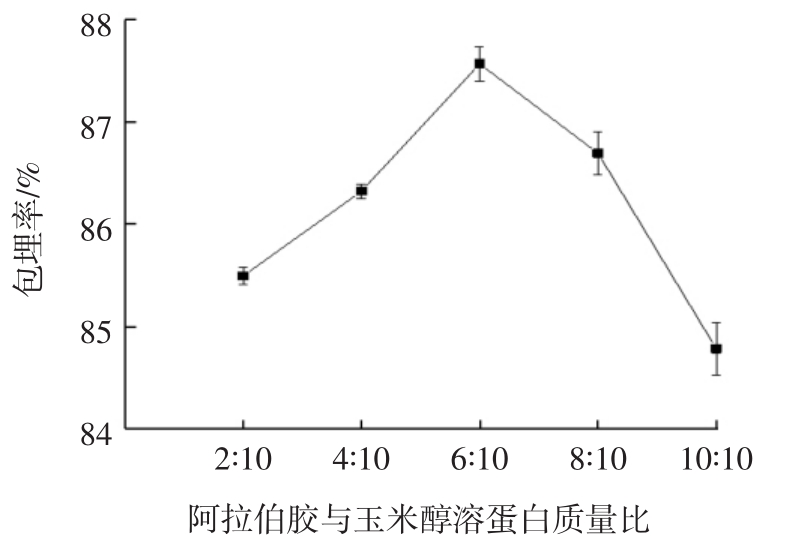
图3 阿拉伯胶与玉米醇溶蛋白质量比对包埋率的影响
Fig.3 Effect of mass ratio of Arabic gum to zein on embedding rate
由图3可知,随着阿拉伯胶与玉米醇溶蛋白质量比从2∶10到6∶10,包埋率从85.495%上升到87.567%,之后包埋率开始下降。由于此时阿拉伯胶与玉米醇溶蛋白所带的电荷完全中和,包埋率最大,之后阿拉伯胶的继续增加导致电荷失衡,致包埋率下降。因此确定最适壁材比为6∶10(质量比)。姜黄素与玉米醇溶蛋白-阿拉伯胶质量比对包埋率的影响见图4。
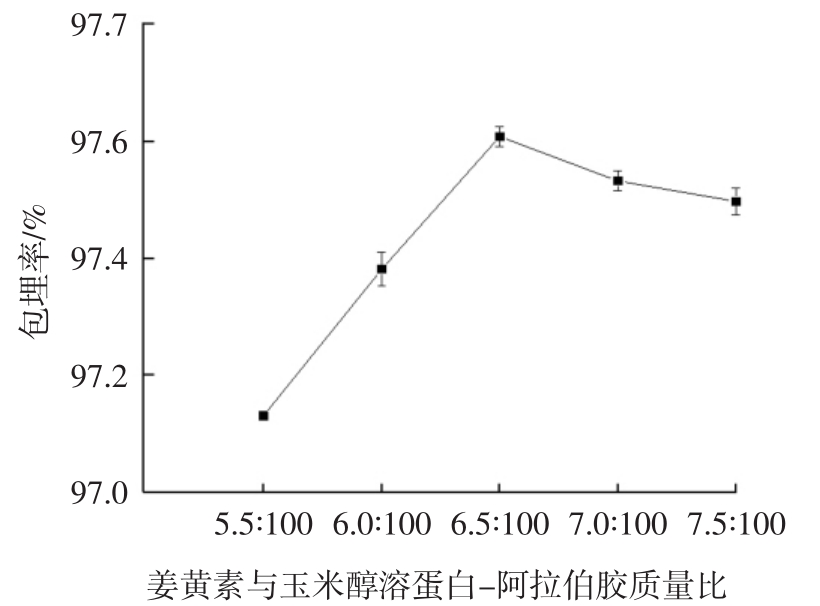
图4 姜黄素与玉米醇溶蛋白-阿拉伯胶质量比对包埋率的影响
Fig.4 Effect of mass ratio of curcumin to zein-Arabic gum on embedding rate
由图4可知,当姜黄素与玉米醇溶蛋白-阿拉伯胶质量比从5.5∶100到6.5∶100时,包埋率从97.130%上升到97.608%,增至7.5∶100时,包埋率下降。可能是当姜黄素与玉米醇溶蛋白-阿拉伯胶质量比为6.5∶100时,壁材的荷载量达到最大负荷,之后比例增加导致游离的姜黄素的量增加,致包埋率下降,因此确定最适芯壁比为 6.5∶100(质量比)。
2.3 姜黄素纳米颗粒制备正交试验
在单因素试验考察基础上,采用L9(34)正交试验对水相与醇相体积比、壁材比、芯壁比3个因素工艺条件进行优化,以包埋率、光稳定性评分、粒径评分为考察指标,使用多指标综合平衡法确定最优工艺。正交试验结果见表1,以光稳定性评分为考察指标的方差分析结果见表2,以包埋率为考察指标的方差分析结果见表3,以粒径评分为考察指标的方差分析结果见表4,不同指标最优组合比较结果见表5。
优组合为A3B3C3,即水相与醇相体积比3∶1,壁材比(阿拉伯胶∶玉米醇溶蛋白)为 8∶10(质量比),芯壁比(姜黄素∶玉米醇溶蛋白-阿拉伯胶)7∶100(质量比),经验证试验得在最优工艺条件下姜黄素纳米颗粒包埋率为95.844%,载药量为 62 mg/g,粒径为 0.940 μm。
表1 姜黄素纳米颗粒制备L9(34)正交试验结果
Table 1L9(34)orthogonal results of preparation of curcumin nanoparticles

试验号 因素 光稳定性评分 包埋率/% 粒径评分A水醇体积比 B壁材质量比 C芯壁质量比 空列1 1(2∶1) 1(4∶10) 1(6∶100) 1 0.32 95.179 -0.717 2 1 2(6∶10) 2(6.5∶100) 2 0.19 96.191 -0.729 3 1 3(8∶10) 3(7∶100) 3 0.27 96.730 0.060 4 2(2.5∶1) 1 2 3 0.34 94.298 -0.150 5 2 2 3 1 0.23 95.426 0.354 6 0.33 96.156 0.105 7 3(3∶1) 1 3 2 0.49 93.708 0.175 8 3 2 1 3 0.40 94.735 0.050 2 3 1 2 9 3 3 2 1 0.36 95.844 0.004 k1 0.260 0.383 0.350 0.303 k2 0.300 0.273 0.297 0.337 k3 0.417 0.320 0.330 0.337极差R 0.157 0.110 0.053 0.034主次因素 A>B>C最优组合 A3B1C1 k1′ 96.033 94.395 95.357 95.483 k2′ 95.293 95.451 95.444 95.352 k3′ 94.762 96.243 95.288 95.254 R′ 1.271 1.848 0.156 0.229主次因素 B>A>C最优组合 B3A1C2 k1" -0.462 -0.231 -0.187 -0.120 k2" 0.103 -0.108 -0.292 -0.150 k3" 0.076 0.056 0.196 -0.013 R" 0.565 0.287 0.488 0.137主次因素 A>C>B最优组合 A2C3B3
表2 以光稳定性评分为考察指标的方差分析结果
Table 2 Variance analysis results with optical stability score as index

注:*p<0.05表示差异显著。
因素 离均差平方和 自由度 均差 F值 显著水平 F检验临界值A 0.04020.02020.000*F0.05(2,2)=19.00 B 0.01820.0099.000F0.10(2,2)=9.00 C 0.004 2 0.002 2.000 e 0.002 2 0.001
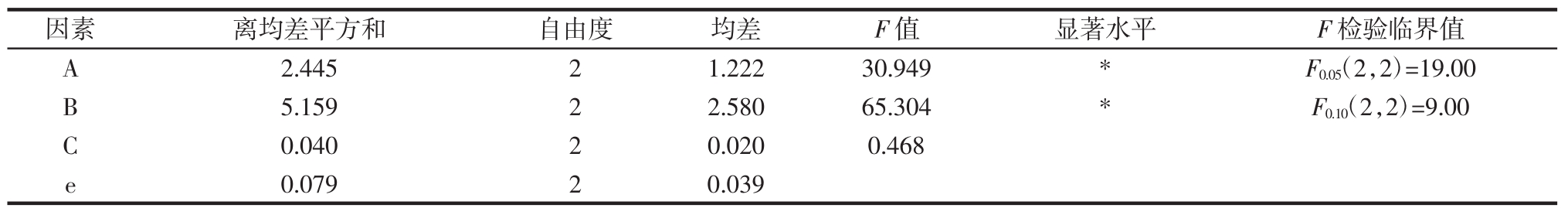
表3 以包埋率为考察指标的方差分析结果
Table 3 Variance analysis results with embedding rate as index
注:*p<0.05表示差异显著。
因素 离均差平方和 自由度 均差 F值 显著水平 F检验临界值A 2.44521.22230.949*F0.05(2,2)=19.00 B 5.15922.58065.304*F0.10(2,2)=9.00 C 0.040 2 0.020 0.468 e 0.079 2 0.039
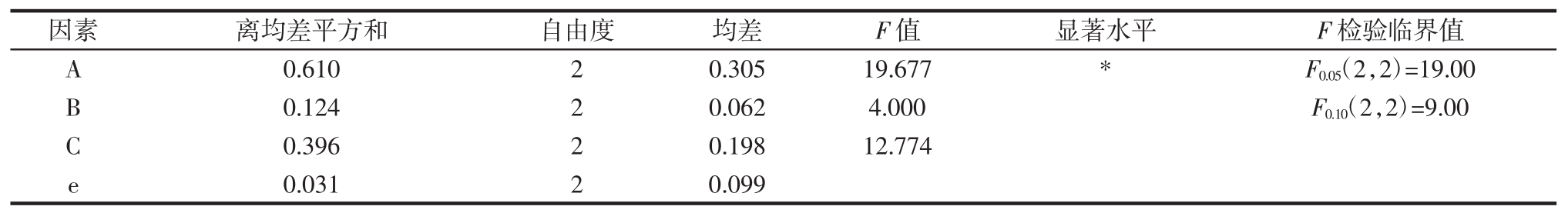
表4 以粒径评分为考察指标的方差分析结果
Table 4 Variance analysis results with particle size score as index
注:*表示差异显著(p<0.05)。
因素 离均差平方和 自由度 均差 F值 显著水平 F检验临界值A 0.61020.30519.677*F0.05(2,2)=19.00 B 0.12420.0624.000F0.10(2,2)=9.00 C 0.396 2 0.198 12.774 e 0.031 2 0.099
表5 不同指标最优组合比较
Table 5 Comparison of optimal combination with different indexes
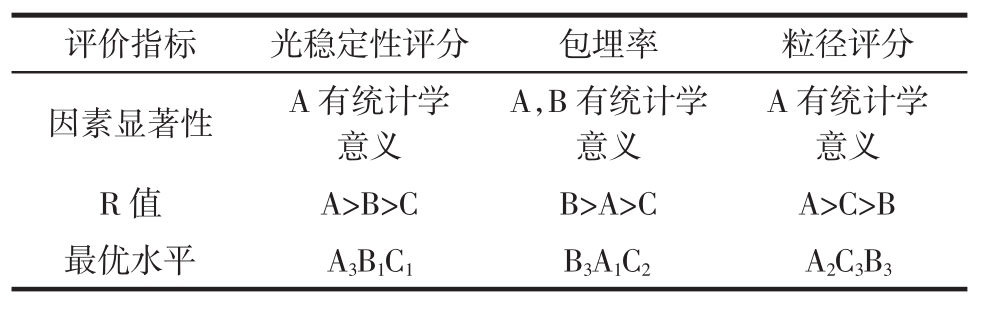
评价指标 光稳定性评分 包埋率 粒径评分因素显著性 A有统计学意义A有统计学意义R 值 A>B>C B>A>C A>C>B最优水平 A3B1C1 B3A1C2 A2C3B3 A,B有统计学意义
由表1、表2、表3、表4、表5可得,因素A对光稳定性评分、包埋率、粒径评分均有显著影响,根据R值,以光稳定性评分为指标时优选A3,以包埋率为指标时优选A1,以粒径评分为指标时优选A2;因素B对包埋率有显著影响,根据R值故选择B3;因素C对3个指标都无显著影响,但因为制备的是纳米颗粒,粒径越小(粒径评分越大)越好,根据R值选择C3。通过多指标综合平衡法分析得出姜黄素纳米颗粒制备的最
2.4 姜黄素纳米颗粒光稳定性试验
姜黄素纳米颗粒在自然光照下的稳定性结果见图5。
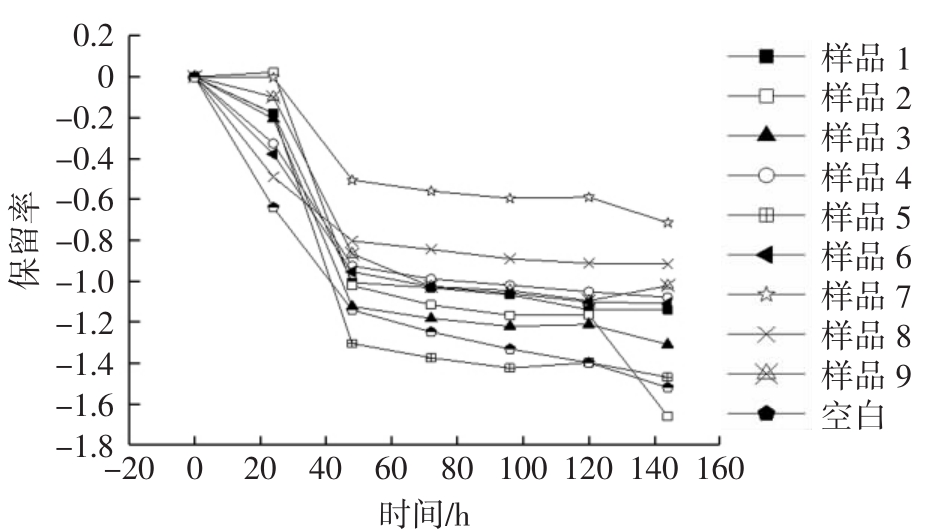
图5 姜黄素纳米颗粒在自然光照下的稳定性
Fig.5 Stability of curcumin nanoparticles under natural light
样品1~样品9对应表1正交试验的9组试验,空白为纯姜黄素样品。
由图5可知,总体来看样品1到样品9,当过了48h后,所有样品的保留率趋于稳定,姜黄素纳米颗粒的姜黄素保留率都比未包埋的要大,因此姜黄素纳米颗粒包埋的姜黄素光解反应比未包埋的要慢。以样品7最为稳定,其在144 h后姜黄素保留率最大(-0.713),姜黄素光解反应最慢。这与许雪儿等[22]的研究结果一致。
3 结论
在姜黄素溶液中加入0.3 g/L的锌离子有助于姜黄素溶液的光稳定性;姜黄素纳米颗粒最优制备工艺:水相与醇相体积比3∶1,壁材比(阿拉伯胶:玉米醇溶蛋白)为 8∶10(质量比),芯壁比(姜黄素∶玉米醇溶蛋白-阿拉伯胶)7∶100(质量比),在此条件下,姜黄素纳米颗粒包埋率为95.844%,载药量为62 mg/g,粒径为0.940 μm;姜黄素纳米颗粒的光解反应比未包埋的姜黄素的光解反应要慢,姜黄素包埋后提高了对光的稳定性。
[1] 王美,傅玉颖,李欣,等.水溶性姜黄色素分散体系的稳定性研究[J].中国食品学报,2018,18(11):34-43.WANG Mei,FU Yuying,LI Xin,et al.Studies on the stability of dispersed system from water-soluble curcumin[J].Journal of Chinese Institute of Food Science and Technology,2018,18(11):34-43.
[2] 李伟锋,蒋建兰.姜黄素药理作用的研究现状[J].中国临床药理学杂志,2017,33(10):957-960.LI Weifeng,JIANG Jianlan.Research status of pharmacological action of curcumin [J].The Chinese Journal of Clinical Pharmacology,2017,33(10):957-960.
[3] LU Y L,WU S M,XIANG B D,et al.Curcumin attenuates oxaliplatin-induced liver injury and oxidative stress by activating the Nrf2 pathway[J].Drug Design,Development and Therapy,2020,14:73-85.
[4] BRONDINO N,RE S,BOLDRINI A,et al.Curcumin as a therapeutic agent in dementia:a mini systematic review of human studies[J].The Scientific World Journal,2014,2014:174282.
[5] HENROTIN Y,PRIEM F,MOBASHERI A.Curcumin:a new paradigm and therapeutic opportunity for the treatment of osteoarthritis:curcumin for osteoarthritis management[J].Springer Plus,2013,2(1):56.
[6] VALLIANOU N G,EVANGELOPOULOS A,SCHIZAS N,et al.Potential anticancer properties and mechanisms of action of curcumin[J].Anticancer Research,2015,35(2):645-651.
[7]HU Y Z,HE Y H,JI J R,et al.Tumor targeted curcumin delivery by folate-modified MPEG-PCL self-assembly micelles for colorectal cancer therapy[J].International Journal of Nanomedicine,2020,15:1239-1252.
[8] 尹芳,王帅,郝越,等.姜黄素的药理学作用及其机制的研究进展[J].河北联合大学学报(医学版),2013,15(6):798-799.YI Fang,WANG Shuai,HAO Yue,et al.Research progress on pharmacological action and mechanism of curcumin[J].Journal of Hebei United University(Health Sciences),2013,15(6):798-799.
[9] 梁桂诚,夏豪.姜黄素的心血管保护作用及其机制的研究进展[J].医学综述,2019,25(2):362-369.LIANG Guicheng,XIA Hao.Research progress in cardiovascular protections and mechanisms of curcumin[J].Medical Recapitulate,2019,25(2):362-369.
[10]雍旭红,陈芊,王强,等.姜黄素抑制帕金森病介导的神经元损伤的药理作用研究[J].华中科技大学学报(医学版),2018,47(3):372-374.YONG Xuhong,CHEN Qian,WANG Qiang,et al.Pharmacological effect of curcumin on neuronal injury induced by Parkinson′s disease[J].Acta Medicinae Universitatis Scientiae et Technologiae Hua-zhong,2018,47(3):372-374.
[11]关延彬,韩冰,田雨冬,等.姜黄素脂质体的制备及质量评价[J].中药材,2019,42(2):385-389.GUAN Yanbin,HAN Bing,TIAN Yudong,et al.Preparation and quality evaluation of curcumin liposomes[J].Journal of Chinese Medicinal Materials,2019,42(2):385-389.
[12]尤宏,何静.新型纳米脂质体包载姜黄素预防多柔比星诱导心肌病的实验研究[J].中国药师,2019,22(3):439-443.YOU Hong,HE Jing.Study on curcumin loaded nano-liposomes in preventing doxorubicin induced cardiomyopathy[J].China Pharmacist,2019,22(3):439-443.
[13]刘延敏,王传胜,韩刚,等.姜黄素固体分散体的制备及体外溶出度测定[J].哈尔滨医科大学学报,2006,40(4):327-328.LIU Yanmin,WANG Chuansheng,HAN Gang,et al.Preparation and in vitro dissolution of curcumin solid dispersion[J].Journal of Harbin Medical University,2006,40(4):327-328.
[14]葛云龙,赵修华,祖元刚,等.姜黄素纳米粒冻干粉的反溶剂法制备工艺优化及溶出特征[J].中草药,2016,47(14):2447-2453.GE Yunlong,ZHAO Xiuhua,ZU Yuangang,et al.Preparation,optimization,and dissolution characteristics of curcumin nanoparticles lyophilized powder by antisolvent method[J].Chinese Traditional and Herbal Drugs,2016,47(14):2447-2453.
[15]陈洁,林华庆,余楚钦,等.辣椒红色素色价与含量的关系及提高稳定性的方法[J].安徽农业科学,2015,43(10):16-18.CHEN Jie,LIN Huaqing,YU Chuqin,et al.Relationship of color value of capsanthin and content and method to improve stability[J].Journal of Anhui Agricultural Sciences,2015,43(10):16-18.
[16]王煜,张玉凤,章慧,等.微胶囊化提高姜黄色素稳定性的研究[J].食品工业科技,2007,28(11):193-195.WANG Yu,ZHANG Yufeng,ZHANG Hui,et al.Study on improving the stability of curcumin by microencapsulation[J].Science and Technology of Food Industry,2007,28(11):193-195.
[17]刘国荣,郜亚昆,辛梦娜,等.醇溶性栀子红色素衍生物的制备及稳定性研究[J].中国食品学报,2019,19(11):150-158.LIU Guorong,GAO Yakun,XIN Mengna,et al.Studies on preparation and stability of alcohol-soluble Gardenia red pigment derivative[J].Journal of Chinese Institute of Food Science and Technology,2019,19(11):150-158.
[18]雷云琛.贮藏条件对浓缩果汁主要色素成分及其抗氧化能力变化的影响[D].长沙:中南林业科技大学,2019.LEI Yunchen.The effects of storage conditions on main pigment components and antioxidant capacity of concentrated fruit juices[D].Changsha:Central South University of Forestry&Technology,2019.
[19]周丹红,王耀,王大山,等.苋菜红色素微胶囊的制备、表征及稳定性研究[J].石家庄学院学报,2016,18(3):19-25.ZHOU Danhong,WANG Yao,WANG Dashan,et al.Studies on amaranth red pigment and its preparation,characterization and stability of microcapsule[J].Journal of Shijiazhuang University,2016,18(3):19-25.
[20]韩爱芝,蒋卉,贾清华,等.响应面试验优化黑果枸杞花色苷微胶囊制备工艺及其稳定性分析[J].食品科学,2016,37(10):82-87.HAN Aizhi,JIANG Hui,JIA Qinghua,et al.Optimization of microencapsulation of anthocyanins from Lycium ruthenicum murr.by response surface methodology and stability of the microcapsules[J].Food Science,2016,37(10):82-87.
[21]李宛陶,邵佩兰,贺晓光,等.金属离子对枣皮红色素稳定性的影响[J].食品工业,2016,37(5):155-158.LI Wantao,SHAO Peilan,HE Xiaoguang,et al.Effect of metal ions on the stability of red pigment of jujube peel[J].The Food Industry,2016,37(5):155-158.
[22]许雪儿,李娟,陈正行,等.玉米醇溶蛋白-阿拉伯胶纳米颗粒的制备及性质表征[J].食品与发酵工业,2018,44(7):179-184.XU Xueer,LI Juan,CHEN Zhengxing,et al.Preparation and characterization of zein-arabic gum nanoparticles[J].Food and Fermentation Industries,2018,44(7):179-184.
[23]张静,马瑛.多指标综合平衡法-正交试验优化九蒸九晒地黄炮制工艺[J].中国药房,2016,27(7):962-965.ZHANG Jing,MA Ying.Optimization of processing technology of nine steaming nine drying of Rehmannia glutinosa by multiple indexes comprehensive balance method-orthogonal test[J].China Pharmacy,2016,27(7):962-965.