随着生活水平的日益提高,人们对健康饮食愈发关注。多糖是一类结构复杂的高分子聚合物,其不仅参与生命体的组成,还具备抗氧化[1]、抗疲劳[2]、抗辐射[3]、抗肿瘤[4]、降血脂[5]、抑制炎症和调节免疫[6]等功能效应,对富含多糖的健康营养食品需求也随之增多。时下科学技术发展迅速,已有越来越多的功能性多糖被逐步开发与利用。
自然界中的多糖主要来自植物、动物和微生物。近年来,微生物多糖具备多种优点且可以通过生物技术途径从廉价的可再生原料中制备,在食品和医药领域开发潜力巨大,因而受到大家的密切关注[7]。微生物多糖包括胞外多糖、胞壁多糖和胞内多糖。其中,微生物胞外多糖因无毒安全、生产周期短、易于分离纯化等特点研究较多,逐渐成为植物和动物等多糖产品的有效替代品[8]。随着研究的推进与发展,微生物胞壁多糖也越发受到瞩目。本文主要围绕细胞外和细胞壁多糖的结构性质与应用进展进行了综述,并对未来的研究方向进行了展望,为进一步开发与利用微生物多糖提供参考。
1 细胞外多糖(exopolysaccharides)
细胞外多糖即胞外多糖(exopolysaccharides,EPS),是微生物在生长过程中的代谢产物之一,通常会在分泌的过程中以荚膜的形式贴合于细胞的表面或者分泌到外部环境中[9]。研究显示,许多EPS具有促进人体健康的作用,加上它们独特的流变学性质,在食品领域成为了良好的乳化剂、稳定剂和增稠剂[10-12]。目前所研究的EPS中,结冷胶、黄原胶和普鲁兰等已在食品工业中广泛使用,此外威兰胶、透明质酸等也展现出了良好的应用前景。
1.1 结冷胶(gellan)
1.1.1 结构特性
结冷胶是自假单胞菌中分离出的EPS的总称,是一种阴离子线性多聚体,由葡萄糖、鼠李糖和葡萄糖醛酸构成其重复单元,具体见图1[13]。
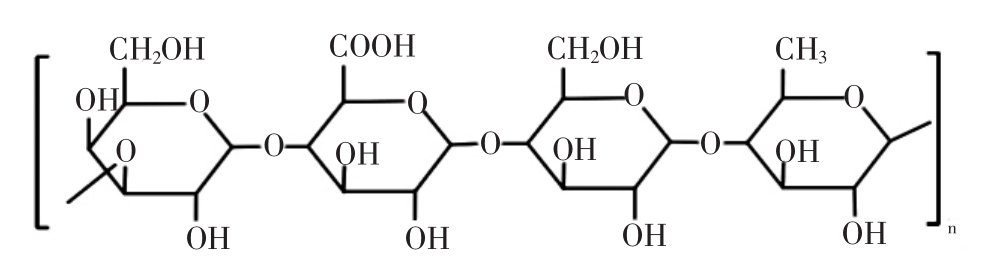
图1 结冷胶的结构组成
Fig.1 The structure formula of gellan
天然结冷胶具备高乙酰基结构,在C-2位置存在甘油基取代基,部分C-6位置还存在乙酰基。在商业生产中,常通过热碱处理发酵液除去两种类型的取代基。结冷胶黏性高,对热和酸稳定,具有良好的抗酶解性,纤维素酶、果胶酶、淀粉酶等均不会对结冷胶的性质产生影响。结冷胶溶于热水,冷凝后可形成水合形式的凝胶,高乙酰基结冷胶形成的凝胶较为柔软富有弹性,脱去乙酰基后产生的胶体刚性更强[13]。结冷胶还可与多价阳离子络合形成透明凝胶,胶凝速率会对其产生影响,研究表明,较低的凝胶化速率可促进结冷胶羧基与阳离子之间的相互作用,对其凝胶强度产生积极影响[14]。
1.1.2 结冷胶的应用状况
结冷胶于食品中广泛应用,在糖果、仿制果酱、果汁、冰激凌和冻类制品中常作为添加剂出现。Xu等[15]研究表明,高乙酰基结冷胶可以赋予蓝莓果汁更高的黏度与更佳的感官特性,并对果汁色泽有一定的保护作用,这与之前Sherafati等[16]在胡萝卜果汁中的研究结论相匹配。
研究显示,通过控制盐离子的浓度可以改变结冷胶凝胶的质地,这种性质与海藻酸钠类似[17],因此结冷胶可用于递送载体的组装。Prezotti等以铝离子为交联剂利用结冷胶和果胶制备缓释性微胶囊,并对白藜芦醇[18]和酮洛芬[19]进行了封装,该微胶囊可以靶向作用于结肠部位并让药物得到持续释放。此外,结冷胶形成的热响应和可逆的物理水凝胶网络在各种环境下都具有较强的稳定性,因此能够替代琼脂作为微生物培养基[20]或在食品和制药工业替代明胶[21];在组织工程中结冷胶也应用广泛,Bonifacio等[22]将结冷胶、甘油与高黏度蜂蜜进行混合,以埃落石纳米管为无机填料,通过上述材料混合形成的水凝胶具有良好的生物相容性与机械性能,可用作软骨修复材料。
1.2 黄原胶(xanthan)
1.2.1 结构特性
黄原胶的结构组成见图2[23]。

图2 黄原胶的结构组成
Fig.2 The structure formula of xanthan
黄原胶主要由黄单胞杆菌产生,主链构成与细菌纤维素相似,均由线性1→4-β-D-葡萄糖单元组成,C-3位置上的每个葡萄糖残基被带电荷的三糖侧链取代,三糖链由两个D-甘露糖与一个D-葡糖醛酸组成,糖醛酸存在于两个甘露糖之间,末端的D-甘露糖单元连接着丙酮酸残基,而与主链连接的D-甘露糖含有一个乙酰基[24]。黄原胶分子间存在较强的氢键作用,拥有高黏度及良好的乳化性,对酸碱稳定,耐高温。与结冷胶相似的是黄原胶也具有较强的抗酶解性,纤维素酶、半纤维素酶和淀粉酶等常见酶都不能有效分解黄原胶。
1.2.2 黄原胶的应用状况
据统计,我国每年黄原胶的产量高达30 000 t,在蛋糕、糖果、罐头、面包、酱料等多种食品中可以作为增稠剂、稳定剂、悬浮剂和改良剂[25];淀粉在加工和贮藏过程中的性状并不稳定,在木薯淀粉中添加黄原胶可以改善产品的流变性与冻融稳定性;黄原胶也能作为一些肉制品的脂肪替代品,具有成为减肥食品的潜质[25]。据报道,食用薄膜和涂层可以降低食品煎炸期间吸油量,一定程度上避免水分的蒸发散失。Sothornvi等[26]将黄原胶与瓜尔豆胶用于香蕉片的涂层,减少了产品油脂的吸收而不影响感官。除了食品,黄原胶在组织工程、医学、化妆品等领域也有大量应用,是目前应用最广泛的胞外多糖。
1.3 热凝胶多糖(curdlan)
1.3.1 结构特性
热凝胶多糖的结构组成见图3[27]。
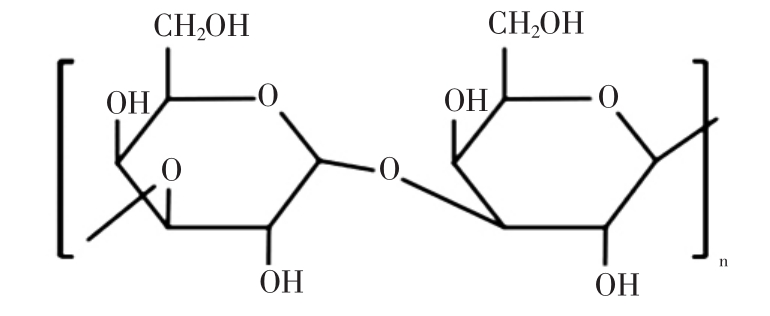
图3 热凝胶多糖的结构组成
Fig.3 The structure formula of curdlan
热凝胶多糖是一种由土壤产碱杆菌属所产生的中性葡聚糖,仅由β-(1,3)糖苷键组成,没有额外的支链或取代基存在,不溶于水,但可溶于碱性介质(pH>12)、二甲基亚砜和甲酸等。尽管热凝胶多糖水溶性不佳,但通过加热其水悬浮液可形成凝胶,根据加热温度可以形成两种类型的凝胶,其中一种是高固化热不可逆凝胶,即加热到80℃以上形成凝胶,温度变化对于凝胶状态不会造成大的影响;而另一种是低凝固热可逆凝胶,加热到55℃左右再冷却形成的凝胶,在温度重新上升后会溶解分散于水中,属于可逆性的凝结;据报道,只有当加热到100℃以上时,该凝胶的状态才达到绝对不可逆性[28]。
1.3.2 热凝胶多糖的应用状况
热凝胶多糖独特的凝胶性使其成为食品工业中的增稠剂或脂肪模拟替代品[29];在蛋糕等烘焙食品中热凝胶多糖可增加产品稳定性和保湿性;在面食、冷冻食品及调味品中加入可以增添口感,改善质地;也可作为功能性成分,生产低热减肥的保健食品。热凝胶多糖成膜性良好,现常与其它胶体共混制备食品薄膜或生物材料[30]。天然热凝胶多糖具有免疫调节和抗肿瘤活性,但水不溶性限制了其发展,时下凝胶多糖衍生物成为了生物医学领域的研究热点之一。据报道,胺化后的热凝胶多糖可用于小干扰RNA靶向肿瘤细胞的输送[31],酯化、磷酸化和羧甲基化可使热凝胶多糖成为良好的药物载体。此外,硫酸化有可能为其引入新的抗病毒特性[32],值得进一步研究。
1.4 普鲁兰(pullulan)
1.4.1 结构特性
普鲁兰多糖的结构组成见图4[33]。

图4 普鲁兰多糖的结构组成
Fig.4 The structure formula of pullulan
普鲁兰多糖是一种水溶性中性真菌多糖,自出芽短梗霉的发酵液中提取。普鲁兰首先经α-(1,6)键连接构成麦芽三糖基本单元,三糖之间再通过α-(1,4)键形成线性无支链的多聚体[34]。普鲁兰多糖在低浓度的碱性溶液中也具备良好的溶解性,其对酸碱与盐离子稳定,具有一定黏度,不溶于乙醇和其他有机溶剂,但可溶于二甲基亚砜和甲酰胺。
1.4.2 普鲁兰多糖的应用状况
普鲁兰多糖主链中含有高浓度羟基,使得它具备多种潜在的生理活性,例如抗氧化、免疫调节、促进消化、降低胆固醇等,在食品、制药、生物医学及组织工程中有着广泛的应用。普鲁兰多糖难以被人肠道消化吸收,可用于生产低热量减肥食品以及益生元食品[35];在液体和固体食物中可替代淀粉使用;也可作为饮料和调味汁中的低黏度填充物或糖果制品中的粘合剂等。普鲁兰多糖透明性高,隔氧性好,成膜性与机械性能卓越,可用作食用薄膜[36],研究发现,普鲁兰多糖膜可保持食物中的水分,并通过抑制微生物的呼吸作用来减少微生物在食品表面的生长,这使得其在食品包装材料方面也颇具优势。普鲁兰多糖及其衍生物具有治愈创伤的潜在作用[34],可制作医用敷料。此外,低分子量的普鲁兰还可作为血浆的替代品。
1.5 细菌纤维素(bacterial cellulose)
1.5.1 结构特性
细菌纤维素的结构组成见图5[37]。

图5 细菌纤维素的结构组成
Fig.5 The structure formula of bacterial cellulose
细菌纤维素(bacterial cellulose,BC)是经 β-(1,4)糖苷键连接而成的直链多糖,重复单元为两个葡萄糖分子结合的纤维二糖[37]。细菌纤维素可由多种细菌产生,例如产碱杆菌、假单胞菌、葡糖醋酸杆菌、根瘤菌和八叠球菌等[38],商业化的细菌纤维素主要由葡糖醋杆菌进行生产。细菌纤维素拥有三维多孔网状结构,并且在微纤维束的表面上含有许多亲水性羟基,这使得其存在高度的持水性,同时还拥有卓越的机械性能,这是其它胞外多糖所不具备的。
1.5.2 细菌纤维素的应用状况
BC具有良好的pH值、温度和冻融适用范围,常在调味酱中作为增稠剂,在豆制品中作为胶凝剂,在冰激凌中作为稳定剂,在风味饮料中用作悬浮剂。因其具有可食用性、降解性、生物相容性和良好的阻隔性,也可成为卓越的食品包装材料[39]。BC还具有显著的降血脂和降胆固醇作用,因此,可以用其生产无脂、低胆固醇和低热量的保健食品,同时它也可以乳化肉制品中的成分从而改善产品品质[40]。另一方面,BC纤维中存在的高密度氢键导致BC具有高结晶度和低可塑性,这限制了其在伤口敷料和新型材料等领域的应用,因此,在之后的发展中,BC的改性化研究将会占据重要地位。
1.6 威兰胶(welan gum)
1.6.1 结构特性
威兰胶的结构组成见图6[41]。
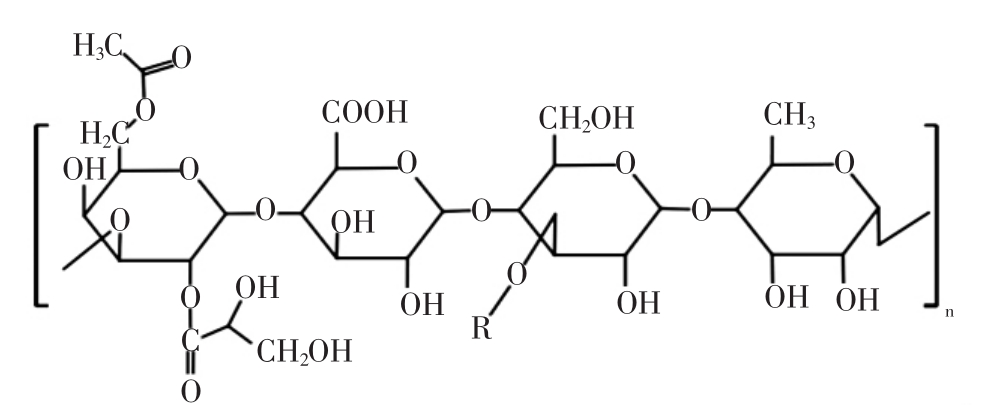
图6 威兰胶的结构组成
Fig.6 The structure formula of welan gum
威兰胶(welan gum,WLG)是通过产碱杆菌属细菌发酵而产生的阴离子多糖,由四糖重复单元构建,由2个葡萄糖、葡萄糖醛酸和鼠李糖组成,在第3个连接的葡萄糖处会出现一个单糖侧链,这个单糖为鼠李糖或者甘露糖,并且超过一半的重复单元具有乙酰基和甘油基取代基[42]。据研究,WLG水溶液具备高黏度,耐酸碱,在150℃的条件下可保持稳定,这种胶体对极端条件的优异耐受性主要归因于其水溶液形成的网络结构。其次,WLG溶液也是典型的非牛顿流体,具有剪切稀化行为。
1.6.2 威兰胶的应用状况
据报道,威兰胶在提高石油采收率方面具有良好的潜质,特别是在高温和高盐度储层中,能提高二次采油的采油率[41];另外,威兰胶与结冷胶、透明质酸等EPS类似,含有大量羧基,属于阴离子多糖,可用于凝胶的合成,故其在递送载体方面具有一定发展潜力。到目前为止,威兰胶食用安全性数据尚且不足,限制其在食品领域的应用,因此亟需展开对威兰胶的安全性评估,研究其在食品中的利用价值。
1.7 透明质酸(hyaluronic acid)
1.7.1 结构特性
透明质酸的结构组成见图7[43]。

图7 透明质酸的结构组成
Fig.7 The structure formula of hyaluronic acid
透明质酸(hyaluronic acid,HA)是一种天然非硫酸化糖胺聚糖,由D-葡糖醛酸和N-乙酰葡糖胺经β-(1,3)糖苷键形成双糖基本单元,双糖单元之间又以β-(1,4)键进一步结合促成长链聚合物。HA具有双螺旋结构,内部含有大量的亲水基团,保水能力出众。HA在自然界广泛分布,存在于人类,动物(如兔、牛、公鸡),细菌中,然而,它在真菌,植物和昆虫中没有发现[44]。在人体中,70 kg成人的HA总含量约为15 g,大约50%的总HA存在于皮肤的真皮和表皮中。
1.7.2 透明质酸的应用状况
通过微生物发酵获得的HA在结构上与内源HA相同;因此,HA及其衍生物广泛用于化妆品工业、医药和外科手术。HA生物活性与分子量密切相关[45],高分子量HA具有抗炎和抗血管生成特性,而低分子量HA具有促炎和促血管生成活性[46]。此外,研究表明HA促进巨噬细胞分化为M2表型,通过与可生物降解的材料混合并用,可以改善细胞增殖和促进组织再生。
HA在美国、加拿大、韩国和日本等作为膳食补充剂销售,主要用于缓解关节疼痛或皮肤皱纹。据报道,将HA添加至低脂肪酸奶并将其提供给轻度膝关节疼痛患者,改善男性患者的肌肉功能[47];在对大鼠的实验报告中,口服摄入的HA可以迁移到大鼠的皮肤中,从而减少皮肤干燥[48]。目前微生物来源的HA来自兽疫链球菌,但由于其可能产生外毒素、发酵条件难以控制以及培养基昂贵限制了其应用。近期有研究将链球菌产生HA相关的基因导入到乳酸乳球菌中[49],从而获得了可生产HA的传统发酵菌株,为微生物大量生产HA提供了可能。
总体而言,EPS可在食品工业中开发多种应用,具体见表1。
表1 不同微生物来源胞外多糖的研究近况
Table 1 Research status of exopolysaccharides from different microorganism

注:-表示暂无相关报道。
菌种名称 种类 主要单糖组成/% 分子量(Mw) 功能特性或潜在应用 参考文献深海热液弧菌 细菌 乙酰葡糖胺(25),葡萄糖醛酸(50),N-乙酰-半乳糖胺(25)1.0×105 ~3.0×105 组织工程中的活性物质递送载体 [50]植物乳杆菌BC25 细菌 甘露糖(92),半乳糖(2),葡萄糖(6) 1.33 ~1.83×104 食品中的营养添加剂 [51]干酪乳杆菌LC2W 细菌 葡萄糖(57.8),鼠李糖(27.7),半乳糖(14.5)1.24×106 具备降血压功能 [52-53]马乳酒样乳杆菌&Lactobacillus satsumensis细菌 α-葡聚糖 8.0×105 免疫调节,抗肿瘤,可作食品添加剂或药品中的成分[54]魏斯氏菌CMGDEX3 细菌 α-葡聚糖 2.0 ~4.0×106 面包中的质地改良剂 [55]叶杆菌属921F 细菌 葡萄糖(50),半乳糖(50) 1.082×106 具有良好的保湿性能 [56]Bacillus sonorensis MJM60135细菌 甘露糖,葡萄糖 - 具备良好的益生性 [57]Bacillus vallismortisWF4 细菌 甘露糖(51.8),葡萄糖(20.8),木糖(13.3),阿拉伯糖(14.1)3.83×105 具乳化性,抗真菌,可用于乳膏的制作[58]嗜热链球菌CRL1190 细菌 葡萄糖(40),半乳糖(60) 1.782×106 食品中的稳定剂、絮凝剂 [59]Lactobacillus Ca6 细菌 聚葡萄糖 1.2 ~1.9×106 抗氧化性,乳化性可作食品中的稳定剂,乳化剂[60]灰略红链霉菌GD5 细菌 阿拉伯糖,葡萄糖,半乳糖,甘露糖,木糖 - 潜在的抗氧化剂,乳化剂,也可作抗菌膜[61]Rhodobacter johrii CDR-SL 7Cii细菌 葡萄糖(60),葡萄糖醛酸(30),鼠李糖(5),半乳糖(5)2.0×106 对热稳定,具乳化性食品和化妆品中的乳化剂[62]茄腐镰刀菌SD5 真菌 鼠李糖(33),半乳糖(67) 1.87×105 抗炎症,抗过敏可作食品添加剂,药物成分[63-64]Fusarium equiseti ANP2 真菌 甘露糖(72.6),葡萄糖(27.3) - 良好的抗氧化剂 [65]曲霉菌Y16 真菌 甘露糖(89.4),半乳糖(10.6) 1.5×104 潜在的抗氧化物质 [66]青霉菌solitum 真菌 甘露聚糖 1.13×104 药理学上有着潜在的价值 [67]链格孢F1 真菌 半乳糖醛酸(5.2),鼠李糖(34.8),甘露糖(37.5),葡萄糖(11.5),半乳糖(11.0)3.246×104 具热稳定性,抗氧化性,食品中良好的抗氧化剂[68]Pestalotiopsis BC55 真菌 β-葡聚糖 2.0×105 - [69]Neopestalotiopsis SKE15 真菌 葡萄糖(50),半乳糖(40),山梨糖醇(10) 1.52 ~1×106 良好的抗菌性,抗氧化性可作有效的食品保护剂[70]Physarella oblonga Physarum polycephalum粘菌 葡萄糖(15.6),半乳糖(18.0),鼠李糖(66.4)- 抗氧化,抑制有害微生生物所产生的活性物质[71]
上述EPS中,结冷胶、黄原胶、透明质酸、威兰胶具有的羧基结构可与多价阳离子形成较强的凝胶,在制作糖果,胶囊等产品有着较大的优势;在增稠稳定方面黄原胶效果最佳,因其用量低,黏度高,在生产中可节省一定成本;具凝胶特性的EPS还可广泛用于各种生物膜的制作与生产。除细菌真菌外,少数粘菌也可产生EPS,但目前粘菌EPS报道极少。
2 细胞壁多糖(cell wall polysaccharides)
2.1 脂多糖(lipopolysaccharide)
2.1.1 结构特性
脂多糖的一般结构组成见图8[72]。
微生物中的脂多糖(lipopolysaccharide,LPS)主要在革兰氏阴性菌的细胞壁外层上大量存在,由脂质A、核心寡糖和O特异性多糖三部分构成[72]。脂质A以β-(1,4)相连的两个氨基葡萄糖多糖为核心,连接着长链脂肪酸与磷酸基团并镶嵌在细菌外膜上。不同细菌来源的脂多糖组成有所不同,体现在聚糖区域的结构组成、脂质A区域的长链脂肪酸和磷酸基团这三者的区别。LPS暴露于菌体表面且具备抗原特征,能够刺激人体的免疫系统从而产生各种免疫反应及不良症状,被认为是内毒素的一种。脂质A是LPS起毒素作用的所负责的结构领域,是主要的免疫刺激中心[73]。
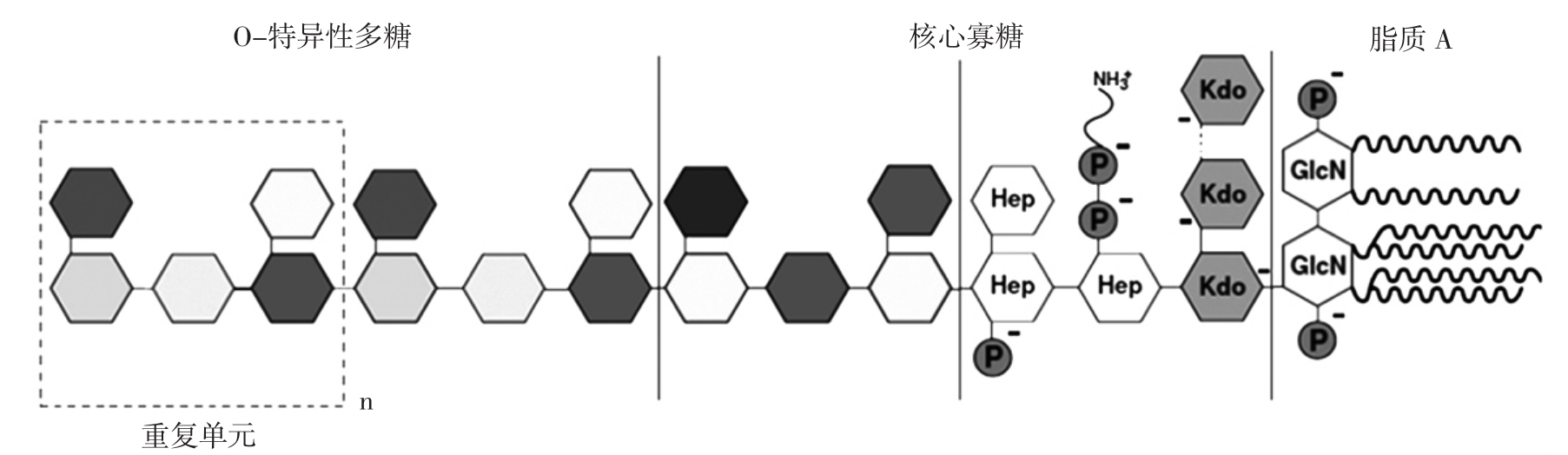
图8 脂多糖的一般结构组成
Fig.8 The common structure of lipopolysaccharides
Hep.D-甘油-D-甘露庚糖;Kdo.2-酮-3-脱氧辛酸;P.磷酸盐;GlcN.氨基葡萄糖。
2.1.2 脂多糖的应用状况
LPS在医药领域研究较多,常用作疫苗佐剂。百日咳是一种由革兰氏阴性细菌百日咳博德特氏菌引起的呼吸道传染病。据报道,Toll样受体4(toll-like receptors 4,TLR4)可以识别LPS与其相结合从而激活信号转导因子并产生免疫反应。Geurtsen等[74]将LPS衍生物单磷酰脂质A与奈瑟氏球菌突变菌株的LPS作为佐剂加入到百日咳疫苗中,采用小鼠实验对治疗效果进行评价,结果显示,两种成分的加入成功改善疫苗的效果,且LPS相关物添加的百日咳疫苗有着较低的反应原性。在近期的研究中,Ledov等[75]从志贺氏菌中分离了LPS,将五酰基和六酰基去除,以获取修饰化的LPS,通过动物与临床试验论证,与完整LPS相比,修饰化的LPS有着较低的毒性与致热原性并保持了免疫原性,这说明了通过减少LPS酰化程度可以一定水平上降低其毒性作用。
还有调查显示,LPS具备伤口治愈的作用。早期有报告称低浓度下的LPS具有促进创伤愈合的功效[76],在最近的研究中,Morishima等[77]将含有LPS成分的软膏涂抹到患者的伤口上,结果显示,伤口在药物处理过后有着不同程度的愈合,这很可能归功于LPS的促进了M2型巨噬细胞的增加,一定程度提高了抗炎因子的水平,加速了血管组织的修复与重建。另外,LPS本身也能激活TLR4信号通路,这条信号通路与创伤愈合过程有关。因此,无毒的LPS衍生物以及新型LPS的开发是今后研究的一个重要方向。
2.2 肽聚糖(peptidoglycan)
2.2.1 结构特性
肽聚糖(peptidoglycan,PTN)是大量存在于细菌细胞壁中的多重网状聚合物,是参与细胞壁组成的重要成分,属于糖胺聚糖的一种,由交替组装的β-(1,4)连接的N-乙酰葡糖胺和N-乙酰胞壁酸的二糖单元组成,重复的双糖聚合链再通过短肽链进一步交联,短肽链最初为五肽,末端位置通常为D-丙氨酸,成熟的PTN分子中末端氨基酸往往会发生裂解脱落[78]。细胞壁中的PTN由于这种纵横交错的复杂网状结构,可以保护细胞不因细胞质的渗透压增大而破裂,并能进一步维持细菌细胞的特定形状。不同菌种的PTN组成不同,革兰氏阳性菌细胞壁较革兰氏阴性菌厚,多糖组成更为复杂,体现在聚糖链长度的差异和氨基酸的多样性[79]。PTN中肽的连接方式有多种,目前研究较多的结合模式为4→3交联,即短肽的三号位氨基酸与相邻短肽的四号位氨基酸直接相连构成肽键或以桥接形式相连。革兰氏阴性菌一般为直接交联,而阳性菌通常会额外存在一段肽桥。目前除了4→3交联,还有4→2,3→3交联等形式[80],每种菌株的交联方式可能不尽相同。
肽聚糖的化学结构本身较为保守,但其非晶体排列使其结构的可视化变得困难。此外,聚糖链和肽链的交联结构难以通过传统电子显微镜观察,导致其结构解析较为困难[81]。目前,根据相对于细菌膜方向的差异,讨论最多的肽聚糖模型有两种,分别为铺设和支架[82],肽聚糖可能的存在模式见图9[82]。
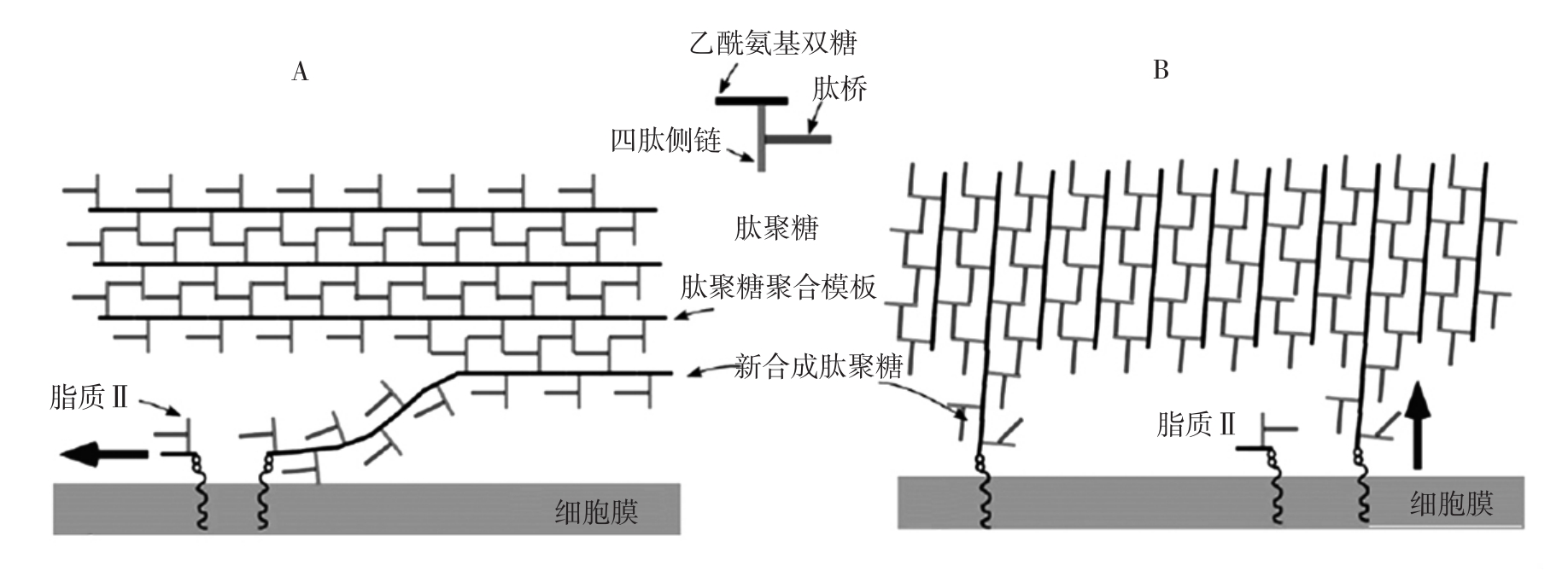
图9 肽聚糖可能的存在模式
Fig.9 The possible pattern of peptidoglycans
A.铺设模型;B.支架模型。
在铺设模型A中,聚糖链在平行于膜的方向延伸;而在支架模型B中,聚糖链垂直于膜排列。已有研究表明,低温电子断层扫描(cryo-electron tomography,CET)和原子力显微镜(atomic force microscopy,AFM)等直接成像的方法在揭示PTN的形态学结构方面起到重大作用。在CET的成像报告中,对革兰氏阴性菌中的新月柄杆菌与大肠杆菌的PTN进行了研究,结果显示这两种菌的PTN多为单层且垂直于细胞的长轴并以散乱的箍状形式围绕菌体,更契合上述的第一种模型[83];革兰氏阳性菌的PTN结构相对复杂,在对枯草芽孢杆菌的AFM观察中,呈现其细胞壁内表面规则的宏观结构,其中聚糖链横穿细胞短轴,比菌体本身更长[84],研究还提出了新的卷曲螺旋模型,但这种模型同样存在争议。
2.2.2 肽聚糖的应用状况
肽聚糖的功能及应用一直处于探索中,其对于生物机体是否存在益处一直是人们关注的焦点。迄今为止,已经有大量关于益生菌的报道,它们可以在一定的数量下为宿主带来诸多益处[85],包括调节胃肠道菌群、降低血液胆固醇、调节免疫、预防病原体感染和癌症等,这些作用都与肽聚糖息息相关。有研究报告,灭活后的鼠李糖乳杆菌对营养不良小鼠的呼吸免疫也有着一定的改善[86],这证明了菌体的某些结构存在着一定功能,鼠李糖乳杆菌属于革兰氏阳性菌,其所富含的肽聚糖极可能是益生菌发挥作用的关键物质。现今已有报道证明益生菌肽聚糖具有免疫调节[87]、抑制炎症[88]、抗肿瘤等[89]多重功效,在与宿主的相互作用中充当信号物质,通过激活巨噬细胞,提高白细胞介素1(interleukin-1,IL-1)和IL-6等因子的表达,增强宿主的防御体系,因此,肽聚糖具有作为保健食品的潜质。但是,肽聚糖的水溶性不佳,产量较低,这使其应用受到很大限制。有3种方式可用于提高肽聚糖的水溶性,一是酶解,据报道,溶菌酶[90]、变溶菌素[91]能够分解肽聚糖;二是酸处理,利用强酸水解肽聚糖,但这种手段很可能会过度破坏肽聚糖结构从而影响其活性;三是化学改性,此种方式国内外鲜有报道,有待后续研究。
2.2.3 其它
细胞壁多糖除了上述两类外,还有真菌细胞壁中的葡聚糖、壳多糖及其复合物等[92]。它们大多具备抗氧化、抗菌、抗肿瘤和增强免疫等作用,部分细胞壁多糖还拥有预防动脉粥样硬化、抑制肥胖[93]以及伤口治愈[94]的潜在功效,其在食品和医药领域有着良好的应用空间。酵母β葡聚糖报道较多且已得到商业化,而对真菌中壳多糖的研究仍然不足[94]。目前商业化壳多糖主要从甲壳动物中分离,在之后的发展中,对真菌壳多糖的研究会趋于完善,同时微生物来源的壳多糖也将占据一定的市场。
3 结论与展望
综上,微生物来源的多糖具有多种功能特性和健康效应,拥有广阔的发展前景。今后,新的微生物多糖的研究与开发将成为该领域的重要发展方向。首先,值得注意的是益生菌胞外多糖对人体具有良好的健康调节作用,但因产量限制尚未得到商业化应用[95],因此,益生菌胞外多糖的商业化规模生产技术将成为研究的热点之一。其次,许多研究证明了改性可以为多糖引入新的性质或增强原本的生物活性[96]。因此,加强对各类微生物多糖的衍生化修饰研究,可一定程度上开拓微生物多糖的应用空间。另外,还需要继续对肽聚糖结构进行解析,其中糖链终止和释放的机制、肽链间的结合模式以及其它类型基团的连接位点等研究仍需深入,为肽聚糖进一步研究与开发提供更可靠的理论基础。
随着科研工作的深入,已有越来越多的微生物多糖被发掘,而以它们为目标所创建的数据库却很少[97]。所以,进一步梳理和分析不同微生物来源多糖的性质和应用,构建相应的网络数据平台也成为该领域一项十分有意义的工作。同时,微生物多糖作为一个庞大的群体,在资源日趋紧张的环境下,开发微生物源的健康食品也具有重要的现实意义和应用价值。
[1]王嘉铭,雷于国,胡国元,等.香菇多糖纯化前后结构和生物活性的比较[J].食品与生物技术学报,2020,39(1):99-106.
[2]王丽敏,舒适,杨娟.楮实多糖对小鼠抗疲劳作用的研究[J].食品研究与开发,2019,40(22):25-28,81.
[3]舒尊鹏,杨燕妮,王毅,等.枳壳多糖对辐射损伤小鼠的防护作用研究[J].中国药理学通报,2018,34(5):670-674.
[4]张锦锦,陈菲菲,严展鹏,等.灵芝β-葡聚糖的碱提取及其抗肿瘤免疫调节研究[J].药学学报,2020,55(3):512-521.
[5]朱振元,李楠,张静怡,等.雪莲果多糖降血脂及降血糖活性的研究[J].现代食品科技,2017,33(5):39-46,76.
[6]Chen D,Sun S,Cai D W,et al.Induction of mitochondrial-dependent apoptosis in T24 cells by a selenium (Se)-containing polysaccharide from Ginkgo biloba L.leaves[J].International journal of biological macromolecules,2017,101:126-130.
[7]Xu L,Qiu Z,Gong H J,et al.Synergy of microbial polysaccharides and branched-preformed particle gel on thickening and enhanced oil recovery[J].Chemical Engineering Science,2019,208:115138.
[8]朱桂兰,童群义.微生物多糖的研究进展[J].食品工业科技,2012,33(6):444-448.
[9]Mozzi F,Gerbino E,Font de Valdez G,et al.Functionality of exopolysaccharides produced by lactic acid bacteria in an in vitro gastric system[J].Journal of applied microbiology,2009,107(1):56-64
[10]Lynch K M,Coffey A,Arendt E K.Exopolysaccharide producing lactic acid bacteria:Their techno-functional role and potential application in gluten-free bread products[J].Food research international,2018,110:52-61.
[11]Moroni A V,Dal Bello F,Arendt E K.Sourdough in gluten-free bread-making:an ancient technology to solve a novel issue?[J].Food microbiology,2009,26(7):676-684.
[12]Hassan A N.ADSA Foundation Scholar Award:Possibilities and challenges of exopolysaccharide-producing lactic cultures in dairy foods[J].Journal of dairy science,2008,91(4):1282-1298.
[13]Morris E R,Nishinari K,Rinaudo M.Gelation of gellan-A review[J].Food Hydrocolloids,2012,28(2):373-411.
[14]Cavallieri A L F,da Cunha R L.The effects of acidification rate,pH and ageing time on the acidic cold set gelation of whey proteins[J].Food Hydrocolloids,2008,22(3):439-448.
[15]Xu X J,Li Y H,Fang S,et al.Effects of Different Acyl Gellan Gums on the Rheological Properties and Colloidal Stability of Blueberry Cloudy Juice[J].Journal of food science,2018,83(5):1215-1220.
[16]Sherafati M,Kalbasi-Ashtari A,Mousavi S M A.Effects of Low and High Acyl Gellan Gums on Engineering Properties of Carrot Juice[J].Journal of Food Process Engineering,2013,36(4):418-427.
[17]Giavasis I,Harvey L M,McNeil B.Gellan gum[J].Critical reviews in biotechnology,2000,20(3):177-211.
[18]Prezotti F,Boni F,Ferreira N,et al.Gellan Gum/Pectin Beads Are Safe and Efficient for the Targeted Colonic Delivery of Resveratrol[J].Polymers,2018,10(1):50.
[19]Prezotti F G,Cury B S,Evangelista R C.Mucoadhesive beads of gellan gum/pectin intended to controlled delivery of drugs[J].Carbohydrate Polymers,2014,113:286-295.
[20]Bhattacharjee K,Joshi S R.A selective medium for recovery and enumeration of endolithic bacteria[J].Journal of microbiological methods,2016,129:44-54.
[21]Freitas F,Alves V D,Reis M A.Advances in bacterial exopolysaccharides:from production to biotechnological applications[J].Trends in biotechnology,2011,29(8):388-398.
[22]Bonifacio M A,Cometa S,Cochis A,et al.Antibacterial effectiveness meets improved mechanical properties:Manuka honey/gellan gum composite hydrogels for cartilage repair[J].Carbohydrate Polymers,2018,198:462-472.
[23]Sharma G,Thakur B,Naushad M,et al.Applications of nanocomposite hydrogels for biomedical engineering and environmental protection[J].Environmental Chemistry Letters,2017,16(1):113-146
[24]Garcia-Ochoa F,Santos V E,Casas J A,et al.Xanthan gum:production,recovery,and properties[J].Biotechnology advances,2000,18(7):549-579.
[25]Niknezhad S V,Asadollahi M A,Zamani A,et al.Optimization of xanthan gum production using cheese whey and response surface methodology[J].Food Science and Biotechnology,2015,24(2):453-460.
[26]Sothornvit R.Edible coating and post-frying centrifuge step effect on quality of vacuum-fried banana chips[J].Journal of Food Engineering,2011,107(3/4):319-325.
[27]Zhang R,Edgar K J.Properties,chemistry,and applications of the bioactive polysaccharide curdlan[J].Biomacromolecules,2014,15(4):1079-1096.
[28]Mangolim C S,da Silva T T,Fenelon V C,et al.Use of FT-IR,FTRaman and thermal analysis to evaluate the gel formation of curdlan produced by Agrobacterium sp.IFO 13140 and determination of its rheological properties with food applicability[J].Food chemistry,2017,232:369-378.
[29]Chen C,Wang R,Sun G,et al.Effects of high pressure level and holding time on properties of duck muscle gels containing 1% curd-lan[J].Innovative Food Science&Emerging Technologies,2010,11(4):538-542.
[30]Cai Z,Dai Q,Guo Y,et al.Glycyrrhiza polysaccharide-mediated synthesis of silver nanoparticles and their use for the preparation of nanocomposite curdlan antibacterial film[J].International journal of biological macromolecules,2019,141:422-430.
[31]Ganbold T,Han S Q,Hasi A,et al.Receptor-mediated delivery of therapeutic RNA by peptide functionalized curdlan nanoparticles[J].International journal of biological macromolecules,2019,126:633-640.
[32]Cai Z,Zhang H.Recent progress on curdlan provided by functionalization strategies[J].Food Hydrocolloids,2017,68:128-135.
[33]Cheng K C,Demirci A,Catchmark J M.Pullulan:biosynthesis,production,and applications[J].Applied microbiology and biotechnology,2011,92(1):29-44.
[34]Singh R S,Kaur N,Sharma R,et al.Carbamoylethyl pullulan:QbD based synthesis,characterization and corneal wound healing potential[J].International journal of biological macromolecules,2018,118:2245-2255.
[35]Chen L,Zhang H,McClements D J,et al.Effect of dietary fibers on the structure and digestibility of fried potato starch:A comparison of pullulan and pectin[J].Carbohydrate Polymers,2019,215:47-57.
[36]Shingel K I.Current knowledge on biosynthesis,biological activity,and chemical modification of the exopolysaccharide,pullulan[J].Carbohydrate research,2004,339(3):447-460.
[37]Stumpf T R,Yang X,Zhang J,et al.In situ and ex situ modifications of bacterial cellulose for applications in tissue engineering[J].Materials science&engineering C,Materials for biological applications,2018,82:372-383.
[38]Jozala A F,de Lencastre Novaes L C,Lopes A M,et al.Bacterial nanocellulose production and application:a 10-year overview[J].Applied microbiology and biotechnology,2016,100(5):2063-2072.
[39]Shi Z J,Zhang Y,Phillips G O,et al.Utilization of bacterial cellulose in food[J].Food Hydrocolloids,2014,35:539-545.
[40]Yu S Y,Lin K W.Influence of Bacterial Cellulose (Nata)on the Physicochemical and Sensory Properties of Frankfurter[J].Journal of food science,2014,79(6):1117-1122.
[41]Xu L,Xu G,Liu T,et al.The comparison of rheological properties of aqueous welan gum and xanthan gum solutions[J].Carbohydrate Polymers,2013,92(1):516-522.
[42]Rinaudo M.Role of substituents on the properties of some polysaccharides[J].Biomacromolecules,2004,5(4):1155-1165.
[43]Volpi N,Schiller J,Stern R,et al.Role,metabolism,chemical modifications and applications of hyaluronan[J].Currentmedicinalchemistry,2009,16(14):1718-1745.
[44]Kogan G,Soltes L,Stern R,et al.Hyaluronic acid:a natural biopolymer with a broad range of biomedical and industrial applications[J].Biotechnology letters,2007,29(1):17-25.
[45]Ibrahim S,Kang Q K,Ramamurthi A.The impact of hyaluronic acid oligomer content on physical,mechanical,and biologic properties of divinyl sulfone-crosslinked hyaluronic acid hydrogels[J].Journal of biomedical materials research Part A,2010,94(2):355-370.
[46]Maharjan A S,Pilling D,Gomer R H.High and Low Molecular Weight Hyaluronic Acid Differentially Regulate Human Fibrocyte Differentiation[J].Plos One,2011,6(10):26078.
[47]Sola R,Valls R M,Martorell I,et al.A low-fat yoghurt supplemented with a rooster comb extract on muscle joint function in adults with mild knee pain:a randomized,double blind,parallel,placebocontrolled,clinical trial of efficacy[J].Food&Function,2015,6(11):3531-3539.
[48]Oe M,Mitsugi K,Odanaka W,et al.Dietary hyaluronic acid migratesintothe skin of rats[J].TheScientificWorldJournal,2014,2014:378024.
[49]Sheng J,Ling P,Wang F.Constructing a recombinant hyaluronic acid biosynthesis operon and producing food-grade hyaluronic acid in Lactococcus lactis[J].Journal of industrial microbiology&biotechnology,2015,42(2):197-206.
[50]Zykwinska A,Marquis M,Sinquin C,et al.Assembly of HE800 exopolysaccharide produced by a deep-sea hydrothermal bacterium into microgels for protein delivery applications[J].Carbohydrate Polymers,2016,142:213-221.
[51]Zhou K,Zeng Y,Yang M,et al.Production,purification and structural study of an exopolysaccharide from Lactobacillus plantarum BC-25[J].Carbohydrate Polymers,2016,144:205-214.
[52]Ai L,Zhang H,Guo B,et al.Preparation,partial characterization and bioactivity of exopolysaccharides from Lactobacillus casei LC2W[J].Carbohydrate Polymers,2008,74(3):353-357.
[53]Ai L,Guo Q,Ding H,et al.Structure characterization of exopolysaccharides from Lactobacillus casei LC2W from skim milk[J].Food Hydrocolloids,2016,56:134-143.
[54]Paiva I M d,Steinberg R d S,Lula I S,et al.Lactobacillus kefiranofaciens and Lactobacillus satsumensis isolated from Brazilian kefir grains produce alpha-glucans that are potentially suitable for food applications[J].LWT-Food Science and Technology,2016,72:390-398.
[55]Ahmed R Z,Siddiqui K,Arman M,et al.Characterization of high molecular weight dextran produced by Weissella cibaria CMGDEX3[J].Carbohydrate Polymers,2012,90(1):441-446.
[56]Chi Y,Ye H,Li H,et al.Structure and molecular morphology of a novel moisturizing exopolysaccharide produced by Phyllobacterium sp.921F[J].International journal of biological macromolecules,2019,135:998-1005.
[57]Palaniyandi S,Damodharan K,Suh J W,et al.Functional Characterization of an Exopolysaccharide Produced by Bacillus sonorensis MJM60135 Isolated from Ganjang[J].Journal of microbiology and biotechnology,2018,28(5):663-670.
[58]Song B,Zhu W,Song R,et al.Exopolysaccharide from Bacillus vallismortis WF4 as an emulsifier for antifungal and antipruritic peppermintoilemulsion[J].Internationaljournal of biological macromolecules,2019,125:436-444.
[59]Lobo R E,Gómez M I,Font de Valdez G,et al.Physicochemical and antioxidant properties of a gastroprotective exopolysaccharide produced by Streptococcus thermophilus CRL1190[J].Food Hydrocolloids,2019,96:625-633.
[60]Trabelsi I,Slima S B,Chaabane H,et al.Purification and characterization of a novel exopolysaccharides produced by Lactobacillus sp.Ca6[J].International journal of biological macromolecules,2015,74:541-546.
[61]Vinothini G,Latha S,Arulmozhi M,et al.Statistical optimization,physio-chemical and bio-functional attributes of a novel exopolysaccharide from probiotic Streptomyces griseorubens GD5[J].International journal of biological macromolecules,2019,134:575-587.
[62]Sran K S,Sundharam S S,Krishnamurthi S,et al.Production,characterization and bio-emulsifying activity of a novel thermostable exopolysaccharide produced by a marine strain of Rhodobacter johrii CDR-SL 7Cii[J].International journal of biological macromolecules,2019,127:240-249.
[63]Mahapatra S,Banerjee D.Structural elucidation and bioactivity of a novel exopolysaccharide from endophytic Fusarium solani SD5[J].Carbohydrate Polymers,2012,90(1):683-689.
[64]Mahapatra S,Banerjee D.Evaluation of in vitro antioxidant potency of exopolysaccharide from endophytic Fusarium solani SD5[J].International journal of biological macromolecules,2013,53:62-66.
[65]Prathyusha A,Mohana Sheela G,Bramhachari P V.Chemical characterization and antioxidant properties of exopolysaccharides from mangrove filamentous fungi Fusarium equiseti ANP2[J].Biotechnol Rep(Amst),2018,19:277.
[66]Chen Y,Mao W,Tao H,et al.Structural characterization and antioxidant properties of an exopolysaccharide produced by the mangrove endophytic fungus Aspergillus sp.Y16[J].Bioresource technology,2011,102(17):8179-8184.
[67]Yan M,Mao W,Chen C,et al.Structural elucidation of the exopolysaccharide produced by the mangrove fungus Penicillium solitum[J].Carbohydrate Polymers,2014,111:485-491.
[68]Wang Y,Li Y,Li S,et al.Extracellular polysaccharides of endophytic fungus Alternaria tenuissima F1 from Angelica sinensis:Production conditions,purification,and antioxidant properties[J].International journal of biological macromolecules,2019,133:172-183.
[69]Mahapatra S,Banerjee D.Production and structural elucidation of exopolysaccharide from endophytic Pestalotiopsis sp.BC55[J].International journal of biological macromolecules,2016,82:182-191.
[70]Fooladi T,Soudi M R,Alimadadi N,et al.Bioactive exopolysaccharide from Neopestalotiopsis sp.strain SKE15:Production,characterization and optimization[J].International journal of biological macromolecules,2019,129:127-139.
[71]Huynh T T M,Phung T V,Stephenson S L,et al.Biological activities and chemical compositions of slime tracks and crude exopolysaccharides isolated from plasmodia of Physarum polycephalum and Physarella oblonga[J].BMC Biotechnol,2017,17(1):76.
[72]Alexander C,Rietschel E T.Bacterial lipopolysaccharides and innate immunity[J].Journal of Endotoxin Research,2001,7(3):167-202.
[73]Steimle A,Autenrieth I B,Frick J S.Structure and function:Lipid A modifications in commensals and pathogens[J].International journal of medical microbiology,2016,306(5):290-301.
[74]Geurtsen J,Banus H A,Gremmer E R,et al.Lipopolysaccharide analogs improve efficacy of acellular pertussis vaccine and reduce type I hypersensitivity in mice[J].Clinical and vaccine immunology:CVI,2007,14(7):821-829.
[75]Ledov V A,Golovina M E,Markina A A,et al.Highly homogenous tri-acylated S-LPS acts as a novel clinically applicable vaccine against Shigella flexneri 2a infection[J].Vaccine,2019,37(8):1062-1072.
[76]Koff J L,Shao M X,Kim S,et al.Pseudomonas lipopolysaccharide accelerates wound repair via activation of a novel epithelial cell signaling cascade[J].Journal of immunology,2006,177(12):8693-8700.
[77]Morishima A,Inagawa H.Improvement in Protracted Wound Healing by Topical Cream Containing Lipopolysaccharide Derived from Pantoea agglomerans[J].Anticancer research,2018,38(7):4375-4379.
[78]Vollmer W,Joris B,Charlier P,et al.Bacterial peptidoglycan(murein)hydrolases[J].FEMS Microbiology Reviews,2008,32(2):259-286.
[79]Vollmer W,Blanot D,De Pedro M A.Peptidoglycan structure and architecture[J].FEMS Microbiology Reviews,2008,32(2):149-167
[80]Catalao M J,Filipe S R,Pimentel M.Revisiting Anti-tuberculosis Therapeutic Strategies That Target the Peptidoglycan Structure and Synthesis[J].Frontiers in Microbiology,2019,10:190.
[81]Vollmer W,Seligman S J.Architecture of peptidoglycan:more data and more models[J].Trends in microbiology,2010,18(2):59-66.
[82]Kim S J,Chang J,Singh M.Peptidoglycan architecture of Grampositive bacteria by solid-state NMR[J].Biochimica et biophysica acta-biomembranes,2015,1848(1 Pt B):350-362.
[83]Gan L,Chen S,Jensen G J.Molecular organization of Gram-negative peptidoglycan[J].Proceedings of the National Academy of SciencesoftheUnitedStatesofAmerica,2008,105(48):18953-18957.
[84]Hayhurst E J,Kailas L,Hobbs J K,et al.Cell wall peptidoglycan architecture in Bacillus subtilis[J].Proceedings of the National A-cademy of Sciences of the United States of America,2008,105(38):14603-14608.
[85]Guimarães A,Abrunhosa L,Pastrana L M,et al.Edible Films and Coatings as Carriers of Living Microorganisms:A New Strategy Towards Biopreservation and Healthier Foods[J].Comprehensive Reviews in Food Science and Food Safety,2018,17(3):594-614.
[86]Kolling Y,Salva S,Villena J,et al.Non-viable immunobiotic Lactobacillus rhamnosus CRL1505 and its peptidoglycan improve systemic and respiratory innate immune response during recovery of immunocompromised-malnourished mice[J].International immunopharmacology,2015,25(2):474-484.
[87]Clua P,Kanmani P,Zelaya H,et al.Peptidoglycan from Immunobiotic Lactobacillus rhamnosus Improves Resistance of Infant Mice to Respiratory Syncytial Viral Infection and Secondary Pneumococcal Pneumonia[J].Frontiers in Immunology,2017,8:948.
[88]Wu Z,Pan D,Guo Y,et al.Peptidoglycan diversity and anti-inflammatory capacity in Lactobacillus strains[J].Carbohydrate Polymers,2015,128:130-137.
[89]He J,Wu Z,Pan D,et al.Effect of selenylation modification on antitumor activity of peptidoglycan from Lactobacillus acidophilus[J].Carbohydrate Polymers,2017,165:344-350.
[90]Brott A S,Clarke A J.Peptidoglycan O-Acetylation as a Virulence Factor:Its Effect on Lysozyme in the Innate Immune System[J].Antibiotics-Basel,2019,8(3):94.
[91]Chang J D,Foster E E,Yang H,et al.Quantification of the D-Ala-D-Lac-Terminated Peptidoglycan Structure in Vancomycin-Resistant Enterococcus faecalis Using a Combined Solid-State Nuclear Magnetic Resonance and Mass Spectrometry Analysis[J].Biochemistry,2017,56(4):612-622.
[92]Synowiecki J,Al-Khateeb N A.Production,properties,and some new applications of chitin and its derivatives[J].Critical reviews in food science and nutrition,2003,43(2):145-171.
[93]Berecochea Lopez A,Decorde K,Ventura E,et al.Fungal chitinglucan from Aspergillus niger efficiently reduces aortic fatty streak accumulation in the high-fat fed hamster,an animal model of nutritionally induced atherosclerosis[J].Journal of agricultural and food chemistry,2009,57(3):1093-1098.
[94]Jones M,Kujundzic M,John S,et al.Crab vs.Mushroom:A Review of Crustacean and Fungal Chitin in Wound Treatment[J].Marine Drugs,2020,18(1):64.
[95]Badel S,Bernardi T,Michaud P.New perspectives for Lactobacilli exopolysaccharides[J].Biotechnology advances,2011,29(1):54-66
[96]张华,王振宇,王雪,等.多糖化学改性方法及其生物活性研究进展[J].食品与发酵工业,2010,36(7):102-107.
[97]Birch J,Van Calsteren M R,Perez S,et al.The exopolysaccharide properties and structures database:EPS-DB.Application to bacterial exopolysaccharides[J].Carbohydrate Polymers,2019,205:565-570.