中国白酒有悠远的历史,多以小麦、高粱、玉米、大米和豌豆等粮食作物为主要原料,经过制曲、蒸梁、拌料、堆积发酵和窖池发酵以及蒸酒等主要生产过程酿造而成[1]。环境中纷繁复杂的微生物类群经自然网罗进入酿酒基质体系,最终由发酵代谢出以乙醇为主体的品类繁多的有机化合物成分,赋予中国白酒特有的“香和味”[2]。白酒种类繁多,因香型差异可以将其划分为清香型、浓香型、酱香型、米香型和其它各类香型。白酒是我国一种独特的蒸馏酒,其酿造风格、口味独特,且全球闻名,与世界其它著名蒸馏酒(如白兰地、威士忌、朗姆酒等)齐名成为六大蒸馏酒之一[3]。
徐岩等[4-5]通过研究证明,中国白酒不等同于酒精,而是含有各类醇、醛、酸、酯等丰富的风味物质且具保健功能的混合饮品。此外,有研究[6-7]报导中国白酒对心脑血管疾病有保护作用,亦能提升机体抵抗氧化损伤的能力,同时阻止体内代谢不良产物的生成,这进一步证实了中国白酒具有保健功效。白酒的生产经历了多种微生物的混合发酵过程,在这一过程中,微生物会代谢产生各种功能成分,如四甲基吡嗪、γ-氨基丁酸和核苷类物质等[7]。γ-氨基丁酸(γ-aminobutyric acid,GABA)具有保护心血管功能、降低血压、抗癫痫、镇痛以及痛觉过敏等作用[8-11],是有益于机体健康的氨基酸之一。此外,γ-氨基丁酸对胰岛β细胞能发挥保护和再生作用,还可以促进脑细胞的新陈代谢与恢复,增强长期记忆[12-13],还具有提高肝、肾机能等生理活性的功能[14]。核苷类化合物具有补益和增强免疫、保护神经、抗氧化、抗癌等生物活性,研究发现[15-16],腺苷能显著提高细胞活力,并在机体的中枢神经系统、心血管系统和凝血系统中发挥重要作用。尿苷具有促进睡眠和抗癫痫的作用,能改善记忆功能,影响神经元可塑性。
高效液相色谱法具有分离效能高、分析速度快、样品用量少等优点,该方法已广泛用于生物发酵中各种成分含量的测定,且使用的流动相简单并具有良好的重现性[17-18]。本研究采用高效液相色谱法,通过对色谱检测条件的优化,建立以高效液相色谱法定量分析中国白酒中γ-氨基丁酸和核苷类物质(腺苷、尿苷)的有效方法,并用所建方法对20种白酒中的上述功能成分进行了检测与分析,为进一步标准化中国白酒的品质评价及开展相关研究奠定基础,同时对指导中国白酒的生产改良、市场推广和深入科学研究有积极的作用和意义。
1 材料与方法
1.1 材料与试剂
待测酒样共20个,1号 ~9号白酒为河北山庄老酒;10号 ~20号白酒为市售酒样。γ-氨基丁酸、腺苷标准品、丹磺酰氯((纯度均>99%)、尿苷(纯度≥98%):美国Sigma公司;甲醇、乙腈(色谱纯):天津一方科技有限公司;乙酸钠、碳酸氢钠(分析纯):天津索罗门生物科技有限公司。
1.2 仪器与设备
1260高效液相色谱仪:美国安捷伦公司;EDAA-2300TH超声波清洗器:上海安谱实验科技股份有限公司;BSA224S电子分析天平:爱来宝医疗科技有限公司;HH-S6恒温水浴锅:上海一凯仪器设备有限公司。
1.3 方法
1.3.1 标准品及样品溶液的配制
1.3.1.1 标准品溶液配制
γ-氨基丁酸标准品溶液:准确称取GABA的标准品10.00 mg置于100 mL容量瓶中,用乙腈溶解并定容,配制成100 mg/L的γ-氨基丁酸标样母液。随后倍比稀释,配制成 0.10、0.20、0.50、1.0、2.0、5.0、10、20 mg/L的系列标准溶液,现配现用。
核苷类物质标准品:精确称取尿苷的标准品1.00mg和腺苷的标准品10.00 mg置于同一10 mL容量瓶中,用10%甲醇溶解并定容,可得尿苷浓度为100 mg/L和腺苷浓度为1 000 mg/L的混合标样母液。倍比稀释即可得到混合标准工作溶液中尿苷溶度为0.5、1.0、2.0、5.0、10 mg/L;腺苷浓度为 5、10、20、50、100 mg/L。
1.3.1.2 样品溶液的配制
测定γ-氨基丁酸:测定前需对样品衍生化处理,准确吸取1 mL的酒样或标准溶液置于具塞试管中,加入0.20 mL的碳酸氢钠溶液和0.40 mL的丹磺酰氯衍生试剂,混匀后在70℃水浴中反应20 min,用0.22 μm的微孔滤膜过滤后待测。
测定核苷类物质:取2 mL酒样用0.22 μm的微孔滤膜过滤后待测。
1.3.2 检测方法
色谱柱:Agilent C18柱(4.6 mm×250 mm,5 μm);检测γ-氨基丁酸的流动相A为乙腈,B为50 mmol/L三水合乙酸钠;检测核苷类物质流动相A为甲醇,B为水,具体色谱条件见表1。
表1 色谱条件
Table 1 The chromatographic conditions

波长/nm γ-氨基丁酸 35 ∶65 5 1.0 40 436核苷类物质 10∶90 10 0.8 40 254检测物质 流动相A∶B(体积比)进样量/μL流速/(mL/min)柱温/℃
1.3.3 标准曲线绘制
取1.3.1.1中的系列标准工作溶液在1.3.2相应的色谱条件下进行测定,以标准物浓度(C)为横坐标,其对应峰面积值(S)为纵坐标,分别建立γ-氨基丁酸和核苷类物质的标准曲线。
1.3.4 精密度试验
取0.50 mg/L的γ-氨基丁酸标准品和核苷类物质混合标准品(尿苷:1.00 mg/L;腺苷:10.00 mg/L)各6份,分别在1.3.2相应的色谱条件下测定含量,计算相对标准偏差(relative standard deviation,RSD)。
1.3.5 加标回收率试验
取2号酒样分别添加0.5、1.0、2.0 mg/L的3种浓度的γ-氨基丁酸标准品,随后衍生化处理;另取2号酒样添加尿苷浓度分别为1、2、5 mg/L,腺苷浓度分别为10、20、50 mg/L混合标准工作溶液,以上加标样品均用0.22 μm的微孔滤膜过滤后,在1.3.2相应的色谱条件下重复测定3次,计算加标回收率和相对标准偏差。
1.3.6 数据处理
色谱数据分析采用仪器自带软件Agilent Chem-Station进行处理。所有线性方程、精密度及回收率试验的数据均由Office Excel 2016处理得出。
2 结果与分析
2.1 色谱条件的优化
γ-氨基丁酸色谱条件的优化:通过对γ-氨基丁酸标准样品的全波长扫描发现,γ-氨基丁酸在436 nm处具有最大吸收峰,因此确定检测波长为436 nm。本试验分别采用50%、55%、60%、65%、70%、75%这6种比例的流动相B进行试验。结果显示,当流动相B为65%时,γ-氨基丁酸的峰型对称,基线稳定。当流速由0.6 mL/min逐渐递增到1.2 mL/min时,γ-氨基丁酸的峰均能分离,但峰保留时间变短且柱压出现波动式变化,使得峰型较差。当流速为1.0 mL/min时,柱压稳定,色谱峰保留时间未发生偏移且峰型最佳。本试验发现在4种不同的柱温条件下,γ-氨基丁酸的分离效果均较好,说明柱温对其影响较小。综合峰型、对色谱柱的保护和柱压稳定性的因素,确定了最佳色谱检测条件:进样量5 μL,流动相A∶B=35∶65(体积比),流速为1.0mL/min,柱温 40℃,检测波长为436 nm。该色谱条件下γ-氨基丁酸标准溶液的色谱图见图1。
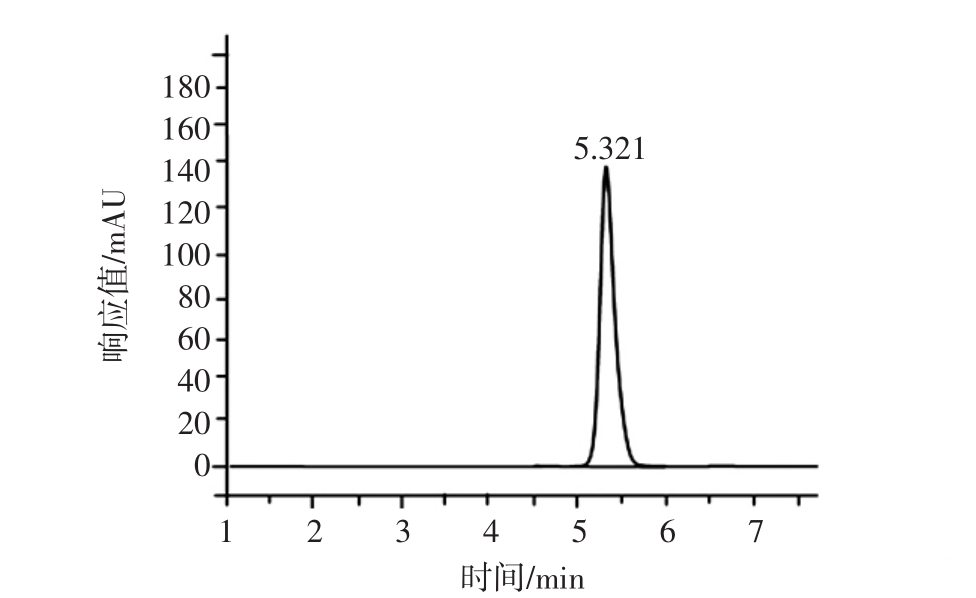
图1 γ-氨基丁酸标准溶液色谱图
Fig.1 The GABA standard solution chromatogram
由图1可知,GABA的保留时间为5.321 min。
核苷类物质检测色谱条件的优化:查阅测定核苷类物质的相关文献[19],确定色谱检测波长为254 nm;本试验分别采用10%、20%、30%、40%、50%这5种甲醇浓度的流动相,发现随着甲醇浓度的升高,腺苷、尿苷与样品中其他组分的分离度降低,出现峰分裂和小峰的现象。当甲醇浓度为10%时,样品中腺苷、尿苷的峰型良好,分离度高,且无拖尾现象。另外,本文考察了0.6、0.8、1.0、1.2 mL/min 这 4 种流速下的分离效果,结果发现在这4种流速下,腺苷和尿苷都完全分离,流速增大虽改善了标准色谱峰与杂质峰的分离度,但流速过高会使峰形变差,柱压显著波动。发现柱温在30℃到50℃之间对色谱峰型与分离效果无明显影响。综合上述结果,确定了最佳色谱检测条件:进样量10 μL,流动相10%甲醇,体积流量为0.8 mL/min,柱温40℃,检测波长为254 nm。该色谱条件下核苷类物质混合标准溶液的色谱图见图2。可知,尿苷、腺苷的保留时间分别为 4.191、11.625 min。
2.2 标准曲线
将γ-氨基丁酸的系列标准溶液以及尿苷和腺苷的混合系列标准溶液分别在2.1的色谱条件下测定,以标准品的浓度为横坐标(C),标准品峰面积为纵坐标(S),绘制标准曲线,得回归方程,结果见表2。
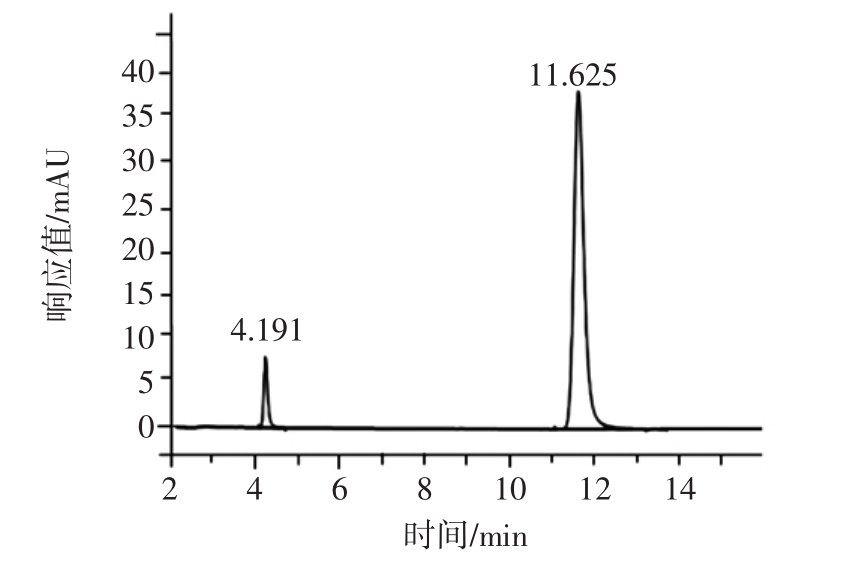
图2 核苷类物质标准溶液色谱图
Fig.2 The two nucleoside substances standard solution chromatogram
表2 回归曲线、相关系数、线性范围
Table 2 The standard curve,correlation index,linearity range
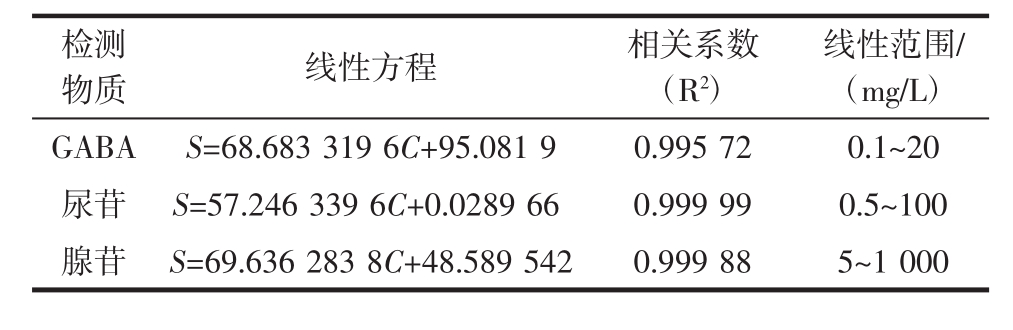
线性范围/(mg/L)GABA S=68.683 319 6C+95.081 9 0.995 72 0.1 ~20尿苷 S=57.246 339 6C+0.0289 66 0.999 99 0.5 ~100腺苷 S=69.636 283 8C+48.589 542 0.999 88 5 ~1 000检测物质 线性方程 相关系数(R2)
由表2可知,所测物质线性相关系数R2≥0.995。采用此方法γ-氨基丁酸在0.1mg/L ~20 mg/L具有良好的线性,尿苷在0.5 mg/L ~100 mg/L具有良好的线性,腺苷在5 mg/L ~1 000 mg/L具有良好的线性,完全满足试验要求。
2.3 精密度试验
通过标准曲线得γ-氨基丁酸、腺苷和尿苷含量,计算相对标准偏差值,结果见表3和表4。
表3 γ-氨基丁酸精密度试验结果(n=6)
Table 3 Results of GABA precision detection(n=6)

测定次数仪器测定值/(mg/L)均值/(mg/L)RSD/%1 0.503 0.505 2.37 2 0.489 3 0.521 4 0.513 5 0.495 6 0.511
由表3和表4可知,γ-氨基丁酸的RSD值为2.37%,尿苷的RSD为1.76%,腺苷的RSD为1.99%,均<5%,可见此法的精密度良好,满足分析要求。
2.4 加标回收率
γ-氨基丁酸和核苷类物质的加标回收率结果分别见表5和表6。
由表5和表6可知,GABA加标回收率在97.93% ~99.72%之间,核苷类物质回收率在97.90% ~101.15%,RSD均<5.0%,表明本方法准确可靠,可以满足测定的要求。
表4 核苷类物质精密度试验结果(n=6)
Table 4 Results of nucleoside substances precision detection(n=6)

项目测定次数仪器测定值/(mg/L)均值/(mg/L)RSD/%尿苷 1 1.025 0.999 1.76 2 1.010 3 0.976 4 0.986 5 1.005 6 0.994腺苷 1 10.143 10.049 1.99 2 9.896 3 9.797 4 10.075 5 10.371 6 10.015
表5 GABA加标回收率试验结果(n=3)
Table 5 Results ofGABA adding standard recovery rate tests(n=3)
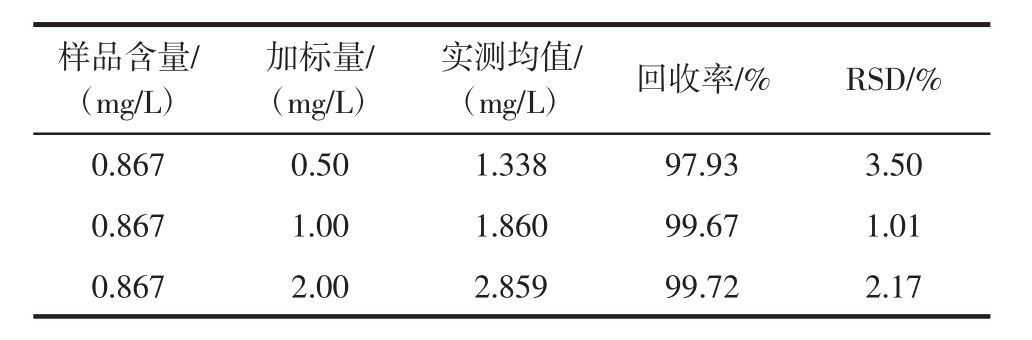
样品含量/(mg/L)加标量/(mg/L)实测均值/(mg/L) 回收率/% RSD/%0.867 0.50 1.338 97.93 3.50 0.867 1.00 1.860 99.67 1.01 0.867 2.00 2.859 99.72 2.17
表6 核苷类物质加标回收率试验结果(n=3)
Table 6 Results of nucleoside substances adding standard recovery rate tests(n=3)

项目 样品含量/(mg/L)RSD/%尿苷 1.056 1.0 2.035 97.90 4.84 1.056 2.0 3.079 101.15 4.14 1.056 5.0 6.057 100.00 2.96腺苷 27.518 10.0 37.407 98.89 3.39 27.518 20.0 47.403 99.43 2.93 27.518 50.0 77.260 99.48 1.60加标量/(mg/L)实测均值/(mg/L)回收率/%
2.5 样品测定
应用2.1确定的色谱条件对20种白酒进行测定见表7。
γ-氨基丁酸在20种白酒中的含量在0.102 mg/L ~0.867mg/L之间,其中酱香型白酒的含量在0.143 mg/L ~0.188 mg/L之间,浓香型白酒的含量在0.102 mg/L ~0.867 mg/L之间,芝麻香型白酒和部分酱香型白酒中未检测到。李波等[20]发现GABA在发酵过程中可以作为酵母的氮源被酵母很好的利用。部分白酒中未检测到GABA,可能是由于在发酵过程中被消耗,进而未检测出。此外,1号 ~9号白酒中浓香型白酒GABA的含量在0.239 mg/L ~0.867 mg/L之间,高于酱香型白酒,同时也高于大部分市售酒样。2号浓香型白酒中GABA的含量最高,达到0.867 mg/L,其次为1号酒样达到0.659 mg/L。因2号样品储存时间相比其他样品久,在本次试验中,储存时间越长,GABA的含量越高。但储存时间的长短与GABA的含量之间是否有一定的规律性还需进行大量试验验证。
表7 样品测定结果
Table 7 The results of samples

注:nd表示未检出;-表示不在线性范围内。
样品香型/酒度GABA/(mg/L)尿苷/(mg/L)腺苷/(mg/L)样品香型/酒度GABA/(mg/L)尿苷/(mg/L)腺苷/(mg/L)1 浓香/38° 0.659 - 10.043 11 浓香/38° 0.285 0.670 30.920 2 浓香/38° 0.867 1.056 27.518 12 浓香/38° 0.102 1.350 32.050 3 浓香/60° 0.239 2.800 51.371 13 浓香/42° - 0.770 15.970 4 酱香/52° 0.188 8.657 69.600 14 浓香/42° 0.154 1.200 29.900 5 酱香/53° 0.143 6.584 94.418 15 浓香/42° - 1.020 20.960 6 酱香/53° nd 3.368 66.421 16 浓香/42° 0.154 0.580 13.810 7 酱香/56° nd 8.140 145.600 17 浓香/52° - 3.030 39.270 8 芝麻香/60° nd 4.570 140.560 18 浓香/52° 0.129 1.770 59.280 9 芝麻香/52° nd 5.500 433.460 19 浓香/52° - 2.640 53.760 10 浓香/38° nd 0.890 19.480 20 浓香/60° nd 2.870 70.160
酒样中核苷类成分检测率为100%,检测到20种白酒中腺苷的含量在10.043 mg/L ~433.460 mg/L之间,尿苷的含量在0.580 mg/L ~8.657 mg/L之间。相比于酱香型和浓香型白酒,芝麻香型白酒中腺苷的含量较高,9号达到433.460 mg/L。酱香型白酒中尿苷含量最高,4号达到8.657 mg/L;其次为芝麻香型白酒,浓香型白酒含量最低。测定结果表明,该酒厂中酱香型(4号 ~6号)和芝麻香型(8号、9号)白酒中这两种核苷类物质含量高于市售酒样,而浓香型白酒(1号 ~3号)则与市售酒样相差不大。
可见,不同香型酒之间GABA和核苷类物质的含量均存在差异。研究报道[21-23],酿造工艺(如原料、酒曲等)对发酵产品中GABA的含量影响显著。不同香型白酒酿造工艺不同,各地气候、环境及微生物的差异很大,但酿造工艺是如何使得不同白酒中GABA、核苷类物质在含量上产生以上差异还需要进一步探究。核苷类物质含量差异与制曲、堆积工艺等关系也需进一步的研究。因此,采用简便快捷的方法测定白酒中的GABA和核苷类物质,对未来探究不同香型白酒中GABA和核苷类物质差异原因有着重要意义。
3 结论
本文建立利用高效液相色谱法精确测定白酒中GABA以及核苷类物质(尿苷、腺苷)的方法,并对20种白酒其功能成分进行测定,发现不同种类的白酒中含量不尽相同。20种白酒中GABA的含量在0.102 mg/L ~0.870mg/L之间,腺苷的含量在10.043mg/L ~433.460mg/L之间,尿苷的含量在0.580 mg/L ~8.657 mg/L之间。分析结果显示,GABA在浓香型白酒中较高,核苷类物质在芝麻香型和酱香型白酒中要高于浓香型白酒。本研究通过对色谱条件的优化以及对精密度、回收率的测定,充分证明了试验的可行性,具有较高的参考价值。本文建立的方法操作简便,灵敏度高,适用范围广,适用于大量样本的测定,为后期探索功能成分合成机制以及酿造工艺如何影响其在白酒中的含量奠定了技术基础。
[1]杨晓,伍时华,吴佳敏,等.五粮生料液态发酵酿造浓香型白酒的初步试验[J].中国酿造,2019,38(10):35-39.
[2]许德富,张宿义,杨平,等.中国白酒的高品质发展趋势[J].酿酒,2019,46(1):17-20.
[3]袁帅.用16SrDNAV4区高通量测序分析两种酒糟细菌多样性[D].贵阳:贵州师范大学,2014.
[4]范文来,徐岩,黄永光.白酒对健康有益还是有害?[J].酿酒科技,2014(11):1-5.
[5]范文来,徐岩.白酒风味物质研究方法的回顾与展望[J].食品安全质量检测学报,2014,5(10):3073-3078.
[6]张金修,李静,郭芳文.白酒中微量成分对人体的作用 [J].酿酒科技,2014(10):143.
[7]周金虎,管健,魏浩林,等.白酒中健康因子的研究进展[J].酿酒科技,2017(7):90-94.
[8]Yogeeswari P,Patel S K,Reddy I V,et al.GABA derivatives for the treatment of epilepsy and neuropathic pain:a synthetic integration of GABA in 1,2,4-Triazolo-2H-one nucleus[J].Biomedicine&Aging Pathology,2012,2(2):31-40.
[9]Wu C,Sun D D.GABA receptors in brain development,function,and injury[J].Metabolic Brain Disease,2015,30(2):367-379.
[10]Ma P J,Li T,Ji F C,et al.Effect of GABA on blood pressure and blood dynamics of anesthetic rats[J].International Journal of Clinical and Experimental Medicine,2015,8(8):14296-14302.
[11]郑红发,黄亚辉,刘霞林,等.γ—氨基丁酸的药理作用 [J].茶叶通讯,2004,31(4):14-18.
[12]Ullah A,Jahan S,Razak S,et al.Protective effects of GABA against metabolic and reproductive disturbances in letrozole induced polycystic ovarian syndrome in rats[J].Journal of Ovarian Research,2017,10(1):1-8.
[13]Nguyen B C Q,Shahinozzaman M,Tien N T K,et al.Effect of sucrose on antioxidant activities and other health-related micronutrients in Gamma-aminobutyric acid (GABA)-enriched sprouting Southern Vietnam brown rice[J].Journal of Cereal Science,2020,93:102985.
[14]Leventhal A G,Wang Y C,Pu M L,et al.GABA and its agonists improved visual cortical function in senescent monkeys[J].Science,2003,300(5620):812-815.
[15]Dobolyi A,Juhász G,Kovács Z,et al.Uridine function in the central nervous system[J].Current Topics in Medicinal Chemistry,2011,11(8):1058-1067.
[16]Olatunji O J,Feng Y,Olatunji O O,et al.Neuroprotective effects of adenosine isolated from Cordyceps cicadae against oxidative and ER stress damages induced by glutamate in PC12 cells[J].Environmental Toxicology and Pharmacology,2016,44:53-61.
[17]张星星,毛清黎,孙俊,等.高效液相色谱法测定红曲发酵食品中洛伐他汀的研究[J].中国酿造,2020,39(5):193-196.
[18]Chen L,Luo S L,Chen J L,et al.A comparative analysis of endophytic bacterial communities associated with hyperaccumulators growing in mine soils[J].Environmental Science and Pollution Research,2014,21(12):7538-7547.
[19]孙忠华,肖建辉,迟强,等.高效液相色谱法测定三种虫草发酵液与菌丝体核苷化合物含量[J].天然产物研究与开发,2014,26(12):2000-2003,2061.
[20]李波,李磊,邓旭衡,等.葡萄酒发酵过程中γ-氨基丁酸含量变化的研究[J].中国酿造,2011,30(7):171-173.
[21]张荣霞,李崎,朱林江,等.青稞红曲啤酒中γ-氨基丁酸(GABA)的研究[J].食品与生物技术学报,2018,37(11):1148-1152.
[22]周艳华,李涛,刘颖.富含γ-氨基丁酸保健啤酒的酿造工艺研究[J].食品工业,2018(5):83-87.
[23]钱敏,汤斯斯,赵文红,等.原料米对广东客家黄酒发酵及产γ-氨基丁酸的影响[J].食品工业科技,2018,39(7):15-19.