在世界粮食生产中,玉米占有重要地位,而我国玉米的种植面积及产量在世界均位居前列,相应的玉米芯产量也较高[1],玉米芯具有组织均匀、硬度适宜、韧性好、吸水性强、耐磨性能好等优点,在使用过程中易破碎[2]。虽然玉米芯的优点很多,但综合利用率并不高,只有少量玉米芯用作糠醛、木糖醇等产品的原料,大部分玉米芯还是被丢弃或者作为燃料烧掉,造成资源极大的浪费[3]。因此开展以玉米芯为原料生产低聚木糖,理论研究和生产技术研究是十分必要的。
玉米芯中含有大量的半纤维素、纤维素和木质素,其中半纤维素的主要成分为戊聚糖,它通过降解可生产低聚木糖[4]。低聚木糖系由2个~7个木糖分子以α-1,4糖苷键结合而成,具有良好的生理活性,如促进双歧杆菌增长调节肠道功能,抗肿瘤功能,增强益生菌功能以及免疫调节功能等。它的甜度比蔗糖和葡萄糖均低,仅为蔗糖的40%,具有抗龋齿性[5]。目前,工业上以玉米芯作为生产原料制备低聚木糖,一般采用酸法、碱法、蒸汽爆破法等方法预处理玉米芯提取戊聚糖。酸、碱法在生产过程中需要消耗大量酸、碱化学品,会造成严重的环境污染,且提取率较低[6]。蒸汽爆破法则需要加入少量的酸碱调节pH值,并且高温蒸汽爆破会导致半纤维素部分水解以及碳水化合物的破坏等副反应的产生[7]。所以提高戊聚糖提取率是使玉米芯充分利用的关键技术问题。
本研究采用高温热解法提取戊聚糖,将料液放入密闭的高温高压反应釜中,无需添加强酸、强碱等化学试剂,原料利用率高,且反应时间短,操作简便。在高温高压条件下,使戊聚糖能充分从半纤维素中溶出,提取率大幅度提升。此方法极大程度节省时间和能源,成本减小,对环境不造成生态破坏。为后续酶解工艺生产低聚木糖提供充足的原料。
1 材料与方法
1.1 材料与试剂
玉米芯粉:公主岭市双正玉米芯开发有限公司,过60目筛备用,水分质量分数4.91%。
氯化铁、地衣酚、无水乙醇、盐酸(均为分析纯):北京化工厂;D-木糖、木二糖 ~木六糖标准品:上海惠世生化试剂有限公司;葡萄糖、L-阿拉伯糖、低聚木糖:山东龙力生物科技股份有限公司;氮气:长春巨洋气体有限责任公司。
1.2 仪器与设备
ME204E型电子分析天平:德国梅特勒-托利多仪器有限公司;PHS-3C型精密pH计:上海雷磁仪器有限公司;WAY-3S型数字阿贝折射仪:上海仪电科学仪器股份有限公司;HH-ZKYY-5L型恒温水浴锅:上海科升仪器有限公司;1260Infinity型高效液相色谱仪、配蒸发光散射检测器:美国安捷伦公司;Varian Cary 300型紫外可见分光光度计:Australia PTY.LTD;FSH-2型反应釜:威海汇鑫化工机械有限公司;Vortex-2漩涡混匀仪:上海沪析实业有限公司;M6型沐美电子秤:深圳市沐美科技有限公司。
1.3 试验方法
1.3.1 原料玉米芯粉水分测定方法
参照GB/T5009.3—2016《食品安全国家标准食品中水分的测定》[8]。
1.3.2 戊聚糖的提取
称取过筛后的玉米芯粉,按固液比1∶15(g/mL)加水配制成1 500 g的浆液,用玻璃棒搅拌均匀,倒入反应釜中,盖严釜盖,不得有漏气的现象,在热解温度为180℃,热解时间为60 min条件下,得到提取液,取上清液10mL,加入10mL 4mol/L的盐酸溶液,置于25mL具塞试管内,置于沸水浴中水解120 min,冷却后用滤纸过滤,收集滤液备用(可适当稀释n倍)[9-10]。
1.3.3 单因素试验
1.3.3.1 固液比对戊聚糖提取率的影响
试验采用了固液比分别为 1 ∶7、1 ∶10、1 ∶15、1 ∶20(g/mL)的4个水平,在热解温度为180℃,热解时间为60min条件下进行试验操作。分析不同固液比对可溶性戊聚糖含量的影响,以确定适宜的固液比范围。
1.3.3.2 热解温度对戊聚糖提取率的影响
试验采用了热解温度分别为 140、160、180、200、220℃的 5个水平,在固液比为 1∶15(g/mL),热解时间为60 min条件下进行试验操作。分析不同热解温度对可溶性戊聚糖含量的影响,以确定适宜的热解温度范围。
1.3.3.3 热解时间对戊聚糖提取率的影响
试验采用了热解时间分别为 0、30、60、90、120 min的5个水平,在固液比为1∶15(g/mL),热解温度为180℃条件下进行试验操作。分析不同热解时间对可溶性戊聚糖含量的影响,以确定适宜的热解时间范围。
1.3.4 正交试验
根据单因素试验结果,确定主要影响因素固液比、热解温度、热解时间3项为考察因素,依据正交试验表进行设计,做三因素三水平正交试验,以确定玉米芯中戊聚糖提取的最适工艺条件[11],正交试验因素水平表见表1。
表1 正交试验因素水平表
Table 1 The factors and levels of orthogonal experiment
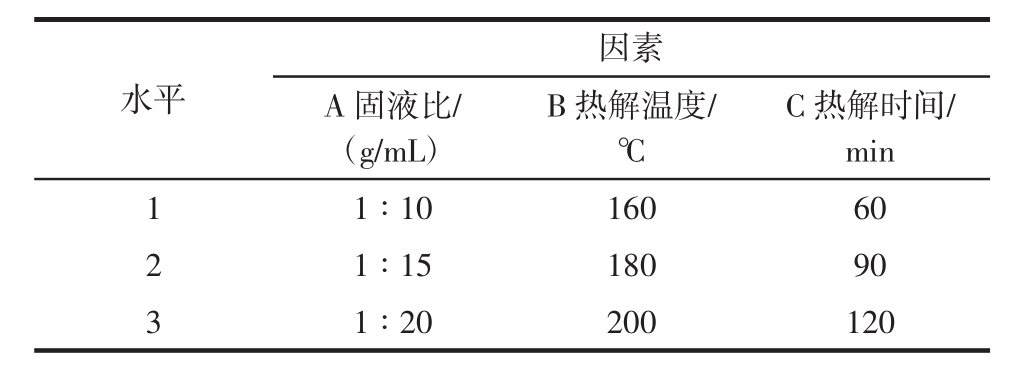
水平C热解时间/min 1 1∶10 160 60 2 1∶15 180 90 3 1∶20 200 120因素A固液比/(g/mL)B热解温度/℃
1.3.5 木糖标准曲线
取6支洁净的10 mL具塞试管,分别加入100 μg/mL的D-木糖标准溶液 0.0、0.4、0.8、1.2、1.6、2.0 mL,补加蒸馏水至3 mL。再依次加入0.3 mL 1%地衣酚-无水乙醇溶液和3 mL 0.1%氯化铁-盐酸溶液,具塞,用漩涡混匀仪混合均匀。沸水浴30 min后,取出试管,流水冲洗冷却至25℃,转移至10 mL容量瓶,用水定容,用1 cm比色皿,以D-木糖标准溶液量为0.0的试剂溶液做参比,分别测定在670、580 nm波长下的吸光值,计算两者之差(ΔA)[12-14]。以ΔA为纵坐标,D-木糖量为横坐标,建立标准曲线和回归方程。
1.3.6 戊聚糖提取率的计算
准确量取1.2.2制备的样品液0.33 mL定容至100 mL,取3 mL于10 mL具塞试管内,按测定木糖标准曲线相同的方法测吸光度,并根据标准曲线得到木糖含量,带入公式计算戊聚糖提取率。每组试验分别进行3次平行试验,以3次试验的平均值计[15-16]。具体样品检测参照NY/T 2335-2013《谷物中戊聚糖含量的测定-分光光度法》。计算公式如下。
式中:X为试样中戊聚糖提取率,%;c为D-木糖标准曲线得到的D-木糖含量,μg;0.88为单糖与聚糖的转换系数;n为稀释倍数;m为样品质量,g。
1.3.7 玉米芯组织结构扫描电镜分析
采用扫面电子显微镜(scanningelectronmicroscope,SEM)分别对粉碎后的玉米芯和经160、180、200℃高温热解后的玉米芯粉干燥样品微观结构进行分析,观察不同温度处理条件下玉米芯表面形态变化[17]。
1.3.8 高效液相色谱定性分析
利用高效液相色谱仪,蒸发光散射检测器检测高温热解液中的戊聚糖,色谱条件为:SUGARKS-802钠型阳离子色谱柱8.0 mm×300 mm,氮气为载气,超纯水为流动相,柱温箱设定在80℃,进样量20 μL,流速为0.6 mL/min,将热解液稀释至一定的质量分数,再经过0.22 μm膜过滤,收集滤液进行高效液相检测,通过比较标准品与高温热解液组分峰的保留时间进行定性分析[18-19]。
1.4 数据处理
全部试验结果用Excel 2016和SPSS 19.0进行数据处理分析。方差分析时,p<0.05或p<0.01,表示具有显著性差异或极显著差异,试验结果具有统计学意义。
2 结果与分析
2.1 木聚糖标准曲线
绘制标准曲线见图1。计算得线性回归方程为y=0.111 2x-0.002 6,线性相关系数0.999 3。
2.2 单因素试验结果
2.2.1 固液比对戊聚糖提取率的影响
固液比对戊聚糖提取率的影响见图2。
从图2可以看出,固液比对戊聚糖的提取效果影响显著,在固液比从 1 ∶7(g/mL)到 1 ∶20(g/mL)的过程中,随着干物质的添加量不断减少,戊聚糖提取率呈现出先增大后减小的趋势,在固液比为1∶15(g/mL)时,提取率达到了最大值。在固液比1∶7(g/mL)时干物质居多,玉米芯不能充分润胀,热解反应不完全,戊聚糖不能完全溶出。
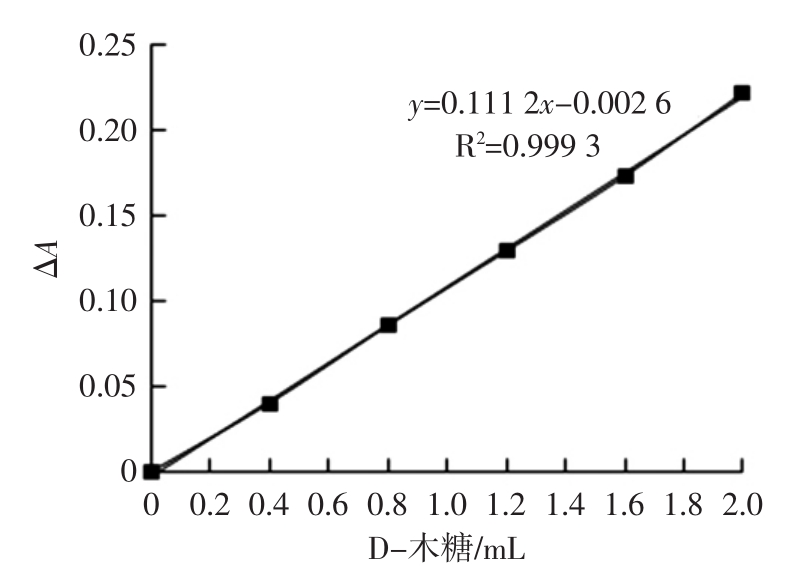
图1 木糖标准曲线
Fig.1 The standard curve of D-xylopyranose
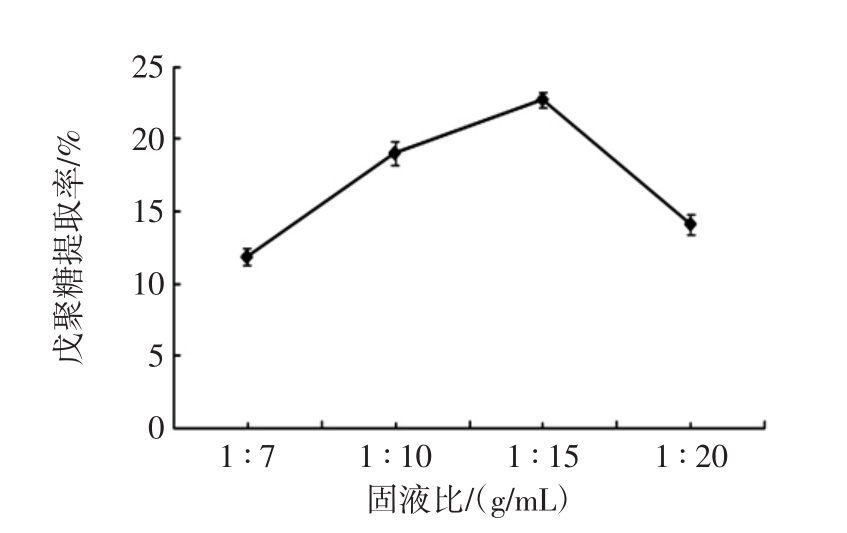
图2 固液比对戊聚糖提取率的影响
Fig.2 Effects of solid-liquid ratio on pentosan content
2.2.2 热解时间对戊聚糖提取率的影响
热解时间对戊聚糖提取率的影响见图3。
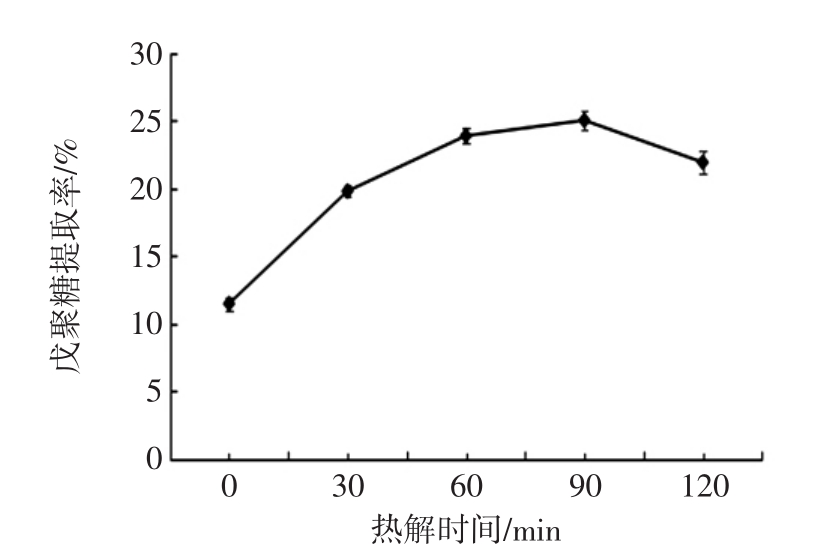
图3 热解时间对戊聚糖提取率的影响
Fig.3 Effects of pyrolysis time on pentosan content
从图3可见,随着提取时间的延长,戊聚糖提取率呈现先上升后下降的趋势,30 min到90 min戊聚糖提取率增长缓慢,在90 min戊聚糖提取率达到了最大值25.01%,但随着时间的增长,提取液颜色加深,会使后续脱色工艺增加难度。在120 min时戊聚糖提取率会下降是因为玉米芯中的半纤维素过多地转化成单糖。
2.2.3 热解温度对戊聚糖提取率的影响
热解温度对戊聚糖提取率的影响见图4。
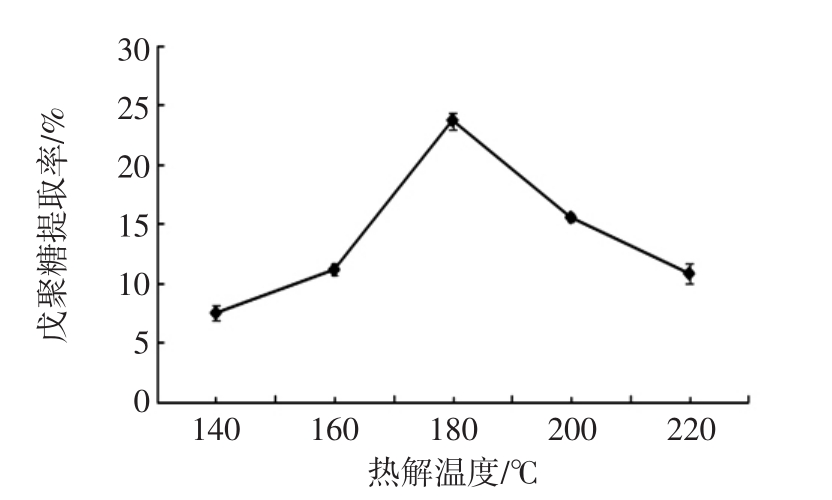
图4 热解温度对戊聚糖提取率的影响
Fig.4 Effects of pyrolysis temperature on pentosan content
从图4可见,热解温度对戊聚糖提取率有明显的影响,热解温度过高或过低都会导致戊聚糖提取率下降,从160℃到180℃,提取率迅速升高,在180℃时达到最大值23.68%,半纤维素溶解充分。热解温度从180℃到220℃,提取率迅速下降,原因是温度过高戊聚糖氧化变质,其它副产物大量析出。
从图4可见,热解温度对戊聚糖提取率有明显的影响,热解温度过高或过低都会导致戊聚糖提取率下降,从160℃到180℃,提取率迅速升高,在180℃时达到最大值23.68%,半纤维素溶解充分。热解温度从180℃到220℃,提取率迅速下降,原因是温度过高戊聚糖氧化变质,其它副产物大量析出。
2.3 正交试验优化工艺参数的结果与分析
正交试验结果与方差分析见表2、表3。
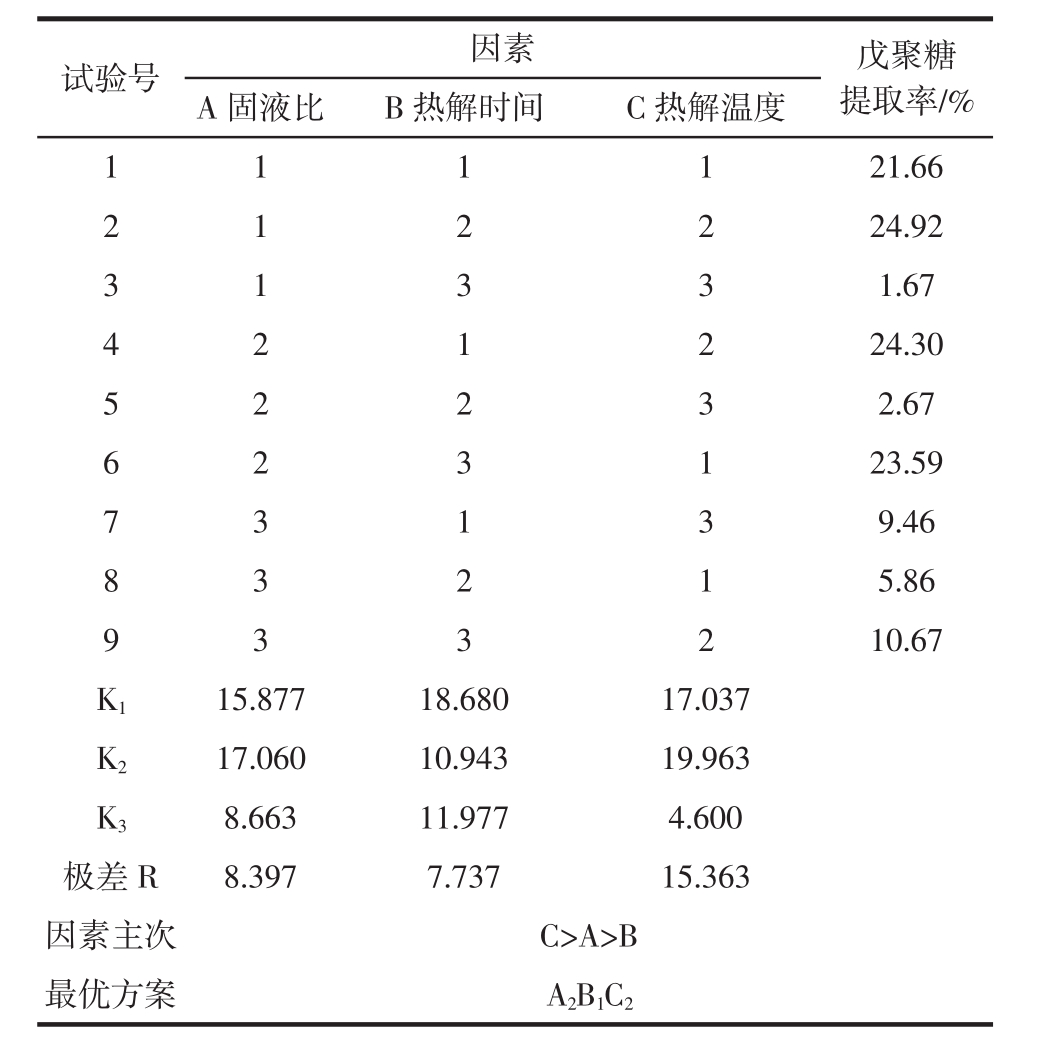
表2 正交试验设计与结果
Table 2 The design and results of orthogonal experiment
试验号 因素 戊聚糖提取率/%A固液比 B热解时间 C热解温度1 1 1 1 21.66 2 1 2 2 24.92 3 1 3 3 1.67 4 2 1 2 24.30 5 2 2 3 2.67 6 2 3 1 23.59 7 3 1 3 9.46 8 3 2 1 5.86 9 3 3 2 10.67 K1 15.877 18.680 17.037 K2 17.060 10.943 19.963 K3 8.663 11.977 4.600极差R 8.397 7.737 15.363因素主次 C>A>B最优方案 A2B1C2
由表2中极差分析可知,3个因素对戊聚糖提取率的影响主次顺序为:C>A>B,即热解温度>固液比>热解时间,玉米芯提取戊聚糖的最佳工艺条件为A1B2C2,提取率为24.92%。由K值分析可知,玉米芯提取戊聚糖的最佳工艺条件为A2B1C2,对该条件进行3次验证试验,平均提取率为25.84%,不仅时间缩短,还节省原
由表2中极差分析可知,3个因素对戊聚糖提取率的影响主次顺序为:C>A>B,即热解温度>固液比>热解时间,玉米芯提取戊聚糖的最佳工艺条件为A1B2C2,提取率为24.92%。由K值分析可知,玉米芯提取戊聚糖的最佳工艺条件为A2B1C2,对该条件进行3次验证试验,平均提取率为25.84%,不仅时间缩短,还节省原料,大大降低了成本,即确定固液比1∶15(g/mL),热解时间60 min,热解温度180℃为玉米芯提取戊聚糖的最佳工艺条件。由表3的方差分析结果可知,热解温度对戊聚糖提取率有显著性影响。料,大大降低了成本,即确定固液比1∶15(g/mL),热解时间60 min,热解温度180℃为玉米芯提取戊聚糖的最佳工艺条件。由表3的方差分析结果可知,热解温度对戊聚糖提取率有显著性影响。
表3 正交试验方差分析
Table 3 Analysis of variance for orthogonal
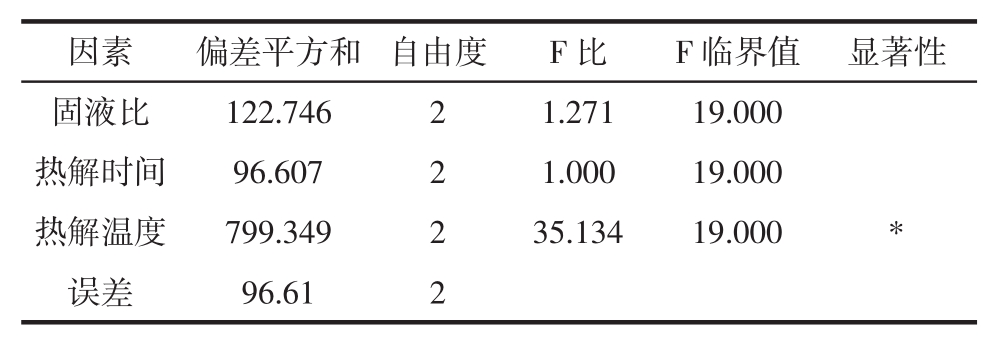
注:*差异显著(P<0.05)。
因素 偏差平方和 自由度 F比 F临界值 显著性固液比 122.746 2 1.271 19.000热解时间 96.607 2 1.000 19.000热解温度 799.349 2 35.134 19.000 *误差 96.61 2
2.4 玉米芯扫描电镜结果分析
不同处理条件下的扫描电镜图见图5。

图5 不同处理条件下的扫描电镜图
Fig.5 Scanning electron micrograph of different processing conditions
如图5A所示,未处理过的玉米芯粉组织结构呈现出黏性较大,结块的状态,表面完整度较高,内部结构紧密。如图5B所示,160℃热解后的样品组织内部出现蜂窝状的小孔,结构稍有松散。如图5C所示,180℃热解后的样品呈现完全松散状态,不规则的小碎片,边缘全部卷曲。如图5D所示,200℃热解后的样品内部结构完全被破坏,呈焦糊不规则微小颗粒状。说明随着热解温度的不断提高,玉米芯中大量的纤维素、半纤维素和木质素在高温热解后受到破坏,分解出过多低聚合度的糖类物质。
如图5A所示,未处理过的玉米芯粉组织结构呈现出黏性较大,结块的状态,表面完整度较高,内部结构紧密。如图5B所示,160℃热解后的样品组织内部出现蜂窝状的小孔,结构稍有松散。如图5C所示,180℃热解后的样品呈现完全松散状态,不规则的小碎片,边缘全部卷曲。如图5D所示,200℃热解后的样品内部结构完全被破坏,呈焦糊不规则微小颗粒状。说明随着热解温度的不断提高,玉米芯中大量的纤维素、半纤维素和木质素在高温热解后受到破坏,分解出过多低聚合度的糖类物质。
2.5 高效液相色谱法结果分析
通过高效液相色谱法对戊聚糖提取液进行定性定量分析,本试验使用SUGARKS-802钠型阳离子糖析专用色谱柱,较好地分离开提取液中的糖类物质,戊聚糖提取液样品液相检测结果见图6。
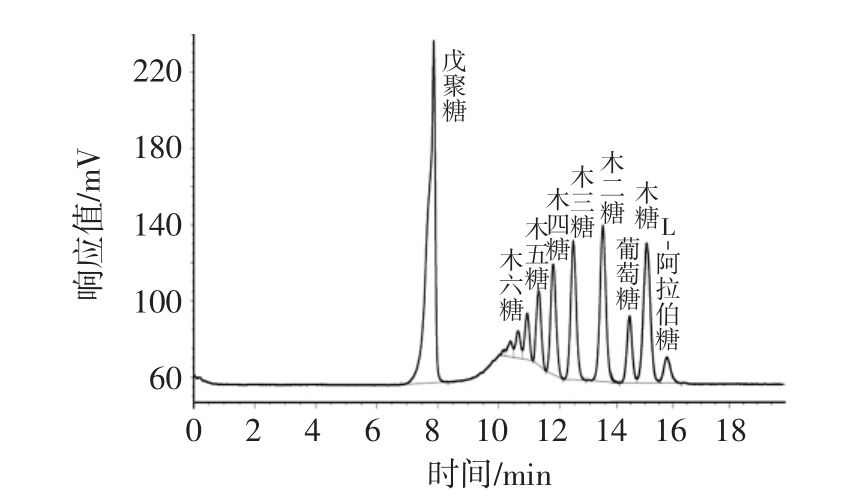
图6 戊聚糖提取液样品色谱图
Fig.6 Chromatogram of pentosan extract sample
通过与标准品的出峰时间对比,确定提取液中含有戊聚糖、木二糖、木三糖、木四糖、木五糖和木六糖等低聚糖,以及葡萄糖、木糖和L-阿拉伯糖3种单糖。通过计算峰面积低聚糖含量高达80.375%。这一结果有利于生产低聚木糖[20-22]。
3 结论
1)本研究采用高温热解法处理玉米芯提取戊聚糖,通过单因素试验和L9(33)正交试验,确定最佳提取工艺条件为固液比1∶15(g/mL),热解温度180℃,热解时间60 min,提取率为25.84%。
2)通过高效液相色谱法进行提取液组分分析结果表明,提取液中含有大量的戊聚糖、木二糖、木三糖、木四糖、木五糖和木六糖。这些糖类物质正是后续酶解工艺所需的低聚糖,可生产大量的低聚木糖。
3)通过扫描电子显微镜的结果显示高温热解对玉米芯组织结构有很大影响,结构状态完全变化。在180℃高温条件下处理的样品结构完全松散,表面积与体积比增大,大大增加了酶解作用,为后序工艺提供了更有利的条件。
4)本试验的目的是利用玉米芯高温热解法提取大量的戊聚糖等低聚糖,通过酶解可以获得大量的低聚木糖,玉米芯具有产量大、价格低的优势,高温热解法不使用强酸、强碱等化学试剂,无污染的优点为后续工艺提供方便,且戊聚糖提取率较高,对实现生物资源的可持续发展具有重要意义。
[1]张培刚,张静文,张凤清.玉米芯中低聚木糖的定性定量研究[J].食品科学,2009,19(30):125-127.
[2]Zhang H,Xu Y,Yu S.Co-production of functional xylooligosaccharides and fermentable sugars from corncob with effective acetic acid prehydrolysis[J].Bioresource Technology,2017,234(15):343-349.
[3]汤卫华,殷海松,刘鹏,等.玉米芯复合酶制备低聚木糖工艺的研究[J].食品研究与开发,2014,35(18):135-38.
[4]隋明,荣加超,张阳,等.酶法制备麸皮中低聚木糖的研究[J].包装与食品机械,2012,30(1):5-9.
[5]侯丽芬,孙向阳,丁长河,等.碱性H2O2预处理玉米芯酶法生产低聚木糖的研究[J].农业机械,2013(6):76-79.
[6]Samanta A K,Jayapal N,Kolte A P,et al.Process for Enzymatic Production of Xylooligosaccharides from the Xylan of Corn Cobs[J].Journal of Food Processing and Preservation,2014,44(8):1405-1413.
[7]李秀婷,孙宝国,宋焕禄,等.玉米芯水不溶性木聚糖的碱法提取及酶解分析[J].中国食品学报,2010,10(5):171-176.
[8]何凤林,沈生文,曾颖,等.玉米芯碱法提取木聚糖及其酶解制备低聚木糖的工艺研究[J].包装与食品机械,2015,33(6):28-33.
[9]魏涛,赵建元,高兆兰,等.低聚木糖调节BALB/c小鼠肠道菌群及润肠通便作用研究[J].安徽农业科学,2013,4(1):159-163.
[10]TENG Chao,YAN Qiaojuan,JIANG Zhengqiang,et al.Production of xylooligosaccharides from the steam explosion liquor of corncobs coupled with enzymatic hydrolysis using a thermostable xylanase[J].Bioresour Technol,2010,101(19):7679-7682.
[11]许丙磊,彭奇均.玉米芯蒸汽爆破处理的研究及响应曲面法优化[J].林产化学与工业,2010,30(6):64-66.
[12]范丽,徐勇,勇强,等.蒸汽爆破强度对玉米芯酶水解制备低聚木糖的影响[J].食品科学,2012,33(22):39-43.
[13]张明霞,庞建光,呼秀智.超声波处理玉米芯制备低聚木糖的条件优化[J].食品工业,2015(4):62-66.
[14]姚笛,叶曼曼,李琳,等.响应面法优化玉米芯中低聚木糖的酶法提取工艺[J].中国粮油学报,2014,29(11):14-18.
[15]Mkelinen H,Juntunen M,Hasselwander O.Prebiotic Po-tential of Xylo-Oligosaccharides[J].Prebiotics and Probi-otics Science and Technology,2009,12(1):245-258.
[16]张玲,丁长河,阮文彬.低聚木糖的应用研究和产品开发进展[J].粮食与油脂,2015,28(2):9-12.
[17]孙军涛,张智超,肖付刚,等.采用高温高压预处理玉米芯和复合酶法制备低聚木糖研究[J].河南农业大学学报,2018,52(2):259-264.
[18]吴彬,马正智,周伟,等.从稻壳中提取制备低聚木糖研究进展[J].中国食品添加剂,2009,37(10):94-99.
[19]Otieno D O,Ahring B K.Athermochemical pretreatment process to produce xylooligosaccharides (XOS),arabinooligos-accharides(AOS)and mannooligosaccharides (MOS)from lignocellulosic biomasses[J].Bioresource technology,2012,112(78):285-292.
[20]Sari Mets muuronen,Katja Lyytikinen,Kaj Backfolk,et al.Determination of xylo-oligosaccharides in enzymatically hyd-rolysed pulp by liquid chromatography and capillary e-lectrophoresis[J].Cellulose,2013,20(2):1572-1582.
[21]Boonchuay P,Techapun C,Leksawasdi N,et al.An integrated process for xylooligosaccharide and bioethanol production from corncob[J].Bioresource technology,2018,256(39):399-407.
[22]晁正,冉玉梅,杨霞,等.麦麸中低聚木糖的制备及抗氧化活性研究[J].核农学报,2014,28(4):655-661.