在报告测量结果时不仅要给出测定的量值是多少,还应给出以数量表示的该值分散程度是多少[1]。它是测量质量的指标,用于判断该测定值的可靠程度。测量不确定度是“表征赋予被测量值分散性的非负参数”。本研究根据CNAS-CL07:2011《测量不确定度的要求》、JJF 1059.1-2012《测量不确定度评定与表示》的规定和JJG 169-2006《常用玻璃量器检定规程》,采用了于2020年7月1日实施的SN/T 2316-2019《出口动物源食品中阿散酸、硝苯砷酸、洛克沙砷残留量的检测方法》[2-4]中新增的检验方法,采用微波消解-液相色谱-原子荧光光谱法测定动物源食品中阿散酸、硝苯砷酸、洛克沙砷残留量,结合实验室日常检测能力与条件,进行测量不确定度分析与评定,为今后评价阿散酸、硝苯砷酸、洛克沙砷测定结果的准确性和可靠性提供技术依据。
1 材料与方法
1.1 材料、试剂与仪器
1.1.1 材料
鸡肝:市售。
1.1.2 试剂
甲醇(色谱级):德国Merck公司;盐酸、硼氢化钾、磷酸二氢钾、过硫酸钾(优级纯):国药集团化学试剂有限公司;氢氧化钠(优级纯):北京化工厂;三氟乙酸(优级纯):上海天莲精细化工有限公司。
1.1.3 仪器
LC-AFS9750型液相色谱-原子荧光光谱仪:北京海光公司;Multiwave PRO型微波消解系统:奥地利Anton Paar公司;T18组织匀浆机:德国IKA公司;Alpha 1-4/LD-plus型冻干机:德国Christ公司;Milli-Q Reference型超纯水仪:德国Millipore公司;VORTEX型涡轮混合器:美国Scientific Industries公司;3-30K型高速冷冻离心机:美国SIGMA公司;N-EVAP-24型水浴氮吹仪:美国Organomation Associates Inc公司。
1.2 方法
1.2.1 样品处理
称取试样2 g(精确至0.001 g)于微波辅助萃取罐中,加入25 mL甲醇溶液(1∶1,体积比),按照微波辅助萃取仪的标准操作步骤进行提取。提取完毕,取出冷却至25℃,10 000 r/min离心10 min。取10 mL上清液,氮气吹扫,用甲醇溶液(1∶1,体积比)定容至5 mL,经0.45 μm有机滤膜过滤后进行测定。按同一操作方法作空白试验。
1.2.2 标准溶液配制
阿散酸、硝苯砷酸、洛克沙砷标准工作液:准确称取适量的阿散酸、硝苯砷酸、洛克沙砷标准品,用去离子水配成浓度为500 μg/mL的标准储备液。再用去离子水稀释成1.00 mg/L标准工作液。
1.2.3 样品测定
设定好仪器测量最佳条件,根据所用仪器的型号和工作站设置相应的参数,点火及对仪器进行预热,预热30 min后进行标准曲线及试样溶液的测定。
1.3 测量模型的构建
1.3.1 被测物含量的测量模型
计算试样中阿散酸(或硝苯砷酸或洛克沙砷)残留量的公式如下:
式中:Xi为试样中被测物的残留量,mg/kg;c1为样液中被测物的浓度,μg/L;c0为空白液中被测物的浓度,μg/L;V为样液体积,mL;V1为吸取上清液体积,mL;V2为最终定容体积,mL;m为最终样液所代表的试样量,g。
1.3.2 标准工作曲线的测量模型
以标准系列溶液中目标化合物的浓度为横坐标,色谱峰面积为纵坐标,绘制标准曲线,得到公式如下:
式中:y为色谱峰面积;c为标准系列溶液中目标化合物的浓度,μg/L;a为斜率;b为截距。
不确定度来源见图1。
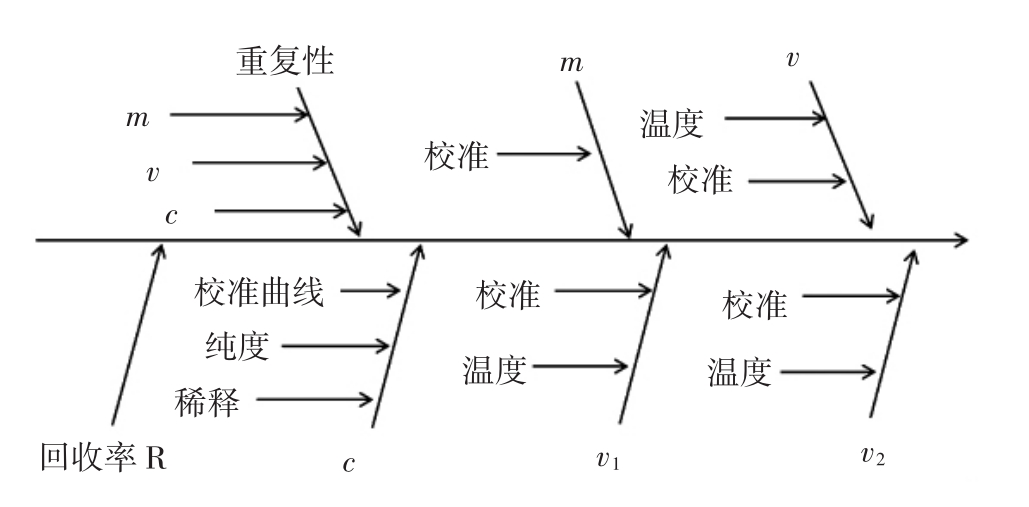
图1 不确定度来源的因果关系图
Fig.1 Causal relationship of the sources of uncertainty
2 结果与分析
2.1 试样质量m的不确定度评定
评估不确定度时,应集中精力分析最大的不确定度分量。质量m的不确定度有2个主要来源:一是重复性变化,可以通过10次连续称量测量,采用A类方法评定,该重复性通过试验合成重复性考虑;二是天平校准引入的不确定度,按B类方法评定。
检定校准证书上给出天平在20℃时的测量结果的不确定度U=4.5 mg,k=2,则天平的标准不确定度为uc(m)=4.5÷2=2.2 mg,其相对不确定度为ur(m)=uc(m)÷m=2.2÷2026=0.001 1。
2.2 体积V、V1、V2不确定度评定
该不确定度主要有3个方面:一是重复性变化,采用A类方法评定,该重复性也通过试验合成重复性考虑;二是校准不确定度,三是温度影响,均按B类方法评定。
2.2.1 校准引入的不确定度分量
根据检定校准证书,25 mL容量瓶的允差为±0.025 mL,10 mL 移液管的允差为±0.010 mL,5 mL容量瓶的允差为±0.005 mL。假设均为三角形分布,则包含因子为![]() ,因此标准不确定度分别为
,因此标准不确定度分别为![]()
![]()
![]()
2.2.2 温度系数引入的标准不确定度分量
检定或校准是在室温20℃环境条件下进行的[3],本研究的温度波动范围为±3℃(置信水平为95%)。水的体积膨胀系数为2.1×10-4℃-1假设正态分布,其包含因子为1.96。25 mL容量瓶、10 mL移液管和5 mL容量瓶,因温度控制不充分而产生的标准不确定度分别为:
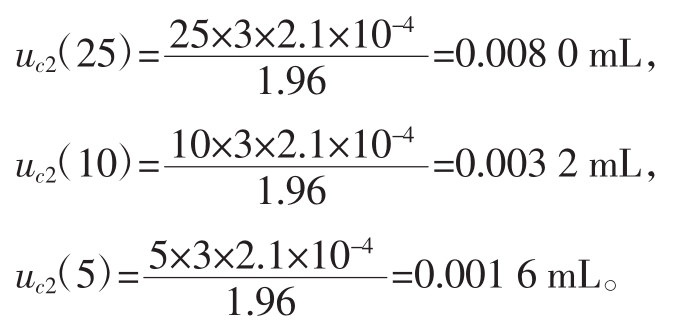
2.2.3 体积V、V1、V2的合成标准不确定度u(cV)、uc(V1)、u(cV2)
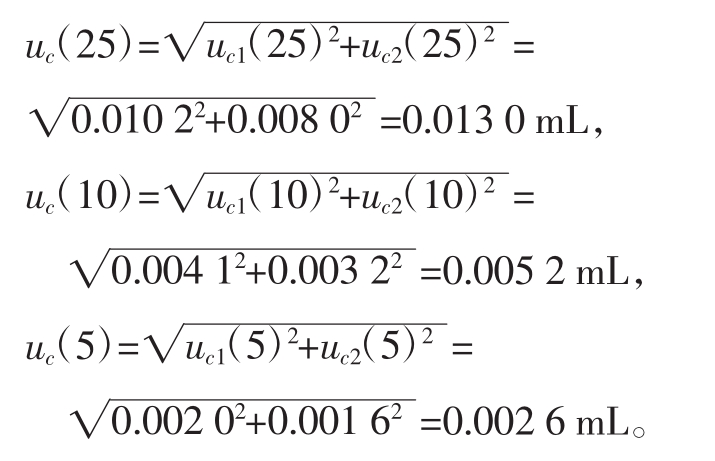
其相对不确定度为
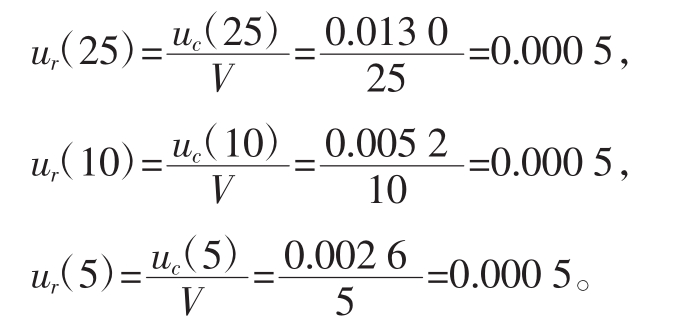
2.3 浓度c的不确定度评定
浓度c的不确定度由3个部分组成:一是由拟合标准工作曲线求得c时测量所产生的不确定度;二是标准储备液的纯度对c测量带来的不确定度;三是由标准储备液配制成不同浓度标准应用液所产生对c测量带来的不确定度;均按B类方法评定。
2.3.1 拟合标准工作曲线求得c时引入的不确定度分量
阿散酸、洛克沙砷、硝苯砷酸的线性范围、线性方程和相关系数见表1,阿散酸标准使用液的峰面积见表2,洛克沙砷标准使用液的峰面积见表3,硝苯砷酸标准使用液的峰面积见表4[3,5]。
表1 阿散酸、洛克沙砷、硝苯砷酸的线性范围、线性方程和相关系数
Table 1 Linear range,linear equation and correlation coefficient of p-arsanilic acid,4-nitrophenylarsonic acid,3-nitro-4-hydroxyphenylarsonic acid

名称线性范围/(μg/L)线性方程相关系数阿散酸 0~120 y=2 269.0x-843.7 0.999 7洛克沙砷 0~120 y=1 564.7x-2 560.5 0.999 2硝苯砷酸 0~120 y=1 461.4x-2 086.9 0.999 4
表2 阿散酸标准使用液的峰面积
Table 2 Peak areas of p-arsanilic acid standard working solution

注:yi′为标准使用液的峰面积。
阿散酸峰面积平行样品1 平行样品2 平行样品3 yi′20.0 43 326 44 169 43 975 44 536 40.0 90 115 89 947 89 933 89 916 60.0 135 284 137 740 134 008 135 296 80.0 182 639 189 637 187 750 180 676 100.0 224 607 223 691 219 785 226 056标准使用液的浓度/(μg/L)
表3 洛克沙砷标准使用液的峰面积
Table 3 Peak areas of 3-nitro-4-hydroxy-phenylarsonic acid standard working solution
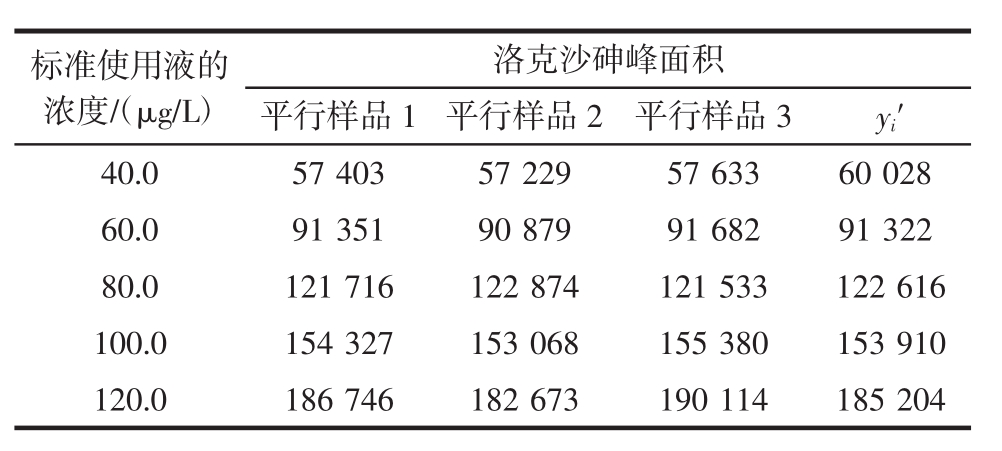
注:yi′为标准使用液的峰面积。
洛克沙砷峰面积平行样品1 平行样品2 平行样品3 yi′40.0 57 403 57 229 57 633 60 028 60.0 91 351 90 879 91 682 91 322 80.0 121 716 122 874 121 533 122 616 100.0 154 327 153 068 155 380 153 910 120.0 186 746 182 673 190 114 185 204标准使用液的浓度/(μg/L)
表4 硝苯砷酸标准使用液的峰面积
Table 4 Peak areas of 4-nitrophenylarsonic acid standard working solution
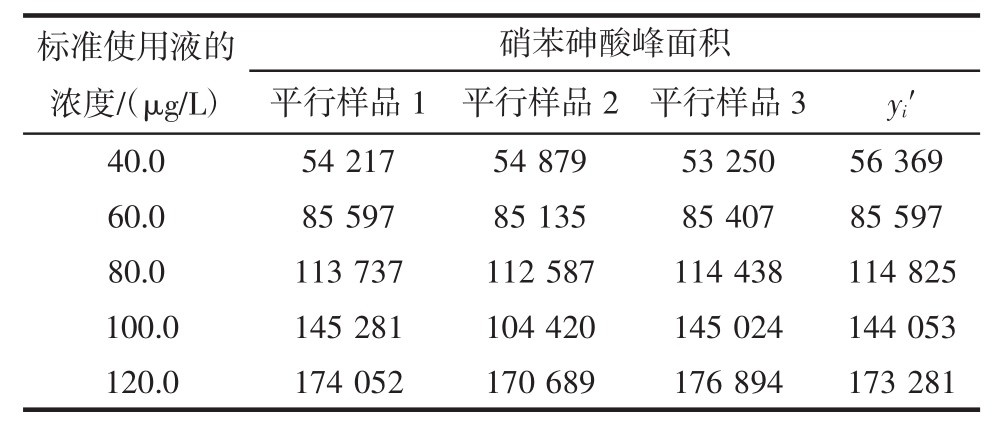
注:yi′为标准使用液的峰面积。
硝苯砷酸峰面积平行样品1 平行样品2 平行样品3 y i′4 0.0 5 4 2 1 7 5 4 8 7 9 5 3 2 5 0 5 6 3 6 9 6 0.0 8 5 5 9 7 8 5 1 3 5 8 5 4 0 7 8 5 5 9 7 8 0.0 1 1 3 7 3 7 1 1 2 5 8 7 1 1 4 4 3 8 1 1 4 8 2 5 1 0 0.0 1 4 5 2 8 1 1 0 4 4 2 0 1 4 5 0 2 4 1 4 4 0 5 3 1 2 0.0 1 7 4 0 5 2 1 7 0 6 8 9 1 7 6 8 9 4 1 7 3 2 8 1标准使用液的浓度/(μ g/L)
依据试验,对一份鸡肝加标样品进行3次重复测量,由峰面积通过线性回归方程求得c阿散酸=48.25 μg/L,c洛克沙砷=45.77 μg/L,c硝苯砷酸=46.20 μg/L 则残差标准偏差为:

2.3.2 标准储备液纯度引入的不确定度分量
计算标准储备液纯度引入的不确定度分量[6]。由标准物质证书获得阿散酸、洛克沙砷、硝苯砷酸标准物质的扩展不确定度分别为1 ng/mL(k=2),因此标准不确定度为:

2.3.3 混合标准储备液稀释操作的不确定度评定
进行混合标准储备液稀释操作引入的不确定度评定[5]。混合标准储备使用经检定或校准的移液枪和单标线A级容量瓶,进行二级稀释,配制成混合标准使用液。因此稀释倍数是![]()
根据计量检定证书,1 mL移液枪、A级50 mL容量瓶和10 mL容量瓶的允差分别为±0.01 mL、±0.05 mL和±0.03 mL[3],在(20±3)℃条件下进行,其相对不确定度 为![]()
![]()
![]()
则储备液稀释操作的相对不确定度为![]()
![]()
2.3.4 浓度c的相对标准不确定度
计算浓度c的相对标准不确定度[5-8]。
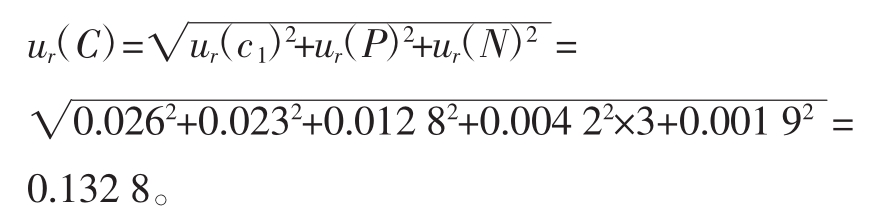
2.4 回收率的不确定度评定
进行回收率引入的不确定度评定[9-11]。分别在空白的鸡肝基质中添加0.50 mg/kg的混合标准液,包含n=6次平行试验,m=3×6=18,另取两份作为空白试验,均按照试验方法操作,并且进行外标法定量,结果见表5。
对测量结果求得相对标准偏差为
表5 回收试验结果(n=6)
Table 5 Results of test for recovery(n=6)

注:yi′为标准使用液的峰面积。
洛克沙砷 87.6 4.3硝苯砷酸 90.9 7.8目标物名称 回收率/% 相对标准偏差/% 平均相对标准偏差/%阿散酸 104.7 3.6 5.2
2.5 重复性的不确定度评定
进行重复性引入的不确定度评定[12-13]。对同一鸡肝样品进行n=11次独立重复性试验,所得阿散酸、洛克沙砷、硝苯砷酸的总量分别为0.849、0.863、0.852、0.875、0.888、0.869、0.862、0.850、0.883、0.869、0.858 mg/kg,平均值 =0.865 mg/kg,采用贝塞尔公式计算,标准不确定度等于一倍标准偏差
=0.865 mg/kg,采用贝塞尔公式计算,标准不确定度等于一倍标准偏差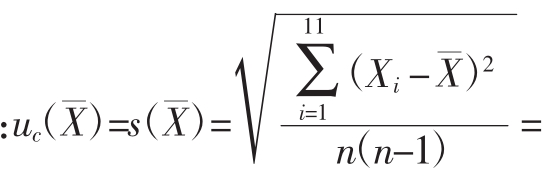
![]() ;其相对不确定度为
;其相对不确定度为![]()
![]()
2.6 合成标准不确定度的评定
总量 X 由下式计算出![]()
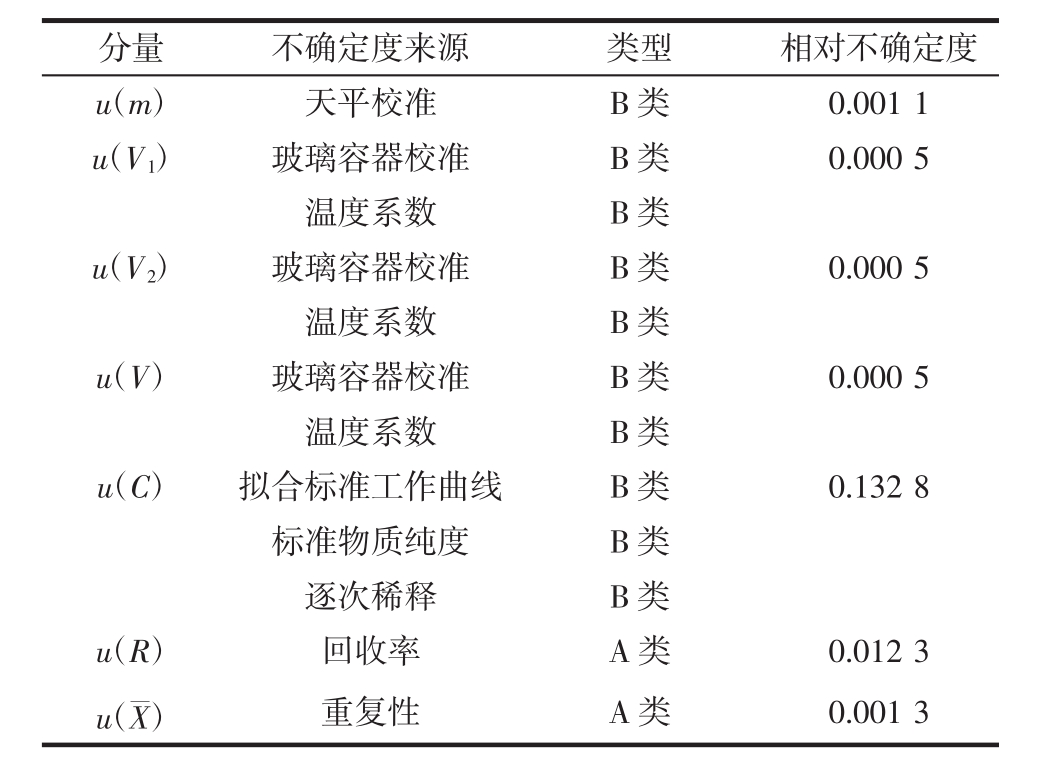
![]() 不确定度各分量的分析结果见表6。
不确定度各分量的分析结果见表6。
表6 不确定度各分量的分析结果
Table 6 Uncertainly in each quantity
?
分量 不确定度来源 类型 相对不确定度u(m) 天平校准 B类 0.001 1 u(V1) 玻璃容器校准 B类 0.000 5温度系数 B类u(V2) 玻璃容器校准 B类 0.000 5温度系数 B类u(V) 玻璃容器校准 B类 0.000 5温度系数 B类u(C) 拟合标准工作曲线 B类 0.132 8标准物质纯度 B类逐次稀释 B类u(R) 回收率 A类 0.012 3 u(X¯) 重复性 A类 0.001 3
由表6,其合成相对标准不确定度[14-15]为:![]()
![]() ,取包含因子k=2,鸡肝中阿散酸、洛克沙砷、硝苯砷酸含量的扩展不确定度:U(X)=k×ur(X)×X=2×0.133×0.865=0.230 mg/kg,该鸡肝中阿散酸、洛克沙砷、硝苯砷酸含量X为:0.865 mg/kg±0.230 mg/kg。
,取包含因子k=2,鸡肝中阿散酸、洛克沙砷、硝苯砷酸含量的扩展不确定度:U(X)=k×ur(X)×X=2×0.133×0.865=0.230 mg/kg,该鸡肝中阿散酸、洛克沙砷、硝苯砷酸含量X为:0.865 mg/kg±0.230 mg/kg。
3 结论
评定鸡肝中阿散酸、洛克沙砷、硝苯砷酸含量测量不确定度,分析测量过程中存在的不确定度来源。通过各不确定度分量的分析与比较得知,使用线性最小二乘法拟合曲线程序的前提是假定横坐标的量的不确定度与纵坐标的量的不确定度相差极大,因此浓度c的不确定度计算程序仅仅与峰面积不确定度有关,而标准储备液纯度和逐次稀释的不确定度足够小以至于可以忽略;另外,引起测量不确定度的最主要来源是测定c值时用最小二乘法拟合标准工作曲线所引入的不确定度。因此,试验人员在实际操作中应引起重视,严格按照高效液相色谱-原子荧光光谱联用仪操作规程进行操作,定期做好仪器的计量检定和期间核查工作,使仪器的技术性能处于良好状态是保证测定结果准确的重要手段,同时择优选择移液器具,从而保证该标准方法可靠,检测结果准确。
[1]韩永志.统计学在理化检验中的应用:第二讲不确定度及其评定[J].理化检验-化学分册,1999,35(10):477-478
[2]中华人民共和国国家质量监督检验检疫总局.测量不确定度评定与表示:JJF 1059.1—2012[S].北京:中国标准出版社,2013
[3]国家质量监督检验检疫总局.常用玻璃量器检定规程:JJG 196—2006[S].北京:中国计量出版社,2007
[4]中华人民共和国海关总署.出口动物源食品中阿散酸、硝苯砷酸、洛克沙砷残留量的检测方法:SN/T 2316—2019[S].北京:中国标准出版社,2019
[5]魏昊.化学分析中不确定度的评估指南[M].北京:中国计量出版社,2002:27-77
[6]赵娜娜,袁堃,周赛静,等.高效液相色谱-原子荧光光谱联用法测定鱼肉罐头中甲基汞的不确定度分析[J].安徽农业科学,2020,48(12):199-202
[7]林舒忆,贾彦博,胡文彬,等.液相色谱-原子荧光联用法测定灵芝孢子粉中甲基汞含量的不确定度评定[J].食品安全质量检测学报,2019,10(13):4352-4357
[8]方芳,陶兰芳.液相色谱—原子荧光联用法测定矿区废水中无机砷、烷基汞含量的不确定度评定[J].中国金属通报,2020(5):197-197,199
[9]毛永杨,杨桐,苏涛,等.高效液相色谱-原子荧光光谱联用法测定牛肝菌中无机汞、甲基汞、乙基汞的不确定度评估[J].食品科学,2017,38(24):272-277
[10]崔颖,倪松,张海滨,等.原子荧光光谱法测定海产品中锡的不确定度评定[J].食品研究与开发,2017,38(13):186-189
[11]曾云想,梁婷婷,汤明河,等.液相色谱-原子荧光光谱法测定水产品中汞形态的含量[J].理化检验-化学分册,2017,53(10):1226-1228
[12]吴雪梅,兰红军,黎少映,等.淡水鱼中无机砷的液相色谱-原子荧光光谱测定法[J].职业与健康,2019,35(12):1629-1632
[13]沈黎,陈晓园,路磊,等.液相色谱-原子荧光光谱联用检测小龙虾和鱼中不同形态砷的研究[J].绿色科技,2013(11):160-162
[14]苏美冬,杨锐,陈佳,等.液相色谱-原子荧光光谱法测定稻米中无机砷含量的不确定度评定[J].农产品加工,2019(18):43-45,48
[15]刘付英,邵志凌,李彩霞.液相色谱-原子荧光联用法测定粮食中无机砷含量的不确定度评定[J].粮油食品科技,2018,26(4):45-49