近年来,伴随高新分子学技术理论的更新、多功能纳米材料的介入、以及高灵敏度电化学等有效手段的开发,基于电信号传感体系的相关检测技术也获得了极大的发展。其原理是电化学生物传感器的换能元件(电极),将识别到的目标物质,在电极表面形成特异性杂交,将杂交信息转化为电流、电位、电导或电阻等特征检测信号输出,从而将信息转换成可测量信号[1]。电化学传感器具有仪器简便、成本低廉、操作简单、检测快速、灵敏度高和特异性好等特点,以其智能化、微型化、便携化的优点已发展为一种较为理想的快速检测体系[2-3]。
目前,在传统食源性有害微生物的检测过程中,普遍存在着操作过程繁琐,耗时较长,检测灵敏度不高,检测专一性不强,检测成本过高的缺陷。与此同时,电化学型生物传感器在检测食源性致病菌的过程中,以其高特异性和高精确度,实现了低成本高效实时检测有害微生物的目标。因此,电化学生物传感器已成为用来鉴定和定量检测食源性致病菌的一条有效途径,并在食品安全监管和疾病的预防控制等方面具有广泛的应用前景[4]。该文综述了近年来电化学生物传感器在检测食源性致病菌领域的最新研究进展并对其发展方向进行展望。
1 检测食源性致病菌及其毒素的电化学生物传感器的分类
电化学生物传感器是识别并转换生物分子信息信号为电信号的一种分析检测装置,主要由两部分组成:生物感受器和换能器。生物感受器识别生物分子,由具有分子识别功能的生物受体或识别靶分析物的生物识别元件构成,生物受体主要包括微生物、组织、细胞、细胞器、抗体抗原、酶、核酸等。生物受体接受对应生物响应,或识别元件识别靶分析物,通过换能器等转换元件将其转换为电信号,再通过信号放大元件将输入的信号转换为大的包含基本特征的可测量电信号,最后将扩增后的信号分析处理[5]。
检测食源性致病菌的电化学生物传感器以生物感受器或换能器不同类型下的各子类而分类[4-5]。按生物感受器的识别元件通常被分为四大类,主要包括抗原/抗体、酶、核酸和噬菌体;按换能器转换信号的类型可分为:光学、电化学、质量敏感型;其中光学传感器又可分为表面等离子共振(surface plasmon resonance,SPR)、光纤、拉曼光谱辅助类型[6];根据最终测量信号的不同可分为,电流型、电阻型、电导型和电位型。在实际应用中称为电流型电化学生物传感器、阻抗型电化学生物传感器、电导型电化学生物传感器、电势型电化学生物传感器[7]。
2 不同类型电化学生物传感器检测食源性致病菌及其毒素的进展
2.1 电流型生物传感器在检测食源性致病菌及其毒素中的应用
电流型电化学生物传感器也被称为安培型电化学生物传感器,是化学传感器最常采用的一种类型,它的检测原理是当工作电极的电位设定在一定值时,被测物在电极表面或其修饰层内氧化还原反应产生电流,从而可以通过生成的电流随时间的变化来定量分析生物电化学反应中的电活性物质[8]。近年来,电流型电化学生物传感器通过制备免疫复合物或与其他免疫分离技术相结合,缩短检测时间,降低检测限,与传统方法相比误差小,具有良好的可操作性。王泽华等[9]制备了电沉积纳米金修饰的16 通道电流型前列腺特异抗原(prostate specific antigen,PSA)免疫传感器,降低了成本,简化预处理过程,获得良好的特异性和重现性。
在食源性致病菌检测的应用中,郭燕等[10]为实现快速准确的检测致奶牛乳腺炎金黄色葡萄球菌(S.aureus),优化培养物中葡萄糖的制备条件,研制对目标菌具有严格选择性的培养基,适用于电流型葡萄糖传感器。基于其良好的抗干扰能力和稳定性,为基层奶牛场提供快速可靠的初步诊断。在检测黄曲霉毒素(aflatoxin B1,AFB1)的应用中,基于免疫分析方法将抗原与牛血清蛋白的结合物(bovine serum albuminaflatoxin B1,BSA-AFB1)或抗体固定在修饰电极表面,有时需要使用酶标记物碱性磷酸醋酶(alkaline phosphatase,ALP)和辣根过氧化物酶(horseradish peroxidase,HRP)[11]。在酶促反应中,常用ALP 标记二抗作为信号放大系统。待检的游离AFB1 与固定在电极表面的BSA-AFB1 竞争结合抗黄曲霉毒素(antibody-afla toxin B1,anti-AFB1)抗体,ALP 催化底液1-萘基磷酸盐产生的响应电流,电流随AFB1 浓度增大而减小。结果表明在实际操作中,大麦样品的背景信号要大于在AFB1 标准液中的信号,所以基质效应是实际样品检测中需要克服的问题。而釆取类似方法,使用多个电极或含有多个电极的多孔微板形成的传感器阵列分析在实际玉米样品中的检测性能,开展多样品同时在线测定,可以效率并节约成本[11]。与此同时,部分研究利用了黄曲霉毒素氧化还原酶(aflatoxin-oxidase,AFO)的催化氧化作用或黄曲霉毒素对乙酰胆碱酯酶(acetylcholinesterase,AChE)的活性抑制作用,但检测效果不理想,如果想进一步降低检测限,提高灵敏度,必须对测试液进行预浓缩处理[12]。
Chen 等[13]研制了一种新型的基于三维石墨烯(3D G)结构的金纳米颗粒修饰的电化学DNA 生物传感器。采用自行设计的生物捕获探针对异化亚硫酸盐还原酶(dissimilatory sulfite reductase,DsrAB)基因进行识别,可检测多种食源性致病菌。此类含有3D G 的金纳米粒子可参与食源性致病菌的富集识别探针的构建。该类型电化学生物传感器具有较大的比表面积,显著提高了检测体系的响应电流值,进而改善了检测有害微生物体系的灵敏度,见图1。
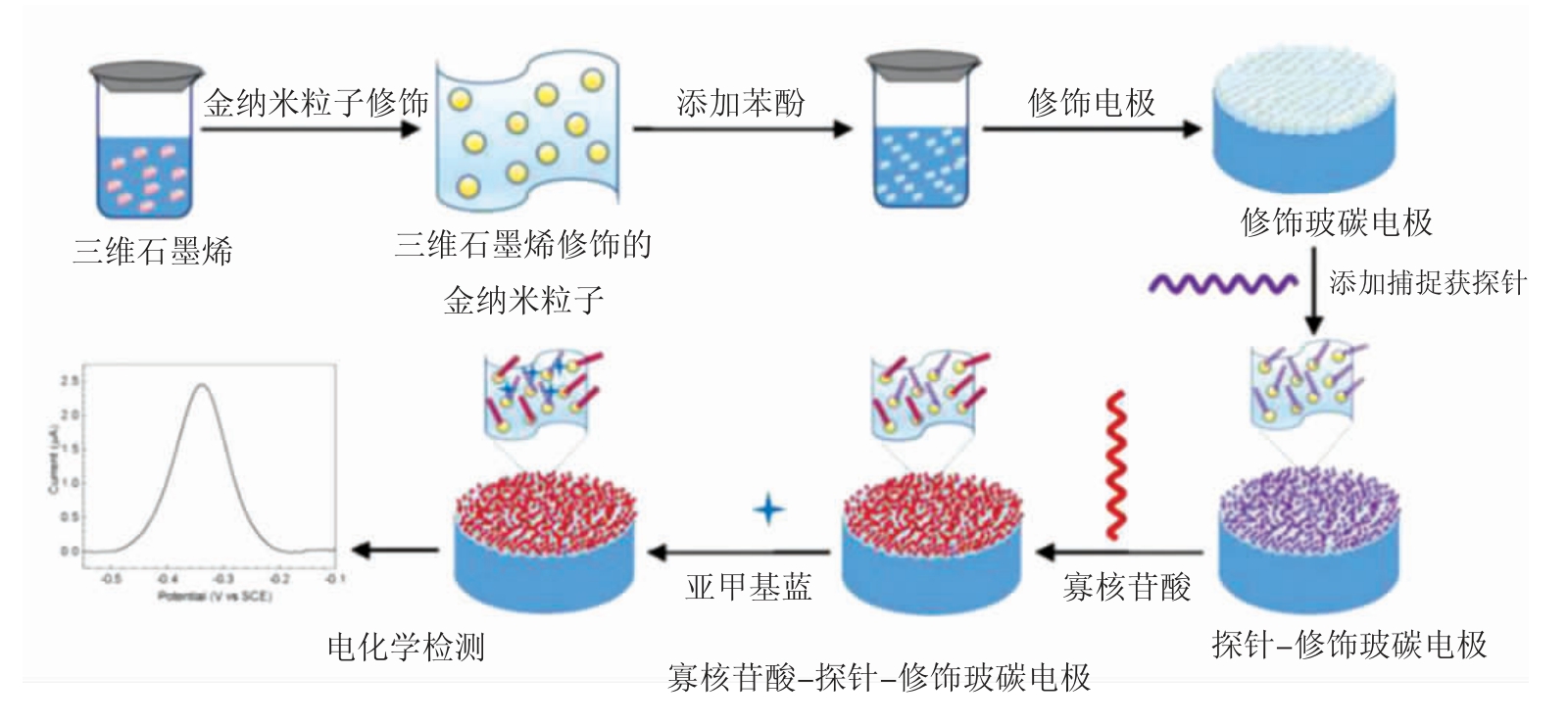
图1 寡核苷酸序列电化学生物传感器的制作原理
Fig.1 Fabrication principle of oligonucleotide sequence electrochemical biosensor
由图1可知,首先制备3D G 修饰的金米(3D GAuNPs),经超声处理后,在分散体上与苯酚充分混合;将制备的混合物涂于玻碳电极(glassy carbon electrode,GCE)。基于Au 键和静电相互作用,采用滴涂法将捕获探针(capture probe,CP),与3D G-AuNPs 进行免疫交联反应,构建修饰电极CP/3D G-AuNPs/GCE;靶标DNA 样品与亚甲基蓝(MB)相互作用并在CP/3D G-AuNPs/GCE 表面产生电流响应。在优化条件下,该传感器灵敏度高,检测限可达9.41×10-15 mol/L。
2.2 阻抗型生物传感器在检测食源性致病菌及其毒素中的应用
阻抗型电化学生物传感器主要是通过检测电极表面发生微生物繁殖代谢转化为电活性物质的生物识别反应引起电极表面阻值的变化来测量分析物。电化学阻抗谱(electrochemical impedance spectroscopy,EIS)是研究传感界面电特性并跟踪界面反应,研究电极系统以及测定固体电解质电导率的一种电化学测量方法,可以检测电极表面的电子传递阻抗,观察生物分子间相互作用的动力学,被广泛应用于电化学传感器的开发[14]。电化学阻抗是一种新的电化学检测技术,近年来开发了基于生物识别特异性来利用电化学阻抗来检测致病菌的方法。根据电极表面固定受体的不同可以将阻抗生物传感器分为四类,分别为免疫型、核酸型、噬菌体型和凝集素型[15-16]。
电化学阻抗技术应用于食源性致病菌的定量检测中一般不需要标记物。基于抗原-抗体的免疫反应导致电极表面阻抗值变化的原理,Zhou 等[17]使用电沉积法制备出一种修饰在金电极表面复合物膜,将anti-AFB1 抗体固定在微电极表面,可应用于病原菌(如大肠杆菌和沙门氏菌)的快速检测。而类似的检测方法也可采用溶胶凝胶法和离子液生物相容性膜固定抗体,可以增强电极表面的导电性,提高灵敏度。核酸生物传感器使核酸在高浓度合成过程中修饰官能团,固定在电极表面,应用于细菌检测[18]。Kara 等[19]基于此方法检测芽孢杆菌炭疽,灵敏度高。噬菌体生物传感器因噬菌体可溶解细菌,特异性强,应用于细菌的检测。Arghavan 等[20]用此方法检测大肠杆菌,大肠杆菌浓度为102 cfu/mL~108 cfu/mL 时测得的阻抗值随着细菌浓度的增大而减小,凝集素生物传感器以凝集素为生物受体与细菌表面的单糖或多糖结合以捕获细菌。Gamella 等[21]用阻抗免标记法检测大肠杆菌,线性范围为5.0×103 cfu/mL~5.0×107 cfu/mL。
Tokonami 等设计了一种具有代表性的基于T4 噬菌体的阻抗生物传感器用于大肠杆菌的检测[22]。结果表明,随着大肠杆菌浓度的增加,电荷转移抗性增强。既可以归因于噬菌体修饰的细菌被束缚在表面,也可以归因于大肠杆菌表面(带负电)和离子氧化还原探针之间的静电相互作用,此类型传感器构建原理见图2。从图2可知,首先将巯基乙胺组装在金电极上(A);其次,使用1,4-二硫氰酸酯作为介质进行交联(B);采用乙醇胺对T4 噬菌体进行固定化和阻断(C),捕获大肠杆菌细胞(D),基于阻抗/线性放大双重反应对大肠杆菌进行检测(E)。
Hoda 等研制了一种新型的用于病毒DNA 检测的电化学生物传感检测装置,利用EIS 对试验步骤进行了优化,确定了制备生物传感器的最佳条件[23]。利用自制的生物传感器和空白溶液的标准偏差,得到了4.7 nmol/L 的检出限,具体构建流程见图3。
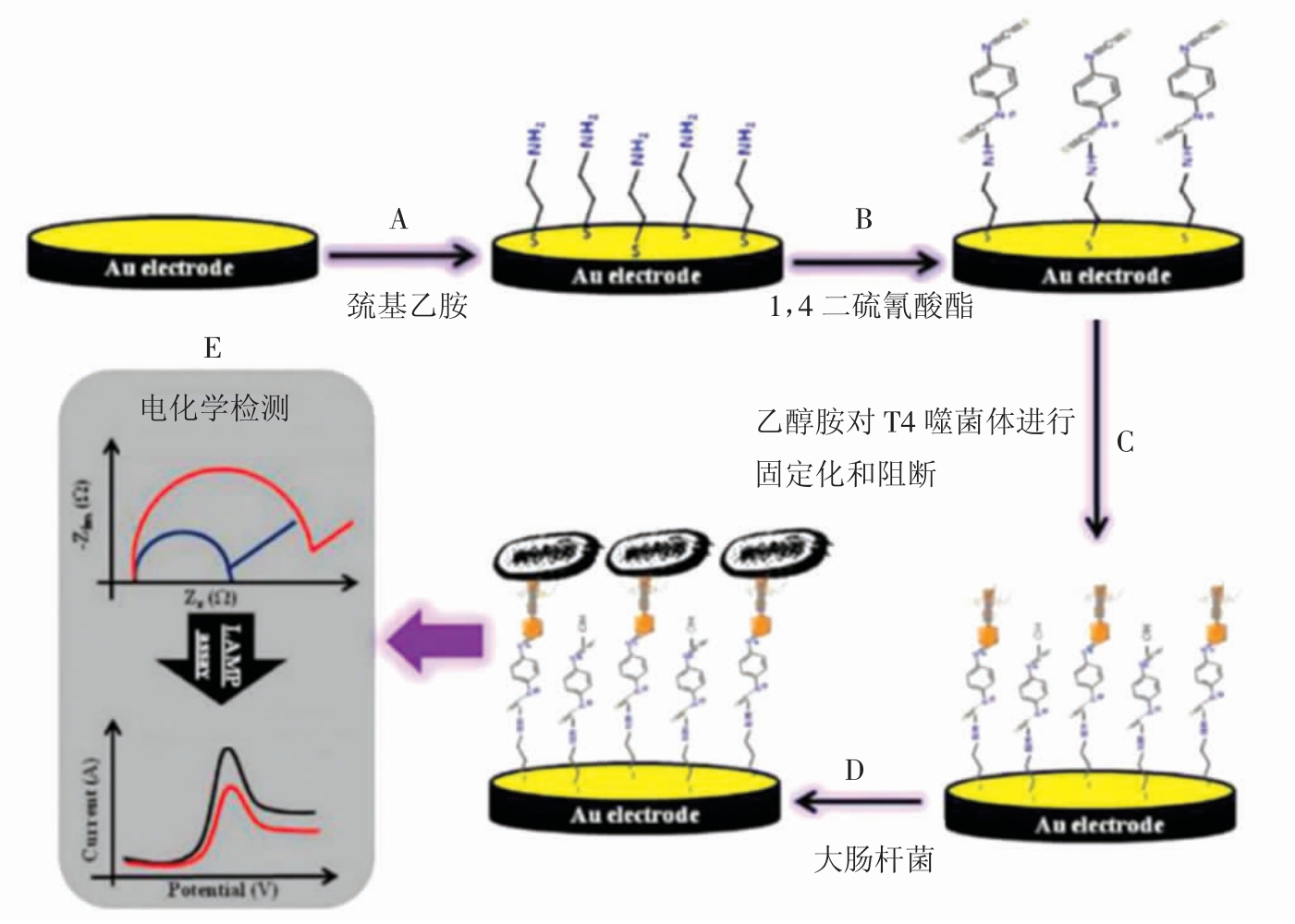
图2 基于T4 噬菌体的阻抗生物传感器构建原理
Fig.2 Construction principle of impedance biosensor based on T4 phage
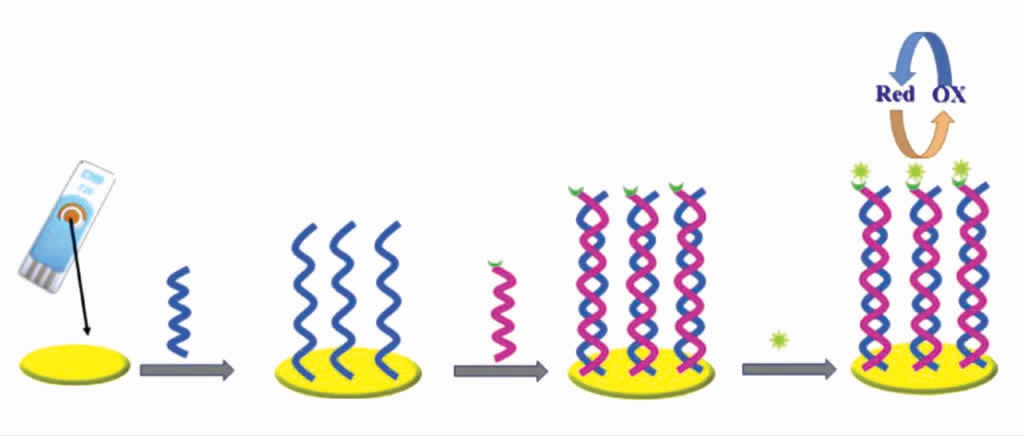
图3 电化学DNA 生物传感器的制备原理示意图
Fig.3 Schematic diagram of preparation principle of electrochemical DNA biosensor
如图3所示,将biao 序列固定在丝网印刷电极表面;再利用生物素化的靶链DNA 进行杂交,制备出DNA 传感器装置;采用双电位脉冲伏安法对链霉亲和素-碱性磷酸酶标记生物素化杂合物产生的阻抗进行电化学检测。
2.3 电导型生物传感器在检测食源性致病菌及其毒素中的应用
电导型电化学生物传感器通过在金属电极上施加交流电压来产生电流,无需参比电极,电极表面通常被涂覆选择性聚合物和相应的离子载体,选择性聚合物成膜沉积在金属电极上,离子载体的浓度和组成的改变会引起的电极间电导发生变化,通过电导参数的变化测定被测物的浓度。电导型传感器通过改变传感器组分来优化灵敏度,将电极作为换能器,测量膜的阻抗,阻抗值与膜接触的样品溶液中的离子浓度有关[24-25]。由此设计的传感器,通过阻抗测量,驱动电势低,具有微型化和大规模生产的优势。由于原理的相近和技术的共通点,电导型常被看作是阻抗型电化学生物传感器的一个分支,近年来在医学领域获得显著发展。针对食源性致病菌的检测,电导型生物传感器更注重电极表面修饰,降低氧化还原电势。Liu 等[26]将anti-AFB1 抗体固定在金微叉指电极表面,用辣根过氧化物酶封闭剩余的活性位点,测量AFB1 浓度,电极表面的抗原-抗体结合物影响了HRP 对底液的催化反应,电解质电导的变化与AFB1 浓度成反比。Solcktkin等[27]釆用差分模式,制备出一种基于金叉指薄膜电极和AChE 活性抑制的传感器,催化底物水解,溶液电导随电极薄膜上离子浓度的变化而变化。利用此体系检测黄曲霉毒素B1,检出限达到0.05 μg/mL。
2.4 电势型生物传感器在检测食源性致病菌及其毒素中的应用
电势型电化学传感器通过检测工作电极和参比电极之间电流为零时的电势变化与电化学反应中离子活性的关系来测量分析物的浓度,基于生物电识别分析,结合多电极接口阵列,可实现高通量检测。在实际应用中,通常与免疫分析方法相结合[28]。Rameil 等[29]开发了一种电位黄曲霉毒素M1 免疫传感器,该测定系统由多克隆anti-AFM1 抗体,Ag/AgCl 参比电极和HRP-AFB1 缀合物组成工作电极。利用3-(4-羟基苯基)-丙酸(p-hydroxybenzene propanoic acid,p-HPPA)作为辣根过氧化物酶的电子给体化合物(HRP),为标记HRP 的抗原提供电子,测试底液中含有的H2O2,电势的变化随AFM1 浓度增大而减小。基于该方法检测黄曲霉毒素M1,获得了良好的线性关系和检出限,其中检出限达到500 pg/mL。Larou 等[30]开发了一种基于生物电识别法(bioelectric recognition assay,BERA)的快速检测黄曲霉毒素M1 的生物传感器系统。通过将AFM1 同源抗体电植入非洲绿猴肾细胞的细胞膜上来实现,银丝工作电极和参考电极插入待测液中,AFM1与细胞膜中的抗体相互作用后使细胞膜电势发生改变。在极低浓度5 pg/mL 下,可以实现在3 min 内的快速检测。该检测系统使用多细胞电极接口阵列,允许高通量的AFM1 分析,每小时可完成160 次独立测试。
3 结论与展望
电化学生物传感器的电极系统组成、电极类型和电解液构成都关乎其灵敏度与特异性,在现有研究基础上构建新型复合生物传感器平台,拓宽电极修饰材料种类,是推动其广泛应用的发展方向,而细致应用分类也是需要完善的问题。电流型传感器发展最为成熟,但需要提高选择性和灵敏度,减少预处理过程,才能实现商业化。阻抗型电化学生物传感器虽然能比其他常规的电化学方法得到更多的电极界面结构的信息,但在检测低浓度微生物时成本较高,限制了其在实际中的应用。电导型和电势型传感器由于原理与其他两种较为相近,实际应用中不是很广泛。为了提高传感器的灵敏度和特异性,可以改善电极表面微结构,使用复合材料和纳米材料。为了实现超灵敏和高通量,就要完善抗体制备技术。另外,为了加快传感技术的发展,除了要融合生物医学等新技术,还要设计开发新型传感器,修饰电极、研发电路模型、研究多样转导机制,解决传感器寿命、不可重复、稳定性差等问题,实现智能化、便携化、商业化发展。在食品加工制造产业中,食源性致病菌和真菌毒素通常以非常低的浓度存在,难以检出,因此电化学传感器的发展可融合介质电泳、电通透等其他技术多元化发展,探求食源性病原菌及其毒素检测体系最优化,实现多重目标检测。电化学传感技术的发展将为各个领域提供一项快速响应、成本低廉、特异性强、灵敏度高的检测方法。
[1]董秀秀,王宇,沈玉栋,等.基于新型纳米材料的电化学免疫传感器及其在食品安全检测中的应用进展[J].中国食品学报,2015,15(4):136-146
[2]王延新,谢书宇,陈冬梅,等.电化学免疫传感器在食品安全检测中的研究进展[J].畜牧兽医学报,2018,49(7):1334-1342
[3]谢银侠.电化学功能核酸生物传感器在转基因食品检测中的发展现状[J].食品安全导刊,2018(10):25-27
[4]储嫣红,邹彬,陈学珊,等.酶电极传感器在食品安全检测中的研究进展[J].食品工业科技,2017,38(17):335-340
[5]Hélder da Silva,João G Pacheco,Júlia McS Magalhães,et al.MIPgraphene-modified glassy carbon electrode for the determination of trimethoprim[J].Biosensors and Bioelectronics,2014,52:56-61
[6]董世彪,赵荣涛,李杨,等.DNA 电化学生物传感器检测病原微生物的应用研究进展[J].军事医学,2015,39(6):480-483
[7]Mead MI,Popoola OAM,Stewart GB,et al.The use of electrochemical sensors for monitoring urban air quality in low-cost, high-density networks[J].Atmospheric Environment,2013,70:186-203
[8]张金玲,杜祎,高广恒,等.酶电极法测定玉米中黄曲霉毒素B1含量[J].山东科学,2018,31(1):60-64
[9]王泽华,曾冬冬,张欢,等.电沉积纳米金修饰的16 通道电流型PSA 免疫传感器的制备[J].中国生物医学工程学报,2015,34(1):55-61
[10]郭燕,窦文超,赵广英.便携式电流型葡萄糖传感器快速检测致奶牛乳腺炎金黄色葡萄球菌的研究[J].中国预防兽医学报,2015,37(10):780-785
[11]马海华,张元,甄彤,等.电化学生物传感器在黄曲霉毒素检测中的研究进展[J].中国粮油学报,2016,31(2):132-140
[12]Larou E, Yiakoumettis I, Kaltsas G, et al. High throughput cellular biosensor for the ultra-sensitive,ultra-rapid de-tection of aflatoxin M1[J].Food Control,2013,29(1):208-212
[13]Shiqiang Chen, Y Frank Cheng, Gerrit Voordouw. Three-dimen-sional graphene nanosheet doped with gold nanoparticles as electrochemical DNA biosensor for bacterial detection[J]. Sensors & Actuators:B.Chemical,2018,262:860-868
[14]朱丹,李强强,逄秀梅,等.阻抗光谱在电化学生物传感器中的应用[J].化学传感器,2016,36(1):42-47
[15]张爱萍,唐佳妮,孟瑞锋,等.电化学法快速检测微生物的发展现状及趋势[J].生物技术进展,2011,1(5):342-346
[16]Marta Sánchez-Paniagua López,Beatriz López-Ruiz.Electrochemical biosensor based on ionic liquid polymeric microparticles. An analytical platform for catechol[J].Microchemical Journal,2018,138:173-179
[17]Materon EM, Huang JPJ, Wong A, et al. Glutathione-s-transferase modified electrodes for detecting anticancer drugs[J]. Biosensors and Bioelectronics,2014,58:232-236
[18]Wu D,Guo AP,Guo ZK,et al.Simultaneous electrochemical detection of cervical cancer markers using reduced graphene oxide-tetraethylene pentamine as electrode materials and distinguishable redox probes as labels[J]. Biosensors and Bioelectronics,2014,54:634-639
[19]Kara P, Meric B, Ozsoz M. Application of Impedimetric and Voltammetric Genosensor for Detection of a Biological Warfare:Anthrax[J].Electroanalysis,2010,20(24):2629-2634
[20]Shabani A, Zourob M, Allain B, et al. Bacteriophage-modified microarrays for the direct impedimetric detection of bacteria[J]. Analytical Chemistry,2008,80(24):9475-9482
[21]Gamella M,Campuzano S,Parrado C,et al.Microorganisms recognition and quantification by lectin adsorptive affinity impedance[J].Talanta,2009,78(4):1303-1309
[22]Umer Farooq,Qiaoli Yang,Muhammad Wajid Ullah,et al.Bacterial biosensing: Recent advances in phage-based bioassays and biosensors[J].Biosensors and Bioelectronics,2018,118:204-216
[23]Hoda Ilkhani,Siamak Farhad.A novel electrochemical DNA biosensor for Ebola virus detection[J]. Analytical Biochemistry,2018,557:151-155
[24]C Day,S Søpstad,H Ma,et al.Impedance-based sensor for potassium ions[J].Analytica Chimica Acta,2018,1034(30):39-45
[25]E Fazio, S G Leonardi, M Santoro, et al. Synthesis, characterization and hydrogen sensing properties of nanosized colloidal rhodium oxides prepared by Pulsed Laser Ablation in water[J]. Sensors & Actuators:B.Chemical,2018,262:79-85
[26]Jia XL, Liu ZM, Liu N, et al. A label-free immunosensor based on graphene nanocomposites for simultaneous multiplexed electro-chemical determination of tumor markers[J]. Biosensors and Bioelectronics,2014,53:160-166
[27]O O Soldatkin, O S Burdak, T A Sergeyeva, et al. Acetyl-cholinesterase-based conductometric biosensor for determination of aflatoxin B1[J].Sensors & Actuators:B.Chemical,2013,188:999-1003
[28]周从燕,李丽蓉,刘入源.纳米基电分析生物传感器在食品兽药残留检测中的研究与应用进展[J].食品安全质量检测学报,2017,8(1):150-155
[29]Steffen Rameil, Peter Schubert, Peter Grundmann, et al. Use of 3-(4-hydroxyphenyl) propionic acid as electron donating com-pound in a potentiometric aflatoxin M1-immunosensor[J].Analytica Chimica Acta,2009,661(1):122-127
[30]Evangelia Larou,Iakovos Yiakoumettis,Grigoris Kaltsas,et al.High throughput cellular biosensor for the ultra-sensitive, ultra-rapid detection of aflatoxin M1[J].Food Control,2013,29(1):208-212