近年来随着人民生活水平的提高和生活方式的改变,对酒类的消费也日益增多,过量饮酒已经成为全世界范围内极受关注的社会公共问题。一次大量饮酒会引发急性酒精中毒,对机体健康产生严重危害,例如致心脑血管疾病、神经系统疾病、消化不良、代谢紊乱及营养失调等[1-2]。随着急性酒精中毒发病率逐年增高,开发有效的解酒药物、缓解酒精中毒症状也显得愈发必要。桧木纯露为桧木植物蒸馏精油后所得的冷凝水溶液,含有黄酮类、萜烯类、槲皮素、鞣质等多种成分,具有良好的抗氧化、清除自由基、抗炎等活性,人们在生活上已试用于解酒去宿醉、提神醒脑,发现有较好的疗效[3-5]。本项目通过小鼠防醉及醒酒实验,考察桧木纯露的解酒作用;通过构建小鼠酒精性肝损伤模型,观察桧木纯露的预防保护作用,并初步探讨其作用机制。为进一步深入研究桧木产品的药用及保健价值提供科学依据。
1 材料与方法
1.1 材料与试剂
桧木纯露:四川桧元素生物有限公司;海王金樽:深圳市海王健康科技发展有限公司,将海王金樽研磨后配成1g/mL 的混悬液备用;56 度二锅头白酒:北京红星股份有限公司;天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、丙二醛(malondialdehyde,MDA)、超氧化物歧化酶(superoxide dismutase,SOD)试剂盒:南京建成生物工程研究所。
清洁级昆明种小鼠:雄性,体重(20±2)g,购自成都达硕实验动物中心,动物合格证号:SCXK(川)2008-24。饲养环境温度为(23±2)℃,湿度为40%~60%,明暗交替周期为12 h。
1.2 仪器与设备
低温高速离心机(H1650R):湘仪离心机仪器有限公司;高速离心机(L530):长沙湘仪离心机仪器公司;7200 型可见分光光度计:上海龙尼柯仪器有限公司;恒温水浴箱(HHSYZL-Ni):北京长风仪器公司;微量加样器:Eppendorf 公司;玻璃匀浆管:上海垒固仪器有限公司。
1.3 方法
1.3.1 防醉实验
取雄性小鼠50只,适应性喂养3 d 后随机分为模型组、海王金樽阳性对照组(0.15 mL/10 g)、桧木纯露高、中、低剂量组(0.2 mL/10 g、0.15 mL/10 g、0.1 mL/10 g)。禁食不禁水12 h 后,各给药组给予相应药物预防,模型组灌以生理盐水(0.15 mL/10 g)。给药30 min 后,各组小鼠灌胃给予56 度红星二锅头(0.15 mL/10 g),观察小鼠醉酒潜伏期(从灌酒到翻正反射消失的时间)、醒酒时间(从灌酒到翻正反射恢复时间)。
1.3.2 醒酒实验
动物分组同1.3.1。各组小鼠灌胃给予56 度红星二锅头0.15 mL/10 g,5 min 后,除模型组给予生理盐水,其余组小鼠分别灌胃给予相应药物治疗。记录小鼠醉酒潜伏期及醒酒时间。
1.3.3 对酒精性肝损伤的保护作用
取雄性小鼠60 只,适应性喂养3 d 后随机分为空白组、模型组、海王金樽阳性对照组(0.15 mL/10 g)、桧木纯露高、中、低剂量组(0.2 mL/10 g、0.15 mL/10 g、0.1 mL/10 g)。每日空白组与模型组给予等体积的生理盐水,各给药组每日灌胃相应剂量药物进行保护,30 min 后除空白组外,其余各组以0.15 mL/10 g 灌胃56 度红星二锅头,持续14 d。
最后一天灌胃结束30 min 后,小鼠眼球取血处死,分离血清,解剖取肝脏,用预冷的生理盐水漂洗后称重,计算脏器系数。
1.3.4 血清中AST、ALT 的测定
AST 及ALT 的测定方法参照试剂盒说明书。将5 μL 待测样本加入基质液中,再依次与2.4-二硝基苯肼、0.4 mmol/L 氢氧化钠溶液反应,后在510 nm 波长下测定各复孔A 值。通过标准曲线法求得各样本相应的AST、ALT 活力单位。
1.3.5 肝脏中氧化/抗氧化相关指标的测定
肝脏组织中SOD 的测定采用水溶性四唑盐法,参照试剂盒说明书操作后于450 nm 处测定各复孔A 值。MDA 的测定使用硫代巴比妥酸法,参照试剂盒说明书操作后于532 nm 处测定各复孔A 值。
式中:A0 为未添加样品的对照组吸光度值;A1 为添加样品的实验组吸光度值。
1.3.6 数据处理方法
数据均采用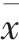 ±s 表示,并采用SPSS19.0 软件进行统计分析,组间比较采用t 检验。
±s 表示,并采用SPSS19.0 软件进行统计分析,组间比较采用t 检验。
2 结果与分析
2.1 防醉实验
实验小鼠防醉实验结果见表1。
表1 小鼠防醉实验结果(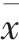 ±s,n=10)
±s,n=10)
Table 1 Results of experiment on preventing drunkenness in mice(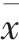 ±s,n=10)
±s,n=10)

注:与模型组比较,*P<0.05,**P<0.01。
组别 醉酒潜伏期/min 醒酒时间/min模型组 3.45±1.65 292.73±39.28阳性药组 8.69±2.31** 261.94±47.90**桧木纯露高剂量组 7.29±2.73** 254.35±50.66**桧木纯露中剂量组 6.57±1.44** 263.28±41.27*桧木纯露低剂量组 4.12±1.92* 279.01±37.41*
由表1可见,与模型组小鼠比较,灌胃白酒前给予不同剂量的桧木纯露和阳性药的小鼠醉酒潜伏期延长(P<0.01 或P<0.05),醒酒时间缩短(P<0.01 或P<0.05)。
2.2 解酒实验
实验小鼠解酒实验结果见表2。
由表2可见,与模型组比较,灌白酒后再灌胃给予不同剂量的桧木纯露和阳性药的小鼠醉酒潜伏期延长(P<0.01 或P<0.05),醒酒时间显著缩短(P<0.01)。
2.3 对酒精性肝损伤的保护作用
2.3.1 对肝脏系数的影响
对酒精性肝损伤小鼠肝脏系数影响结果见表3。
表2 实验小鼠解酒实验结果(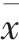 ±s,n=10)
±s,n=10)
Table 2 Results of experiment on relieving alcoholism in mice(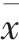 ±s,n=10)
±s,n=10)

注:与模型组比较,*P<0.05,**P<0.01。
组别 醉酒潜伏期/min 醒酒时间/min模型组 3.12±1.30 276.6±44.86阳性药组 5.67±0.91** 237±65.28**桧木纯露高剂量组 6.11±1.67** 242.4±48.60**桧木纯露中剂量组 5.33±1.42* 249±37.08**桧木纯露低剂量组 6.02±1.22** 252±54.62**
表3 对酒精性肝损伤小鼠肝脏系数的影响(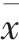 ±s)
±s)
Table 3 Effect on liver index in mice induced by ethanol(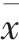 ±s)
±s)

注:与空白组比较,##P<0.01;与模型组比较,*P<0.05,**P<0.01。
组别 n 肝脏系数空白组 10 4.35±1.02模型组 8 6.80±0.81##阳性药组 10 4.57±0.36**桧木纯露高剂量组 10 4.67±0.61**桧木纯露中剂量组 10 4.89±0.97*桧木纯露低剂量组 9 5.06±0.56*
由表3可见,模型组中酒精性肝损伤小鼠的肝脏系数较空白组小鼠显著升高(P<0.01),给予桧木纯露和阳性药保护的小鼠肝脏系数较模型组降低(P<0.01或P<0.05)。
2.3.2 对血清AST 和ALT 的影响
对小鼠血清中AST 和ALT 活性影响结果见表4。
表4 对小鼠血清中AST 和ALT 活性的影响(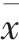 ±s)
±s)
Table 4 Effects on levels of AST and ALT in serum in mice(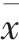 ±s)
±s)

注:与空白组比较,##P<0.01;与模型组比较,*P<0.05,**P<0.01。
?
由表4可见,给药14 d 后,与空白组比较,模型组小鼠血清AST 和ALT 活性显著升高(P<0.01);与模型组比较,阳性药组和桧木纯露高、中剂量组显著降低(P<0.01 或P<0.05),但桧木纯露低剂量组AST 和ALT活性无显著性差异。
2.3.3 对肝脏SOD 活性和MDA 含量的影响
对小鼠肝脏SOD 活性和MDA 含量影响结果见表5。
由表5可见,与空白组比较,模型组小鼠肝脏内SOD 活性显著降低(P<0.01),MDA 的水平显著升高(P<0.01);与模型组比较,阳性药组与桧木纯露各剂量组SOD 的活性升高(P<0.01 或P<0.05)。MDA 水平显著降低(P<0.01)。
表5 对小鼠肝脏SOD 活性和MDA 含量的影响(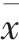 ±s)
±s)
Table 5 Effects on levels of SOD and MDA in liver in mice(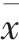 ±s)
±s)

注:与空白组比较,##P<0.01;与模型组比较,*P<0.05,**P<0.01。
组别 n SOD/(U/mgprot) MDA/(mmol/gprot)空白组 10 166.34±30.56 0.51±0.12模型组 8 109.11±31.24## 1.96±0.57##阳性药组 10 143.29±25.70** 1.04±0.31**桧木纯露高剂量组 10 150.62±20.16** 1.23±0.46**桧木纯露中剂量组 10 134.48±32.02** 1.19±0.25**桧木纯露低剂量组 9 121.65±38.69* 1.30±0.44**
3 结论与讨论
近些年来,因为人们生活水平的增高,人均饮酒量的上升造成酒精性肝病的发病率也逐年上升,成为仅次于病毒性肝炎的第二大肝病[6]。一次大量饮酒会引发急性酒精中毒,严重影响身体健康,危害社会安定。急性酒精中毒可对机体产生严重损害,例如致心脑血管疾病、神经系统疾病、消化不良、代谢紊乱及营养失调等疾病。随着急性酒精中毒发病率逐年增高,对其进行防治也显得愈发重要。
乙醇进入机体后约90%~95%在肝脏内被氧化代谢,加快乙醇在体内代谢的机理包括加快肝脏中乙醇的氧化代谢、增强清除自由基的能力等。ALT 主要存在于肝细胞浆内,当肝细胞损伤时,细胞内转氨酶可进入血中,引起血ALT 升高。AST 也存在于肝细胞浆内,AST 并分布于线粒体内,当肝细胞损害严重时,线粒体内AST 释放入血,因此转氨酶是肝细胞损害的敏感标志,也是乙醇所致肝损伤较敏感且常见的指标[7]。酒精摄入过多会导致肝组织的抗氧化物质消耗增加,SOD 水平下降。MDA 是脂质过氧化反应的终产物,能反映组织中自由基的含量和自由基引发的脂质过氧化程度[8]。
桧木是裸子植物中扁柏属的一种植物,桧木纯露为桧木植物蒸馏所得的冷凝水溶液。桧木纯露中除了含有少量精油成分之外,还含有全部植物体内的水溶性物质。拥有百分之百植物水溶性物质的纯露,其所含矿物养分(如单宁酸及类黄酮)是精油所缺乏的,其低浓度的特性容易被皮肤所吸收,完全无香精及酒精成份,温和不刺激。有研究表明,桧木纯露具有很好的抗氧化效果,对羟基自由基(·OH)具有一定的清除作用,对超氧自由基具有明显的抑制作用,可发挥抗炎、护肝等作用,桧木其叶子的主要化学成分是挥发油、黄酮类、鞣质等[9-11],而萜类和黄酮类化合物对ConA 致小鼠免疫性肝损伤均具有一定的保肝作用[12]。
实验结果表明,在防醉实验和解酒实验中,桧木纯露均可延长小鼠的醉酒潜伏期,且缩短醒酒时间(P<0.01 或P<0.05)。在酒精性肝损伤实验中,桧木纯露能缓解酒精对小鼠肝脏系数的影响(P<0.01 或P<0.05),降低血清中ALT、AST 水平(P<0.01 或P<0.05)及肝脏内MDA 含量(P<0.01),升高SOD 活性(P<0.01或P<0.05),有效缓解酒精对肝脏的损伤,增强抗氧化能力,减轻过氧化损伤,为桧木作为具有抗氧化能力、护肝作用的保健食品提供了一定的理论研究依据。
桧木纯露具有显著的防醉解酒作用,可增强酒精中毒小鼠的抗氧化能力,对小鼠酒精性肝损伤具有一定的保护作用。桧木纯露有望进一步开发成为解酒护肝的保健食品,其有效成分和作用机制还需更深入的研究。
[1]梁娜,秦清娟,邹勇,等.魔芋葡甘聚糖对小鼠的防醉解酒作用[J].食品工业科技, 2015,36(14):366-369
[2]张志毕,张媛,于浩飞,等.余甘子提取物对小鼠急性酒精肝损伤的保护作用研究[J].食品工业科技,2017,38(5):350-356
[3]陈兴芬,单承莺,马世宏,等.侧柏叶化学成分、生理活性及防脱发功能研究进展[J].中国野生植物资源,2010,29(3):1-5
[4]赵永光,常立新,周永国,等.超声波法提取侧柏叶片中黄酮类化合物的研究[J].河北农业大学学报,2005,28(2):54-56
[5]刘廷礼,邱琴,赵怡,等.侧柏叶挥发油成分的GC-MS 分析[J].中药材,2000,23(8):460-461
[6]黄立峰,朱乾坤.金线莲提取物对小鼠急性酒精性肝损伤的保护作用[J].福州总医院学报,2005(z1):279-280
[7]袁军清,蔡明来.柴芦疏肝解毒胶囊对动物实验性肝损伤的保护作用[J].中国医药指南, 2011,9(24):42-43
[8]李丹, 郭春林, 王春艳.郁芝胶囊对大鼠酒精性脂肪肝的治疗作用[J].中国老年学,2012,32(6):1200-1202
[9]陈兴芬,单承莺,马世宏,等.侧柏叶化学成分、生理活性及防脱发功能研究进展[J].中国野生植物资源,2010,29(3):1-5
[10]赵永光,常立新,周永国,等.超声波法提取侧柏叶片中黄酮类化合物的研究[J].河北农业大学学报,2005,28(2):54-56
[11]刘廷礼,邱琴,赵怡,等.侧柏叶挥发油成分的GC-MS 分析[J].中药材,2000,23(8):460-461
[12]李国栋,陈园园,王盼,等.野菊花中萜类和黄酮类化合物保肝作用研究[J].中草药,2013(24):3510-3514