糖尿病的治疗药物现在主要是胰岛素和口服降糖药,但还是有许多轻重不一的不良反应[1]。与之相比,改善饮食习惯,采用膳食调节则具有安全、廉价和方便等优势。据报道,目前已有数百种植物源可以用做降糖改善剂[2],降糖活性物质包括多糖、肽类、黄酮类、萜类、生物碱、酚类等[3]。秋葵(Abelmoschus esculentus),也称羊角豆,为锦葵科一年生的草本植物[4],蕴含多种生物活性物质[5-7],例如多糖等黏性物质[8]、多酚[9]、黄酮类物质[10]。刘雪蕊等报道秋葵多糖对α-葡萄糖苷酶的有较强的抑制作用,可以让糖尿病小鼠的血糖值明显降低[11]。冯冠英等[12]报道黄秋葵水提液能够降低糖尿病小鼠的血糖(P<0.01),并呈一定剂量依赖性,它的作用机制可能是因为秋葵中所含的甾醇类成分抑制α-葡萄糖苷酶的活性。
目前,秋葵的主要食用方法是鲜食,但在室温下仅能贮藏2 d~3 d,非常不耐贮藏。目前,已有将秋葵的粉剂原料加入到营养片中的研究报道[13],改变了传统鲜秋葵作为烹饪原料的消费模式,提高了秋葵的利用率。但是,关于秋葵微粉改善血糖作用的研究报道较少。因此,本试验采用前期试验制备的川秋葵微粉作为研究对象,通过测定川秋葵微粉对α-葡萄糖苷酶的抑制作用,对葡萄糖透析延迟指数以及对葡萄糖的吸附能力来考察川秋葵微粉的体外降血糖活性;其次,通过人体试验对其血糖生成指数(glycemic index,GI)值与血糖负荷(glycemic load,GL)值进行测定,旨在证实与探讨秋葵微粉具有改善血糖的作用,为其在食品添加剂、医疗、保健用品等的开发利用上提供依据。
1 材料与方法
1.1 材料与仪器
川秋葵1 号:四川省植物工程研究院;阿卡波糖(纯度≥98.0 %)、对硝基苯基-β-D-吡喃半乳糖苷(p-nitrophenyl-β-D-galactopyranoside,PNPG)(纯度≥99.0%)、酵母源α-葡萄糖苷酶(10 000 U/mL):Sigma公司;高温α-淀粉酶(20 000 U/g):上海源叶生物科技有限公司;其他化学试剂均为国产分析纯。
HHS-8S 电子恒温不锈钢水浴锅:上海光地仪器设备有限公司;UV Power 紫外可见分光光度计:北京莱伯泰科仪器有限公司;MK-3 酶标仪:美国Thermo公司;H2050R 台式高速冷冻离心机:长沙湘仪离心机有限公司;QYC-2102C 恒温振荡培养箱:上海福玛实验设备有限公司;HX-200 型高速中药粉碎机:浙江省永康市溪岸五金药具厂;XDW-2C 小型低温超微粉碎机:济南达微机械有限公司;FX101-3 型电热鼓风干燥箱:上海树立仪器仪表有限公司;VGM01 可孚电子血糖仪:杭州微策生物技术有限公司。
1.2 试验方法
1.2.1 川秋葵微粉准备
鲜川秋葵→预处理→护色处理→热风干燥→粗粉碎→微粉碎→过筛→成品→干燥密闭保存备用
果荚长度:7.0 cm 左右。预处理:选择无腐烂、无病虫害的新鲜川秋葵,清洗、沥干、去蒂,横切成0.5 cm左右的小段。护色处理:采用90 ℃沸水对新鲜秋葵烫漂30 s。干燥时间为7.4 h,干燥温度为51.0 ℃。微粉粒度:150.0 目。
1.2.2 川秋葵微粉基本成分的测定[11]
粗蛋白质含量参照GB 5009.5-2016《食品安全国家标准 食品中蛋白质的测定》;粗灰分含量参考GB 5009.4-2016《食品安全国家标准食品中灰分的测定》;粗脂肪含量参照GB 5009.6-2016《食品安全国家标准食品中脂肪的测定》;水分含量参照GB 5009.3-2016《食品安全国家标准食品中水分的测定》;碳水化合物含量采用GB/Z 21922-2008《食品营养成分基本术语》中规定的碳水化合物为食品总质量100-水分-灰分-脂肪-蛋白质-膳食纤维;膳食纤维含量参考GB 5009.88-2014《食品安全国家标准食品中膳食纤维的测定》;果胶含量参考李加兴等[14]的方法执行;VC 含量采用南京建成生物工程研究所试剂盒测试测定;总黄酮含量、总酚含量的测定参考李孟秋等[15]的方法。
1.2.3 川秋葵微粉体外降血糖活性研究
川秋葵微粉对α-葡萄糖苷酶的抑制作用参照刘雪蕊[11]的方法执行。α-淀粉酶活力抑制的测定参照Chau C F 等[16]和梅新等[17]的方法。葡萄糖吸附能力的测定参照Cheickna Daou 等[18]的方法。葡萄糖透析延迟指数(glucose dialysis retardation index,GDRI)的测定采用蒽酮比色法[19-21]。
1.2.4 川秋葵微粉体内降血糖活性研究
1.2.4.1 受试对象
根据体质量指数(body massindex,BMI)为18.5kg/m2~23.9 kg/m2,选取20 例志愿者(男8 例,女12 例,年龄18 岁~20 岁),均为在校大学生,身体健康,无碳水化合物不耐受症,无任何代谢性疾病,无糖尿病家族史和其他代谢病史。经四川旅游学院伦理审核批准,志愿者均签署知情同意书。
1.2.4.2 口服葡萄糖耐量试验
口服葡萄糖耐量试验于清晨进行,志愿者要求禁食10 h,采志愿者指尖血,使用可孚电子血糖仪,测其空腹血糖值。志愿者口服葡萄糖溶液(50 g 葡萄糖溶于200 mL 温水中),分别于服后15、30、45、60、90 min 和120 min 测血糖值。
1.2.4.3 食物血糖应答试验
口服葡萄糖耐量试验合格者进行受试食物血糖应答试验。试验当天清晨,测定其空腹血糖值后,进食受试食物(含有50 g 碳水化合物),并分别于进食后15、30、45、60、90 min 和120 min 测血糖值。
1.2.4.4 GI 和GL 计算
秋葵微粉的GI 值的计算采用Wolever 计算公式[22-23],GL 值的计算按照Salmeron 公式[24]。
1.3 数据处理
试验数据经3 次平行试验后得到,试验数据以均数±标准差( ±SD)表示,组间比较采用单因素方差分析,P <0.05 表示有显著性差异。统计分析使用Excel 2013、SPSS16.0、Origin8.1 等软件。
±SD)表示,组间比较采用单因素方差分析,P <0.05 表示有显著性差异。统计分析使用Excel 2013、SPSS16.0、Origin8.1 等软件。
2 结果与分析
2.1 川秋葵微粉组分的测定
制备的川秋葵微粉的得率为18.47%,组分见表1。
表1 川秋葵微粉的组分表
Table 1 The ingredient list of Sichuan okra micropowder

组分 粗脂肪/%总酚/(mg/g)含量 0.89±0.024 2.68±0.492 29.09±1.506 6.15±1.835 17.54±4.274 30.17±2.143 13.48±0.017 43.65±2.738 6.41±0.842 9.91±0.134 0.87±0.017粗蛋白质/%碳水化合物/%粗灰分/%水分/%不溶性膳食纤维/%可溶性膳食纤维/%总膳食纤维/%果胶/%总黄酮/(mg/g)
从表1可知,川秋葵微粉含有丰富的碳水化合物,包括果胶、可溶性膳食纤维和不可溶性膳食纤维等多糖成分。刘雪蕊指出[11]秋葵多糖提取物能有效抑制α-葡萄糖苷酶活性,可使糖尿病小鼠的血糖值明显降低,并可降低小鼠血清内的总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,T G)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol, LDL-C)含量,提高血清高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C),可以有效缓解由高血糖引发的脂代谢混乱的现象。有研究指出,高粱麸皮提取的黄酮类物质对α-淀粉酶活性具有良好的抑制效果[25-26]。由此推测,秋葵微粉降血糖活性可能与其富含多糖、黄酮类物质息息相关。
2.2 川秋葵微粉对α-葡萄糖苷酶活性的抑制
不同浓度下的川秋葵微粉对α-葡萄糖苷酶抑制作用结果见表2。
表2 川秋葵微粉对α-葡萄糖苷酶活性的抑制率
Table 2 Inhibition rate of Sichuan okra micropowder on αglucosidase activity
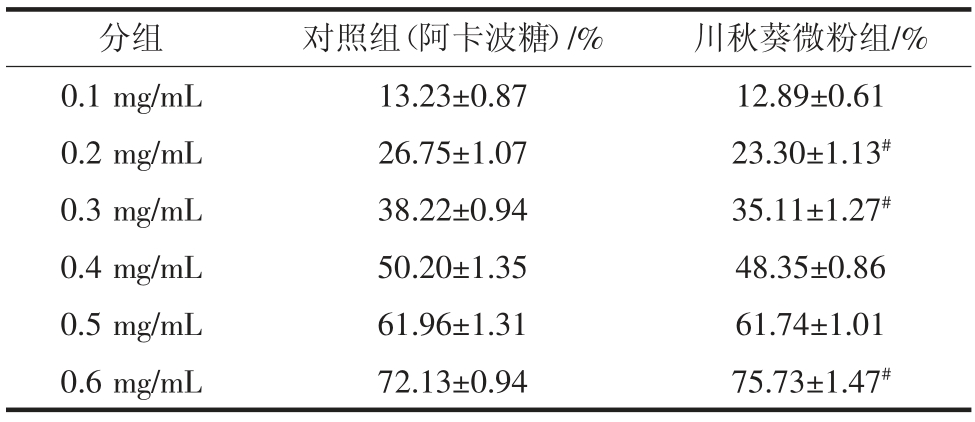
注:与对照组相比,#P <0.05,差异显著。
分组 对照组(阿卡波糖)/% 川秋葵微粉组/%0.1 mg/mL 13.23±0.87 12.89±0.61 0.2 mg/mL 26.75±1.07 23.30±1.13#0.3 mg/mL 38.22±0.94 35.11±1.27#0.4 mg/mL 50.20±1.35 48.35±0.86 0.5 mg/mL 61.96±1.31 61.74±1.01 0.6 mg/mL 72.13±0.94 75.73±1.47#
秋葵微粉浓度从0.1 mg/mL 增大到0.6 mg/mL 时,抑制率随微粉浓度的增大而增大。当秋葵微粉浓度为0.1 mg/mL 时,对α-葡萄糖苷酶抑制率为12.89%,当秋葵微粉浓度为0.6 mg/mL 时,抑制作用增强,抑制率达到75.73 %,说明秋葵微粉对α-葡萄糖苷酶抑制作用存在剂量依赖性。经计算得到秋葵微粉的IC50 为0.406 1 mg/mL,阳性药物阿卡波糖的IC50 为0.403 7 mg/mL,阿卡波糖对α-葡萄糖苷酶抑制活性优于秋葵微粉,但是差异不显著(P >0.05)。
2.3 川秋葵微粉对α-淀粉酶活性的抑制
不同浓度下的川秋葵微粉对α-淀粉酶抑制作用结果见表3。
表3 川秋葵微粉对α-淀粉酶活性的抑制率
Table 3 Inhibitory rate of Sichuan okra micropowder on the activity of α-amylase
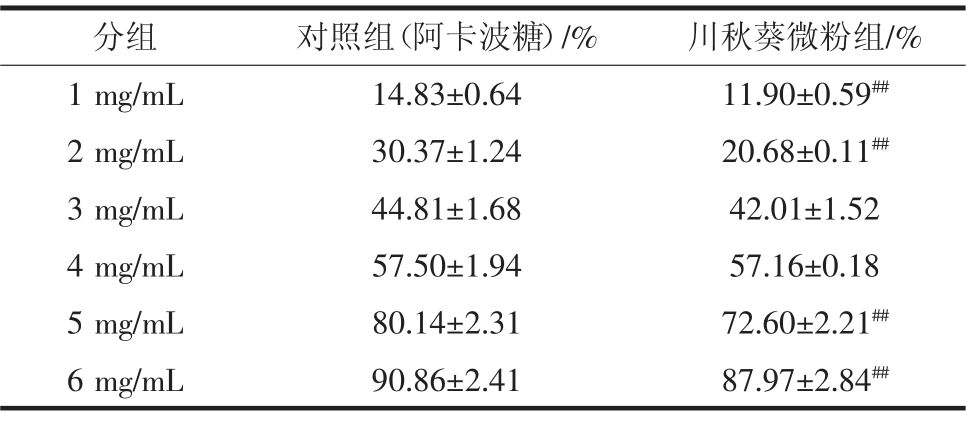
注:与对照组相比,##P <0.01,差异极显著。
分组 对照组(阿卡波糖)/% 川秋葵微粉组/%1 mg/mL 14.83±0.64 11.90±0.59##2 mg/mL 30.37±1.24 20.68±0.11##3 mg/mL 44.81±1.68 42.01±1.52 4 mg/mL 57.50±1.94 57.16±0.18 5 mg/mL 80.14±2.31 72.60±2.21##6 mg/mL 90.86±2.41 87.97±2.84##
秋葵微粉浓度从1 mg/mL 增大到6 mg/mL 时,抑制率呈上升趋势。当秋葵微粉浓度为1 mg/mL 时,对α-淀粉酶抑制率为11.90%,当秋葵微粉浓度为6 mg/mL时,抑制作用最强,抑制率达87.97%,说明川秋葵微粉对α-淀粉酶抑制作用存在剂量依赖性。经计算得到秋葵微粉的IC50 为0.737 1 mg/mL,阳性药物阿卡波糖的IC50 为0.699 4 mg/mL,阿卡波糖对α-淀粉酶抑制活性优于秋葵微粉,但差异不显著(P >0.05)。
2.4 川秋葵微粉对葡萄糖吸附能力的影响
膳食纤维可以通过吸附葡萄糖降低小肠葡萄糖浓度,从而达到降低血糖的作用[27],在不同葡萄糖浓度下(5 mmol/L~100 mmol/L)秋葵葡萄糖吸附能力如表4所示。
表4 川秋葵微粉在不同浓度下葡萄糖吸附能力
Table 4 Glucose adsorption capacity of Sichuan okra micropowder at different concentrations

注:同列数值后的不同小写字母表示两者差异显著(P <0.05);同列数值后的不同大写字母表示两者差异极显著(P <0.01)。
葡萄糖浓度/(mmol/L) 葡萄糖吸附量/(mg/g)5 374.94±1.58bA 10 385.99±3.92cB 50 397.08±0.64dC 100 369.06±1.34aA
有研究显示,食物的主要成分不同,与葡萄糖的结合能力不同,主要受食物成分的组成、微观结构、性质以及化学反应活性影响[28]。秋葵微粉富含膳食纤维、果胶,其本身是生物大分子,具有一定的空间网络结构,经微粉碎处理后,膳食纤维网络结构松散,比表面积增大,截留能力增强,有利于葡萄糖的吸附,这与杨远通等[29]研究结果相似。由表4可知,在葡萄糖浓度较低(5 mmol/L~50 mmol/L)时,随着葡萄糖浓度的增加,秋葵微粉对葡萄糖吸附能力提高,差异极显著(P<0.01)。常世敏等[30]研究也表明超临界CO2 处理梨渣得到的不溶性膳食纤维物对葡萄糖吸附能力和葡萄糖溶液的浓度相关,且随着葡萄糖溶液浓度的增加,其吸附能力随之增强。然而,当葡萄糖浓度为100 mmol/L时,秋葵微粉对葡萄糖吸附能力极显著下降(P <0.01)。这可能是由于随着葡萄糖浓度的提高,秋葵微粉中的膳食纤维对葡萄糖的吸附量接近饱和,吸附过程达到动态平衡[20]。
2.5 川秋葵微粉对葡萄糖透析延迟指数的测定
葡萄糖透析延迟指数(GDRI)能够反映秋葵微粉使葡萄糖在胃肠道被延迟吸收的能力,秋葵微粉对葡萄糖延迟吸收能力的影响见表5。
表5 川秋葵微粉在不同时间下葡萄糖透析延迟指数
Table 5 Glucose dialysate index of Sichuan okra micropowder at different times

注:同行数值后的不同小写字母表示两者差异显著(P <0.05);同行数值后的不同大写字母表示两者差异极显著(P <0.01)。
项目 葡萄糖透析延迟指数/%10 min 30 min 60 min 90 min对照组 0 0 0 0秋葵微粉 37.66±2.51aA 44.92±3.11bAB 49.63±4.45bB 47.48±2.55bB
由表5可知,秋葵微粉可延迟葡萄糖吸收,秋葵微粉对葡萄糖延迟吸收指数在10、30、60、90 min 时分别为(37.66±2.51)%、(44.92±3.11)%、(49.63±4.45)%、(47.48±2.55)%。试验结果进一步证实了秋葵微粉对葡萄糖具有较好的吸附能力,与2.4 中的结果一致。有研究表明,GDRI 与秋葵微粉中的膳食纤维中的糠醛酸含量相关[31]、与膳食纤维内在结构和表面特性也有一定的相关[31]。本试验中,秋葵微粉的GDRI 要显著高于橄榄核中提取纤维的GDRI(22 %~29 %)[32]、芒果皮中纤维的GDRI(21 %)[33]和杨桃果渣纤维的GDRI(25 %)[34]、麦麸中纤维的GDRI(5.3%)[35]。
同时,秋葵微粉对葡萄糖延迟吸收的能力随透析时间的增加呈增大趋势,这与冯雁波等[36]研究的松仁粕膳食纤维对葡萄糖延迟吸收的结果一致。与Daou等[18]研究的葡萄糖延迟吸收指数随透析时间的延长变化趋势一致。与10 min 对应的GDRI 比较,30 min 时GDRI 显著升高(P <0.05),60 min 与90 min 时的GDRI极显著升高(P <0.01);30 min 与60、90 min 对应的GDRI 差异不显著(P >0.05);60 min 与90 min 对应的GDRI 差异不显著(P >0.05)。可能的原因是秋葵微粉中的不溶性多糖与葡萄糖分子间和分子内作用力,如范德华力和氢键等相互作用达到饱和,吸附过程达到动态平衡,因而不能够吸附更多的葡萄糖分子[37]。
2.6 川秋葵微粉的GI 和GL
秋葵微粉的GI 和GL 值见表6,秋葵微粉为低GI食物和低GL 食物。食物的GI 值受到多方面因素的影响[38],例如食物的组分与含量、碳水化合物的类型以及食物的加工方式等因素。
表6 川秋葵微粉的GI 和GL 值
Table 6 GI and GL values of Sichuan okra micropowder

注:以葡萄糖粉作为参照食物(GI=100)[38]。
?
由表6可知,秋葵微粉富含膳食纤维、多酚类物质以及黄酮类物质,从而使其在调节血糖方面的生理功效明显增强。其次,对秋葵进行微粉碎处理,膳食纤维网络结构松散,比表面积增大,有利于葡萄糖的吸附延缓其吸收。
葡萄糖粉和秋葵微粉餐后2 h 血糖应答曲线如图1所示。

图1 葡萄糖粉和秋葵微粉餐后2 h 血糖应答曲线
Fig.1 Glucose response curve of glucose and okra powder 2 h after meal
与葡萄糖组相比,##P <0.01。
葡萄糖粉和秋葵微粉的空腹血糖值均在正常范围内。进食30 min 时,葡萄糖粉的血糖值达到最高峰,随后,葡萄糖粉的血糖值开始下降,血糖最高值为9.0 mmol/L,血糖最低值为4.9 mmol/L;而秋葵微粉的血糖值极显著低于葡萄糖粉(P<0.01),波动较小,呈现缓升缓降的趋势,血糖最高值为5.0 mmol/L,血糖最低值为4.6 mmol/L。相较于葡萄糖粉餐后血糖的速升速降,秋葵微粉更加有利于机体餐后血糖的稳定,是糖尿病患者良好的食物选择。
3 结论
通过体外血糖试验,研究秋葵微粉对α-淀粉酶和α-葡萄糖苷酶的活力抑制效果,根据相应的IC50可知,阿卡波糖对α-葡萄糖苷酶的活力抑制效果优于秋葵微粉(P >0.05),秋葵微粉IC50 为0.406 1 mg/mL,阿卡波糖的IC50 为0.403 7 mg/mL。阿卡波糖对α-淀粉酶活力的抑制能力也优于秋葵微粉(P >0.05),秋葵微粉的IC50 为0.737 1 mg/mL,阿卡波糖的IC50 为0.699 4 mg/mL。秋葵微粉对葡萄糖有较好的吸附能力,且随着葡萄糖浓度增加,秋葵微粉对葡萄糖的吸附能力先提高后下降,当葡萄糖溶液浓度为50 mmol/L 时,秋葵微粉的葡萄糖吸附能力最强(P <0.01),为(397.08±0.64)mg/g。秋葵微粉的GDRI 随透析时间延长而先增加后降低,60 min 达到最高值(49.63±4.45)%。通过人体血糖试验证实秋葵微粉属于低GI(40.8)和低GL(9.1)食物,秋葵微粉食用后2 h 血糖应答曲线极显著低于葡萄糖粉(P <0.01)。
糖尿病或糖耐量异常以及胰岛素抵抗为主要临床表现的代谢综合征(metabolic syndrome,MS)[39]是一种生活方式病,因此饮食选择对于MS 的防治至关重要。本试验结果为将秋葵微粉开发为具有改善血糖的食品添加剂、保健用品提供理论依据。
[1]Pasquel F J, Powell W, Peng L, et al. A randomized controlled trial comparingtreatment with oral agents and basal insulin in elderly patients with type 2 diabetes in long-term care facilities[J]. BMJ Open Diabetes Res Care,2015,3(1):e000104
[2]郭君,银金兰,康桂英.具有降血糖活性的植物药[J].内蒙古医学杂志,2004(5):362-363
[3]张丽娜.水翁花对胰脂肪酶和α-淀粉酶抑制活性及作用机制初步探讨[D].上海:华东理工大学,2012
[4]刘娜. 黄秋葵的综合利用及前景[J].中国食物与营养,2006(6):27-30.DOI:10.5297/ser.1201.002
[5]V Sabitha, S Ramachandran, K R Naveen, et al. Antidiabetic and antihyperlipidemic potential of Abelmoschus esculentus(L.)Moench.in streptozotocin-induced diabetic rats[J]. Journal of pharmacy & bioallied sciences,2011,3(3):397-402
[6]Okada Y, Okada M, Sagesaka Y. Screening of Dried Plant Seed Extracts for Adiponectin Production Activity and Tumor Necrosis Fac-tor-Alpha Inhibitory Activity on 3T3-L1 Adipocytes[J]. Plant Foods for Human Nutrition,2010,65(3):225-232
[7]Yamada K, Anai T, Hasegawa K. Lepidimoide, an allelopathic substance in the exudates from germinated seeds[J]. Phytochemistry,1995,39(5):1031-1032
[8]张娜.黄秋葵果胶的提取工艺研究[J].安徽农业科学,2012,40(35):17319-17321
[9]刘怡彤,段振华,马华林,等.超声波辅助提取黄秋葵多酚和多糖的工艺研究[J].食品工业科技,2013,34(21):246-253
[10]方晴霞,金戈.黄秋葵中总黄酮的含量测定[J].医学导报,2004,23(9):675
[11]刘雪蕊.黄秋葵多糖的提取及其降血糖活性研究[D].天津:天津科技大学,2017
[12]冯冠英,宋晓雪,徐志立,等.黄秋葵对糖尿病小鼠的降血糖作用[J].转化医学电子杂志,2017,4(11):44-47
[13]闫天龙.黄秋葵系列产品开发及关键技术研究[D].成都:西华大学,2016
[14]李加兴,石春诚,马浪,等.黄秋葵果胶理化特性的研究[J].食品科学,2015,36(17):104-108
[15]李孟秋,翟俊乐,田欢,等.黄秋葵提取物体外抗氧化活性的研究[J].中国食品添加剂,2015(10):65-69
[16]Chau C F , Huang Y L. Comparison of the Chemical Composition and Physicochemical Properties of Different Fibers Prepared from the Peel of Citrus sinensis L. Cv. Liucheng[J]. Journal of Agricultural and Food Chemistry,2003,51(9):2615-2618
[17]梅新,木泰华,陈学玲,等.超微粉碎对甘薯膳食纤维成分及物化特性影响[J].中国粮油学报,2014,29(2):76-81
[18]Daou C, Zhang H. Study on Functional Properties of Physically Modified Dietary Fibres Derived from Defatted Rice Bran[J].Journal of Agricultural Science,2012,4(9):85-97
[19]黄清霞,雷激,李华鑫,等.高生物活性柠檬膳食纤维的功能特性研究[J].食品工业科技,2012,33(5):226-229
[20]黄冬云,钱海峰,苑华宁,等.木聚糖酶制取米糠膳食纤维的功能性质[J].食品与发酵工业,2013,39(12):30-34
[21]郭晓蕾,朱思潮,翟旭峰,等.硫酸蒽酮法与硫酸苯酚法测定灵芝多糖含量比较[J].中华中医药学刊,2010,28(9):2000-2002
[22]李小玲,张文青,卫姝岑,等.燕麦荞麦加工食品血糖生成指数与血糖负荷的测定[J].临床医药实践,2017,26(4):249-252
[23]WOLEVER T M S, DAVID J A, ALEXANDR A L J. The glycemic index: methodology and clinical implication[J]. Am J Clin Nutr,1991(54):864-865
[24]SALMERN J, ASCHERIO A, RIMM E B, et al. Dietary fiber,glycemic load, and risk of NIDDM in men[J]. Diabetes Care, 1997,20(4):545-550
[25]APOSTOLIDIS E, KWON Y I, SHETTY K. Potential of cranberrybased herbal synergies for diabetes and hypertension management [J]. Asia Pacific Journal of Clinical Nutrition, 2006, 15(3):433-441
[26]刘睿,潘思轶,刘亮,等.高粱原花青素对α-淀粉酶活力抑制动力学的研究[J].食品科学,2005,26(9):189-192
[27]陈菊红,顾正彪,洪雁.改性马铃薯渣的功能特性研究[J].食品工业科技,2009,30(1):130-133
[28]郭雅靖,颜梦婷,林圣楠,等.几种原花青素的降血糖作用及与常见食品原料的结合研究[J].食品科学,2017,38(19):156-163
[29]杨远通.超微粉碎对猕猴桃渣膳食纤维功能性质的影响[J].食品与机械,2011,27(1):11-14
[30]常世敏,张玉星,田益玲.超临界CO2 对梨渣不溶性膳食纤维物化特性的影响[J].食品研究与开发,2016,37(7):97-101
[31]LOPEZ G,ZOS G, RINCON F,et al. Relationship between physical and hydration properties of soluble and insoluble fibre of artichoke[J].Journal of Agricultural and Food Chemistry,1996,44(9):2773-2778
[32]ROD RIGUEZ-GUTIERREZ G, RUIBO-SENENT F, LAMAMUNOZ A, et al. Properties of lignin, cellulose, and hemicelluloses isolated from olive cake and olive stones: Binding of water, oil, bile acids, and glucose[J]. Journal of Agricultural and Food Chemistry,2014,62(36):8973-8981
[33]CAMIRE M E, DOUGHERTY M P. Raisin dietary fibrecomposition and in vitro bile acid binding[J]. Journal of Agricultural and Food Chemistry,2003,51(3):834-837
[34]Chau C F,Chen C H,Lin C Y.Insoluble fiber-rich fraction derived from Averrhoa caramola: Hypoglycemic effects determined by in vitro methods[J].LWT-Food Science and Technology,2004,37(3):331-335
[35]Adiotom Re J, Eastwood M A, Edwa Rdsa, et al. Dietary fibre: In vitro methods that anticipate nutrition and metabolic activity in humans [J]. American Journal of Clinical Nutrition, 1990, 52(1):128-134
[36]冯雁波,包怡红.超微粉碎对松仁膳食纤维体外降血糖、降血脂功能的影响[J].食品工业科技,2016,37(23):342-346,350
[37]Chau C F,Chen C H,Lin C Y.Insoluble fiber-rich fractions derived from Averrhoa carambola: hypoglycemic effects determined by in vitro methods[J]. LWT-Food Science and Technology, 2004, 37(3):331-335.
[38]杨月欣,崔红梅,王岩,等.常见谷类和薯类的血糖生成指数[J].营养学报,2003,25(2):185-189
[39]吴铁良.代谢综合征诊治进展[J].现代预防医学,2010,37(16):3200-3202