微胶囊技术是利用成膜材料将固体、液体或气体完全包裹,与外界隔离的一种技术过程[1-2],微胶囊技术形成的微型容器称为微胶囊,其内部被包埋的物质称为芯材,芯材可以是气体、液体或固体,也可以是几种不同物质的混合体。包覆的芯材外层膜材料称为壁材,其包埋结构通常为单层结构或多层结构[3]。微胶囊化可以改变芯材的物理形态、控制芯材的释放、改善芯材稳定性、减少有效物质的损失、降低芯材毒副作用[4-5]。目前微胶囊技术已在食品、化工、医学、材料、环境、生物技术等诸多领域获得广泛应用[6-7]。
2-苯乙醇也称β-苯乙醇,化学名称为2-苯基乙醇(2-pheny ethyl alcohol),2-苯乙醇是一种具有玫瑰花气味的透明液体。它具有抗菌、抗炎、保肝、抗病毒、免疫调节、增强记忆、强心等功效[8-9]。苯乙醇是我国规定允许使用的食用香料,可应用在蜂蜜、面包和浆果等食品生产中,但由于2-苯乙醇在加工以及后续贮藏过程中容易挥发,失去其特征香味,不利于生产应用[10]。因此,对2-苯乙醇进行微胶囊化处理,使其作为芯材包埋在微胶囊壁材内部,能够有效防止其挥发,并且可以实现控制释放,提高2-苯乙醇的安全利用价值[11]。
羧甲基壳聚糖(carboxymethyl chitosan,CMC)是一种壳聚糖衍生物,具有良好的水溶性、乳化性、成膜性等特点,可用于微胶囊制备[12]。海藻酸钠(sodium alginate,SA)是一种来源于海藻的线性阴离子天然多糖,具有良好的成膜性、生物可降解性和生物相容性,也常作为药物释放载体和微胶囊壁材[13]。
本文以2-苯乙醇为芯材,选择水溶性良好的CMC、SA 为壁材,CaCl2 为交联剂,通过复凝聚法制备2-苯乙醇微胶囊。考察制备条件对微胶囊含油量、粒径以及表面形貌的影响,探索找出最佳制备条件,研究微胶囊的稳定性(快速释放、长期缓释性能、吸水对微胶囊结构的影响)。微胶囊在贮存期间,由于大部分壁材不可能很好的将芯材和外界环境完全隔绝,环境中的水分会随着时间的推移进入微胶囊中,这就需要精确考察微胶囊的吸水性能,但目前对于微胶囊的吸水性能的研究相对较少,需要一种直观准确的方法考察微胶囊的吸水性能。而氯化钴(cobalt chloride,CoCl2·6H2O)在环境中呈樱紅色,遇热完全脱水时变成蓝色。依水化程度能呈现出蔚蓝、天青、淡蓝、青紫、紫红、粉紅等色彩[14]。因此本文创新的利用氯化钴的特性将其作为指示剂,制备了CoCl2 水分指示剂微胶囊,利用色差仪考察微胶囊吸水量与颜色变化之间的关系,以更简单快速判断微胶囊的吸水情况,为2-苯乙醇安全高效利用提供理论依据。
1 材料与方法
1.1 材料与试剂
2-苯乙醇(>99.0%,色谱纯)、羧甲基壳聚糖(分析纯,水溶性,分子量:314 kDa)、海藻酸钠(化学纯,黏度:[(200±20)mPa·s]:阿拉丁公司;氯化钙(分析纯)、无水乙醇(分析纯):广州试剂厂;六水合氯化钴(分析纯):西陇化工。
1.2 仪器与设备
JJ-1 机械搅拌器、超声波清洗器:上海机械仪器公司;电子天平:赛多利斯科学仪器(北京)有限公司;CR-10 色差仪:柯尼卡美能达控股公司;Lambda 750 s紫外-可见-近红外分光光度计:美国PE 公司;S-3 000N 30 kV 扫描电子显微镜:日立公司;THZ-82 水浴恒温振荡器:金坛市盛蓝仪器制造有限公司;电子数显卡尺:Five sheep 公司;DHG-9030 A 电热恒温鼓风干燥箱:上海-恒科技有限公司;均质机:杭州精细设备厂。
1.3 方法
1.3.1 不同壁材含量微胶囊的制备
称取一定量CMC 倒入装有100 mL 去离子水的烧杯中,配成浓度分别为6、8、10、12、14 mg/mL 溶液,通过机械搅拌溶解均匀,再使用均质机在10 000 r/min 条件下均质10 min;称取一定量CaCl2 倒入装有50 mL去离子水的烧杯中,配成浓度分别为10、20、30、40、50 mg/mL 的溶液,通过机械搅拌溶解均匀,再使用均质机在6 000 r/min 条件下均质10 min,将溶解好的CaCl2 溶液逐滴缓慢滴入上述机械搅拌状态下的CMC溶液中;称取一定量SA 倒入装有100 mL 去离子水的烧杯中,配成浓度分别为20、25、30、35、40 mg/mL 的溶液,通过机械搅拌溶解均匀,将1 mL 的2-苯乙醇逐滴加到继续搅拌的SA 溶液中,再使用均质机在8 000 r/min条件下均质10 min,将均质完成后的2-苯乙醇/SA 溶液逐滴缓慢滴入到上述机械搅拌状态下的CMC/CaCl2混合液中。滴加完成后所得的微胶囊在烧杯中静置1 h,用去离子水洗涤几次、过滤后,将所得到的颗粒置于真空干燥箱中干燥,干燥条件为60 ℃,最终收集得到2-苯乙醇微胶囊产品。
1.3.2 2-苯乙醇微胶囊含量测定
称取0.2 g 的2-苯乙醇倒入50 mL 容量瓶中,用无水乙醇定容至刻度线并摇匀,配制成4 mg/mL 母液。分别移取200、400、600、800、1 000、1 200、1 400 μL 母液至10 mL 容量瓶中,加入无水乙醇定容摇均,配制成0.08、0.16、0.24、0.32、0.40、0.48、0.56 mg/mL 的2-苯乙醇标准样品,再分别在258 nm 波长条件下进行扫描。以吸光度为纵坐标,浓度为横坐标绘制标准曲线,得到线性回归方程:Y=0.0116X-0.0156,R2=0.997。
称一定量微胶囊置于研钵中,反复快速研磨均匀后将其移入25 mL 容量瓶中,加入无水乙醇定至刻度线并摇匀,超声1 h 后过滤,在258 nm 条件下检测滤液吸光度Y,通过标准曲线和所得吸光度计算出2-苯乙醇含量。微胶囊中2-苯乙醇含量计算公式如下:
式中:Y 为滤液吸光度;m 为微胶囊质量,g。
1.3.3 2-苯乙醇微胶囊结构表征
采用扫描电镜观察2-苯乙醇微胶囊的表面形貌。取适量微胶囊用双面胶贴于样品圆台上,固定后进行喷金。喷金条件是:抽真空至压力小于10 Pa,并持续3 min~4 min;控制电流量在15 mA 以上;喷金时间为120 s。扫描电镜条件为:电压为10 kV,样品放置高度为15 mm。采用复凝聚法制备微胶囊的粒径较大,故可直接使用游标卡尺量出微胶囊粒径。从样品中随机选取50 个微胶囊颗粒,用电子数显游标卡尺进行逐个测量,并且对每个微胶囊从3 个不同角度进行测量并取平均值为一个微胶囊的粒径,最终50 个微胶囊粒径的平均值为2-苯乙醇微胶囊的平均粒径,计算公式如下:
式中:di 为第i 个微胶囊的粒径,mm;n 为微胶囊的总个数。
1.3.4 2-苯乙醇微胶囊性能测试
1.3.4.1 微胶囊的快速释放性能
包埋含量最高编号为CMC4 的微胶囊作为缓释试验样品,称取0.2 g 制备好的微胶囊置于100 mL 的锥形瓶中,准确量取60 mL 无水乙醇加入锥形瓶中,用橡皮塞将锥形瓶口密封,放入水浴恒温振荡器内,调节水温为30 ℃并以一定的频率震荡。然后在10、20、40、60、80、100、120、180 min 时间节点时从溶液体系中取出少量液体,并加入同等体积的无水乙醇。通过测试液体中2-苯乙醇的吸光度,计算出微胶囊随时间释放2-苯乙醇到溶液中的浓度变化情况。以相同的条件对微胶囊在50 ℃和70 ℃的加热条件下测试其快速释放性能,考察温度对微胶囊释放性能的影响。
1.3.4.2 微胶囊的自然长期释放性能
将所制备3 个系列微胶囊中各选取一组微胶囊放于密封袋中贮存一段时间,分别从贮存1、3、7、18、35 d 的样品中称取0.2 g 微胶囊,用研钵进行快速研磨,迅速将其研磨好的粉末转入25 mL 容量瓶内加入无水乙醇定容,再放入超声波清洗器中超声1 h 后过滤,测试滤液的吸光度,通过1.3.2 中的标准曲线方程式求出溶液中2-苯乙醇的浓度,并计算出微胶囊在不同时间段释放出的2-苯乙醇含量。
1.3.4.3 微胶囊的吸水性能
研究微胶囊吸水性能,以水分指示剂CoCl2 代替2-苯乙醇为芯材,采用上述相同制备条件制备一组水分指示剂CoCl2 微胶囊。称取2.9 g 水分CoCl2 微胶囊放在表面皿上,置于常温空气中,然后每隔一段时间对其进行称重,同时通过色差仪测试样品的L*、a*、b*值并记录,观察这3 个值或其中某一个值随吸水量的变化规律,拟合计算吸水量与L*、a*、b*值的关系。
1.4 数据处理
采用Origin 9.0 和Excel 2010 对数据进行处理作图,采用Photoshop 8.0 对图像进行编辑处理。
2 结果与分析
2.1 制备条件对微胶囊2-苯乙醇含量的影响
采用单因素试验方法考擦各壁材用量对微胶囊2-苯乙醇含量、粒径和表面形貌的影响,试验分成3个系列。首先确定SA 浓度为30 mg/mL、CaCl2 浓度为30 mg/mL,CMC 浓度分别为6、8、10、12、14 mg/mL,相应编号为CMC1、CMC2、CMC3、CMC4、CMC5;其次确定SA 浓度为30 mg/mL、CMC 浓度为12 mg/mL,CaCl2浓度分别为10、20、30、40、50 mg/mL,相应编号为Ca1、Ca2、Ca3、Ca4、Ca5;最后确定CMC 浓度为12 mg/mL、CaCl 浓度为30 mg/mL,SA 浓度分别为20、25、30、35、40 mg/mL,相应编号为SA1、SA2、SA3、SA4、SA5,3 个系列试验所加入的2-苯乙醇的量都为1 mL,结果如图1所示。

图1 壁材用量对微胶囊中2-苯乙醇含量的影响
Fig.1 The effect of wall material usage for 2-Phenylethanol content in microcapsules
由图1可知,壁材中CMC、CaCl2、SA 的用量对微胶囊中2-苯乙醇含量存在一定影响。随着CMC 用量的增加,微胶囊中2-苯乙醇含量也随之增大。当CMC用量为12 mg/mL 时,微胶囊包埋的2-苯乙醇含量为1.41%,达最大值。可当CMC 浓度高于12 mg/mL 时,微胶囊中2-苯乙醇含量反而会开始下降。随着SA 含量的增加,微胶囊包埋2-苯乙醇的含量也先增大后降低,当SA 用量为35 mg/mL 时,微胶囊中的2-苯乙醇含量最高,为1.42%。CMC 与SA 通过静电相互作用,当二者其中之一用量过大时,会有剩余的另一种壁材残留在溶液中,导致溶液电导率增大,从而使得微胶囊乳液不稳定,乳液中成球率降低,包埋率下降[15]。另外,当溶液中SA 的浓度逐渐增大,使得溶液的黏度也逐渐增大,导致体系中CMC 与CaCl2 混合不均匀,降低了微胶囊芯材的包埋效率[16]。当CaCl2 的用量为30 mg/mL时,微胶囊中含有2-苯乙醇的量最高,为1.40%。因为SA 与CaCl2 中的钙离子交联生成的SA 沉淀,能在芯材表面形成一层保护膜,此时交联效果最好,所形成的微胶囊包埋效果最佳。
所制备的微胶囊颗粒平均直径大小分布在1.25mm~1.53 mm 之间。当CMC 用量为10 mg/mL 时,微胶囊平均粒径最大为1.37 mm。当CaCl2 的用量为10 mg/mL时,微胶囊平均粒径最大为1.53 mm。当SA 的用量为40 mg/mL 时,微胶囊平均粒径最大为1.46 mm。
2.2 微胶囊的快速缓释性能
从制备的样品中选择CMC4 微胶囊,固定水浴恒温振荡器的振动频率,通过在不同温度(30、50、70 ℃)下对微胶囊的快速释放进行测试,研究其快速释效果,试验结果如图2。
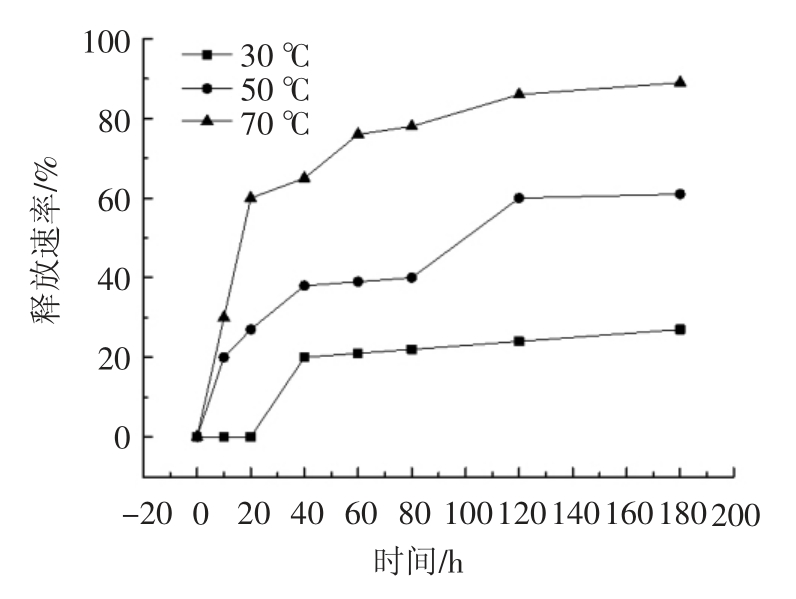
图2 2-苯乙醇微胶囊在不同温度下的缓释曲线图
Fig.2 The release plot of 2-phenylethyl alcohol microcapsules at different temperatures
在较低温度30 ℃下,样品在前20 h 基本没有释放,40 h~200 h 范围内,释放率逐渐增加到20%~30%。但是当温度增加到50 ℃和70 ℃时,微胶囊的缓释趋势均为前期释放速率较快,后期释放速率趋于平缓,这是由于释放开始时,包埋在微胶囊内表面和囊壁内的芯材2-苯乙醇先释放,传质阻力小,所以释放速率大,当微胶囊外表层的2-苯乙醇释放完毕后,微胶囊内部的2-苯乙醇在向外释放过程中,传质阻力变大,释放速率逐渐趋于平缓[17]。结果表明在较低温度下,微胶囊释放较慢,而由于芯材2-苯乙醇蒸气压随着温度的升高而升高,产生更强的不规则运动,挥发性增加,故在温度较高时释放速率较快,释放曲线也呈现差异[18]。因此,低温有助于2-苯乙醇微胶囊的贮存。
2.3 微胶囊的自然长期缓释性能
从制备的样品中选择CMC4(a)、SA4(b)、Ca3(c)3组微胶囊,将它们装入密封袋中,放置在阴凉干燥处,不进行外界辅助处理使其自然释放,由此来观察微胶囊的长期释放效果,结果见图3。
由图3可知,微胶囊中的2-苯乙醇含量随着时间的推移而逐渐降低,前7 d2-苯乙醇的释放速率快,CMC4、Ca3、SA4 样品的2-苯乙醇累积释放速率分别达到12.86%、23.1%、17.16%。而随着贮藏时间的推移,累计释放速率增加逐渐变缓,并在35 d 后CMC4、Ca3、SA4 样品累积释放速率才分别达到24.67 %、32.77%、31.17%。这一现象是由于在刚制备出的样品,微胶囊粒径小,比表面积大,平均孔径大,并且在微胶囊微量内表面芯材释放速度快,所以开始时微胶囊释放速率大;随着时间的推移,微胶囊表层的芯材已经释放完全,内部芯材开始逐步向外释放,传质推动了减小,从而使得微胶囊释放速率降低[19]。试验结果表明,微胶囊放置在密封袋中也会存在一定程度的释放,一方面是由于微胶囊表面及表层所含的2-苯乙醇进行扩散释放所致,而另一方面由于市场上所售的普通密封袋密封效果欠佳,导致微胶囊中的芯材容易挥发,同时外界水分会进入袋中,与微胶囊接触引起壁材溶胀,从而进一步促进芯材释放[20]。因此,对2-苯乙醇进行微胶囊化处理后稳定性得到较大提高,对内部芯材具有持久的释放作用。

图3 微胶囊中2-苯乙醇长期释放速率曲线
Fig.3 2-phenylethyl alcohol long-term release rate curvet of the microcapsules at different time
2.4 微胶囊的表观形貌以及吸水性测试
不同存放时间下2-苯乙醇微胶囊的表面形貌如图4所示。
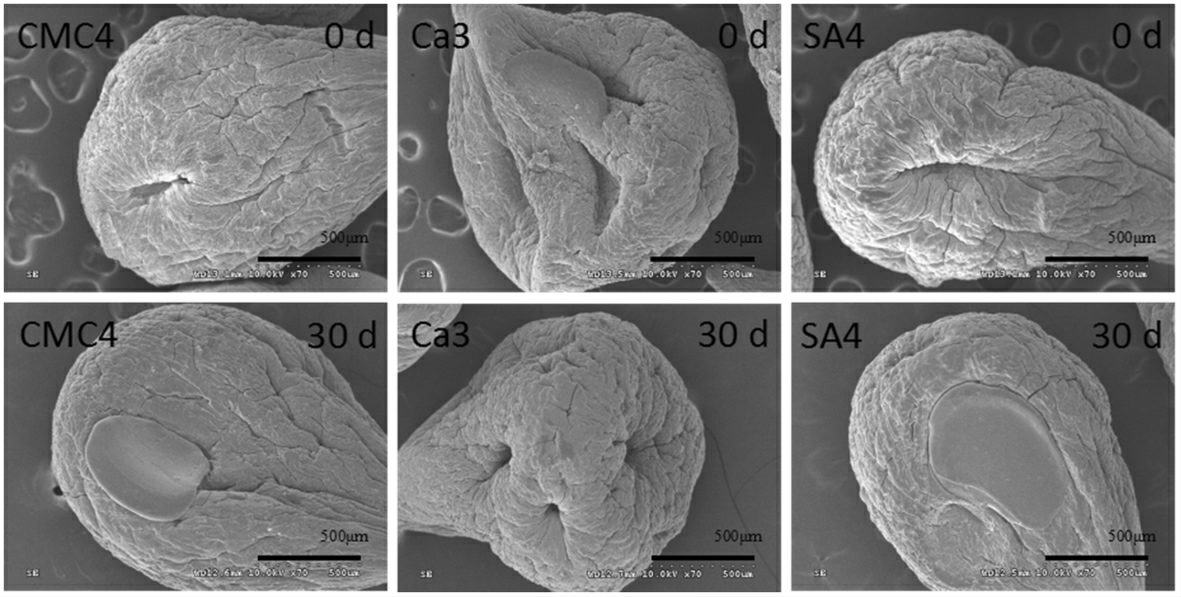
图4 2-苯乙醇微胶囊在新制备出时(0 d)以及贮藏30 d 后的表观形貌微胶
Fig.4 The morphology of 2-phenylethyl alcohol microcapsules prepared at the time of preparation(0 d)and 30 days after storage
新制备的CMC4、Ca3、SA4 3 组样品(0 d),微胶囊呈不规则球形,并在一端出现拖尾的现象,这是复凝聚法制备微胶囊的过程中,形成的微胶囊重量较大,在重力作用下导致微胶囊产生拖尾而呈现不规则形貌[21],而且微胶囊表面出现一定程度的褶皱,并且有一定的裂纹,这是用复凝聚法制备微胶囊的干燥过程中,样品快速失水而造成的[22]。将CMC4、Ca3、SA4 3 组微胶囊放置30 d 后,再对其表面形貌变化进行观察,从图中可看出,微胶囊在经过一段时间的贮存后,表面形貌变得比较圆润,而且裂纹减少,这是由于微胶囊在吸收水分后膨胀所致的。
从制备的样品中选择CMC4(a)、SA4(b)、Ca3(c)3 组微胶囊装入市面可买到的密封袋中,在室内阴暗、室温为25 ℃左右的条件下贮藏,进行吸水性能测试,得到微胶囊在不同贮存时间的质量,如图5所示。
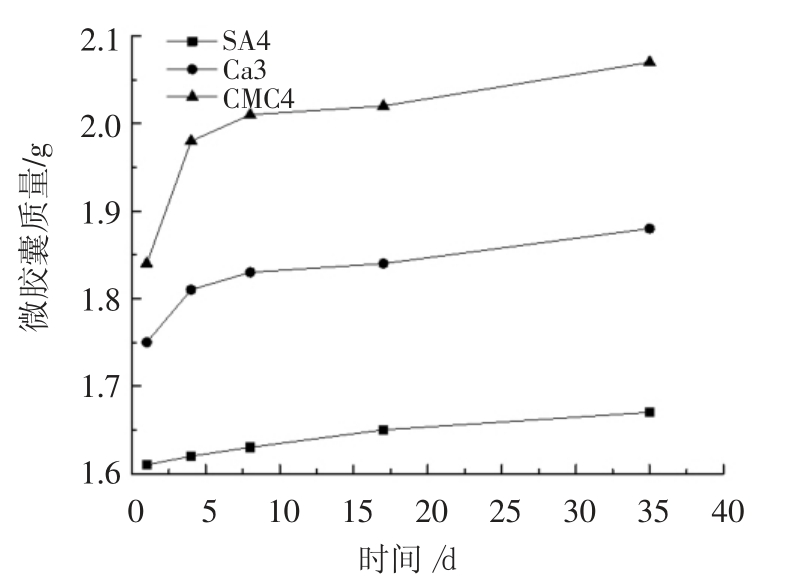
图5 2-苯乙醇微胶囊的吸水性能
Fig.5 Water absorption properties of 2-phenylethyl alcohol microcapsules
从图5可以看出,微胶囊在贮存过程中会逐渐吸收空气的水分,且其吸收水分的能力随着时间推移而逐渐再减小。贮存初始阶段(前7 d)时,微胶囊的吸水能力较强,随着时间的推移,微胶囊的吸水能力下降。这可能的原因是在贮存初始阶段,制得的微胶囊刚刚干燥完成,其表面含水量较低,因此微胶囊的吸水能力会较强;但随着贮存时间的推移,微胶囊表面吸附的水分浓度逐渐与空气中的水分浓度接近,从而使吸附的水分逐渐向微胶囊的内部扩散,传质推动力减小,因此使微胶囊的吸水能力降低[23]。试验表明在长时间的贮存中,选择的壁材能较好的限制环境的水分进入微胶囊内部,保护芯材。
2.5 微胶囊吸水量与颜色变化的关系
以水分指示剂氯化钴(CoCl2)作为芯材,根据上述制备2-苯乙醇微胶囊的条件,制备对应的CoCl2 微胶囊,利用色差仪测试CoCl2 微胶囊的L*、a*、b*值(L*代表明暗度,正值说明样品比标准板偏亮,负值则偏暗;a*代表红绿色,正值说明样品比标准板偏红,负值则偏绿;b*值代表黄蓝色,正值说明样品比标准板偏黄,负值则偏蓝)[24],找到微胶囊吸水量与其颜色变化的数学关系。
在表面皿中放入2.9 g 新制备的指示剂微胶囊,并长时间置于常温空气中,微胶囊的颜色变化如图6所示。
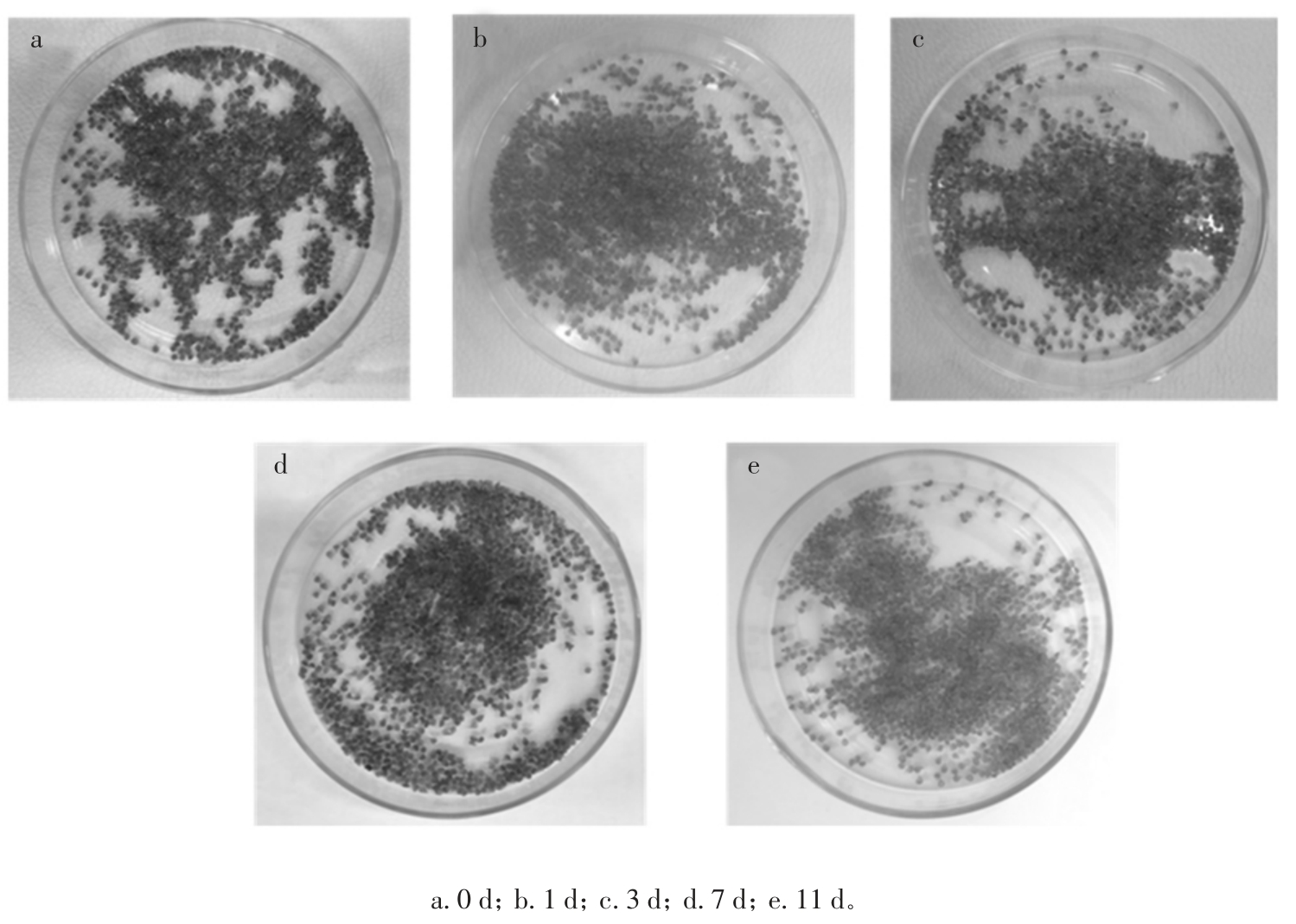
图6 含CoCl2 微胶囊颜色随放置时间的变化
Fig.6 The Color of CoCl2 microcapsules at different storage time
图6a 为新制备出的微胶囊,呈蓝色。在空气中放置一天后,部分微胶囊转变为蓝紫色,如图6b所示。再相隔3 d 后,微胶囊全部转变为紫色,如图6c所示。7 d后,放置在空气中的指示剂微胶囊变成粉色,如图6 d所示。放置11 d,微胶囊全部变成红色,如图6e所示。由于无水CoCl2 初始呈蓝色,在吸水后呈现红色,所以在刚制备出的指示剂微胶囊几乎不含水分,其颜色为无水CoCl2 初始颜色蓝色,随着微胶囊逐渐吸收空气中的水分,其颜色也随之由蓝紫色逐渐向粉红色转变,并再进一步吸水后呈红色。
对放置于常温空气中的指示剂微胶囊每隔一段时间,进行称重计算微胶囊的吸水量,利用色差仪对样品的L*、a*、b*值进行检测,进而分析微胶囊吸水量和L*、a*、b*值之间的对应关系。研究发现,微胶囊的吸水量与b*值变化有着较高的拟合度,结果如图7所示。
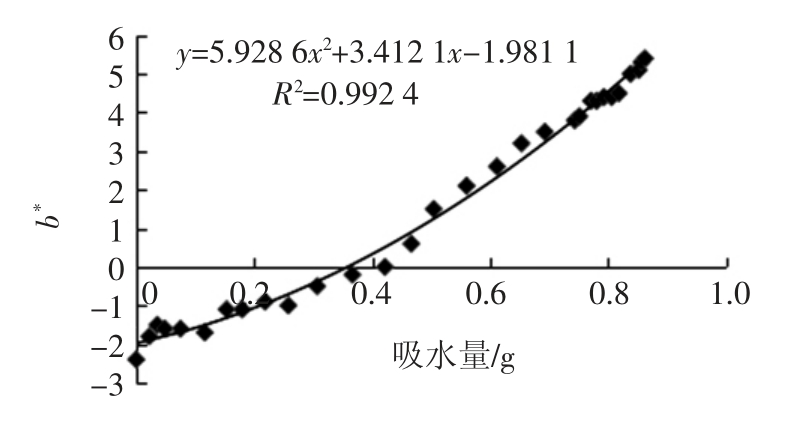
图7 微胶囊吸水量与CoCl2 的b*的变化曲线
Fig.7 The relationship between absorbed water and b*of CoCl2 microcapsules
微胶囊的吸水量与b*值变化呈现一种二次函数曲线关系,以微胶囊的吸水量为横坐标,以b*值变化为纵坐标,可以得到拟合曲线公式为:Y=5.928 6X2+3.412 1X-1.981 1,R2=0.992 4,该结果有助于通过简单测试微胶囊颜色变化来获得其吸水情况,从而了解微胶囊的结构变化。
3 结论
以羧甲基壳聚糖、海藻酸钠为壁材,2-苯乙醇为芯材,采用复凝聚法制得2-苯乙醇微胶囊,发现在微胶囊最佳制备条件下,2-苯乙醇包埋量最高可达1.42%。在普通塑料密封袋中贮存微胶囊,微胶囊中2-苯乙醇包埋量有所下降,35 d 后的包埋量降至0.98%,表明需选择合适的贮存方式以保持微胶囊的品质。环境温度对微胶囊释放存在影响,通过调节使用温度可实现对2-苯乙醇的缓控释放。以CoCl2 作为指示剂制备了指示剂微胶囊,采用色差仪研究微胶囊吸水量与颜色变化关系之间的关系,并建立了两者的定量关系,发现它们存在二次函数曲线关系;在精油微胶囊中加入指示剂微胶囊,可以简便地观测分析微胶囊的含水量和微胶囊结构。本文所提供的研究方法和结果,对其他种类微胶囊的安全使用和贮藏亦具有一定指导意义。
[1]Yang Z, Peng Z, Li J, et al. Development and evaluation of novel flavour microcapsules containing vanilla oil using complex coacervation approach[J].Food Chemistry,2014,145(7):272-277
[2]Neubauer M P, Poehlmann M, Fery A. Microcapsule mechanics:From stability to function [J].Advances in Colloid & Interface Science,2014,207(1):65-80
[3]Xie Y,Zou J.The Effects of Creep-recovery Characteristics of Wall Material on Morphology of Microcapsule[J].Journal of Chinese Institute of Food Science & Technology,2017,17(7):9-16
[4]Pothakamury U R, Barbosa-Cánovas G V. Fundamental aspects of controlled release in foods[J].Trends in Food Science & Technology,1995,6(12):397-406
[5]Rao A V, Shiwnarain N, Maharaj I. Survival of Microencapsulated Bifidobacterium pseudolongum, in Simulated Gastric and Intestinal Juices[J].Canadian Institute of Food Science & Technology Journal,1989,22(4):345-349
[6]Dima C,Pătra cu L,Cantaragiu A,et al.The kinetics of the swelling process and the release mechanisms of Coriandrum sati-vum,L.essential oil from chitosan/alginate/inulin microcapsules[J].Food Chemistry,2015,195(2):39-48
[7]Shamaei S,Seiiedlou S S,Aghbashlo M,et al.Microencapsulation of walnut oil by spray drying:Effects of wall material and drying conditions on physicochemical properties of microcapsules[J].Innovative Food Science & Emerging Technologies,2017,39:101-112
[8]Xue Z,Yan R,Yang B.Phenylethanoid glycosides and phenolic glycosides from stem bark of Magnolia officinalis[J].Phytochemistry,2016,127:50-62
[9]Miha’M,Vereš R,Markoš J,et al.Intensification of 2-phenylethanol production in fed-batch hybrid bioreactor:Biotransformations and simulations[J].Chemical Engineering & Processing Process Intensification,2012,57-58(1):75-85
[10]沈靖轩,肖维毅,徐兰兰,等.苯乙醇微胶囊的稳定性及热释放行为研究[J].日用化学工业,2017,47(5):277-280
[11]Olivares A, Silva P, Altamirano C. Microencapsulation of probiotics by efficient vibration technology [J].Journal of Microencapsulation,2017,34(7):667-674
[12]Rinaudo M. Chitin and chitosan:properties and applications[J].Progress in polymer science,2006,31(7):603-632
[13]杨秀敏,李芝,王志.啶虫脒/羧甲基壳聚糖微球的制备与控制释放性能的研究[J].河北农业大学学报,2011,34(4):95-98
[14]Liu X P, Zhao H L, Yu-Hui H E, et al. Measurement of Soil Water Diffusivity of Surface Soil from Sandy Croplands and Application Study of Cobalt Chloride Test Paper[J].Journal of Soil & Water Conservation,2007,21(6):147-150
[15]Park S J,Shin Y S,Lee J R.Preparation and Characterization of Microcapsules Containing Lemon Oil[J].Journal of Colloid & Interface Science,2001,241(2):502-508
[16]Kai M P,Brighton H E,Fromen C A,et al.Tumor presence induces global immune changes and enhances nanoparticle clearance[J].ACS Nano,2016,10(1):861-870
[17]韩光涛,杨子明,彭政,等.广藿香油缓释微胶囊的制备及其性能分析[J].材料导报,2013,27(6):108-111
[18]Kim H, Park C. Enzymatic synthesis of phenethyl ester from phenethyl alcohol with acyl donors[J].Enzyme & Microbial Technology,2017,100:37-44
[19]Ramarao C,Ley S V,Smith S C,et al.Encapsulation of palladium in polyurea microcapsules[J].Chemical Communications,2002,10(10):1132-1133
[20]Wang Z,Gao J,Ustach V,et al.Tunable Permeability of Crosslinked Microcapsules from pH-Responsive Amphiphilic Diblock Copolymers:A Dissipative Particle Dynamics Study[J].Langmuir,2017,33(29):72-88
[21]Ach D, Briançon S, Broze G, et al. Formation of microcapsules by complex coacervation[J].Canadian Journal of Chemical Engineering,2015,93(2):183-191
[22]Li R,Chen R,Liu W,et al.Preparation of enteric-coated microcapsules of astaxanthin oleoresin by complex coacervation[J].Pharmaceutical Development & Technology,2016:1-26
[23]李昌宝,李丽,吴雪辉,等.罗汉果籽油微胶囊的乳化配方及其性质分析[J].南方农业学报,2012,43(8):1203-1207
[24]曹连平,王力民,李锡军,等.色差仪的应用实践[J].印染,2004,30(24):33-38