防腐剂是一种能防止食品腐败变质的食品添加剂,主要原理就是抑制食品中微生物的繁殖[1]。乳酸菌是一大类发酵糖产生大量乳酸的兼性厌氧菌,许多乳酸菌除产生乳酸、乙酸和双乙酰外,还可以产生一些具有抑菌性能的细菌素,这些物质不仅能保持食品的风味还可以抑制食品腐败菌的生长,在食品防腐保鲜方面起着重要的作用[2-3]。乳杆菌属细菌是乳酸菌属中最为重要的菌属,作为一种安全的益生菌,乳酸菌大量的分布在海洋鱼类的肠道中,可以增强动物包括鱼在内的机体免疫反应和生长[19],近年来关于鱼肠道乳酸菌的分离以及抑菌物质研究、乳杆菌食品防腐保鲜逐渐成为热点。
李晓婷等[4]研究发现ALAC-1 和ALAC-4 两株乳杆菌对黄曲霉具有良好的抑菌作用,其菌株代谢产物中的蛋白类、有机酸等物质可以抑制霉菌的生长;杜琨[5]研究发现添加乳酸菌产生抑菌物质的保鲜剂可提高冷却猪肉在冷藏过程中的保鲜效果,延长冷却猪肉的保质期。马欢欢等[6]研究表明,Lb.plantarum DL3 对黑曲霉的抑制率高达92.28%,发现其对黑曲霉的抑菌作用主要通过破坏黑曲霉孢子的完整性,从而抑制其生长、繁殖。刘佳秀等[22] 发现海洋鱼类来源的L.plantarumY12 具有抑制鱼肉中腐败菌的生长、防止鱼肉腐败的功能。
本文主要采用牛津杯琼脂扩散法研究从4种海鱼(鲅鱼、大黄鱼、梭鱼和鸦片鱼)肠道中分离出的乳杆菌代谢产物对几种常见的食品腐败菌的拮抗效果,旨在筛选出拮抗活性较强的乳杆菌菌株,并初步判定出菌株产生的主要抑菌物质属于哪类物质,能加速人类对海洋源乳酸菌资源的开发和利用,对海洋源乳酸菌将来在乳制品、蔬菜、饲料、肉制品的发酵以及食品的防腐保鲜中的应用都有指导的意义。
1 材料与方法
1.1 材料与试剂
海鱼:大连市内海鲜商行;试验所用6种腐败菌大肠杆菌(Escherichia coli)、金黄色葡萄球菌(Staphylococcus aureus)、沙门氏菌(salmonella)、单增李斯特菌(Listeria monocytogenes),志贺氏菌(Shigella Castellani)、副溶血性弧菌(Vibrio Parahemolyticus)标准菌株:大连工业大学大连市益生菌功能研究重点实验室保存菌株;MRS 琼脂、MRS 肉汤、LB 营养肉汤、LB琼脂培养基、牛肉膏、酵母膏、蛋白胨、胰蛋白胨、大豆蛋白胨:北京奥博星生物技术有限责任公司;胃蛋白酶:北京索莱宝科技有限公司;氯化钠、乙酸钠:天津石英钟厂霸州市化工分厂;30 %过氧化氢、无水葡萄糖、磷酸氢二钾、MnSO4·4H2O:天津市科密欧化学试剂有限公司;MgSO4·7H2O:天津市瑞金特化学品有限公司。
1.2 主要仪器设备
DNP-9082 型电热恒温培养箱、电热恒温通风干燥箱:上海精宏实验设备有限公司;SW-CJ-2FD 超净工作台:苏州安泰空气技术有限公司;5804R 型冷冻离心机:Eppendorf 中国有限公司;AW200SG 型厌氧工作站:英国ELECTROTEK 公司;SX-500 型全自动高压灭菌锅:日本Tomy Digital Biology 公司;PL303 型电子分析天平、S210-K 型SevenCompact pH 计:梅特勒-托利多仪器有限公司;V-1100D 型可见分光光度计:上海美谱达仪器有限公司;KQ5200DE 型数控超声波清洗器:昆山市超声仪器有限公司;SL-II 型层析实验冷柜:宁波新芝生物科技股份有限公司;L320 生物光学显微镜:深圳市西派克光学仪器有限公司。
1.3 方法
1.3.1 海鱼肠道菌株分离
超净工作台内,用70%酒精擦拭海鱼鱼体表面解剖海鱼胃肠道、无菌剪刀剪碎置于无菌研钵中,加入0.85%灭菌的生理盐水15 mL,研磨3 min,形成匀浆液,吸取1 mL 溶液作为海鱼肠道原液。取0.1 mL 原液加入0.9 mL 0.85%的无菌生理盐水试管中,进行梯度稀释,吸取100 μL 的稀释液于MRS 固体培养基上涂布,30°C 厌氧培养48 h,直至形成单个菌落。
挑选菌落形态良好的单菌落置于5%过氧化氢溶液的载玻片中,进行过氧化氢酶试验[7]。0.5 min 内产生气泡的为过氧化氢酶阳性细菌、反之为过氧化氢酶阴性细菌。
对过氧化氢酶阴性菌株进行革兰氏染色,观察菌株颜色,菌株呈现蓝紫色为革兰氏阳性细菌(G+)、呈现红色为革兰氏阴性细菌(G-)[18]。
以过氧化氢酶试验阴性、革兰氏染色阳性的菌株进行后续试验,筛选具有抑菌活性的乳杆菌。
1.3.2 初筛乳杆菌的抑菌试验
采用牛津杯琼脂扩散法[8]进行抑菌试验,牛津杯直径为8 mm,以抑菌圈的平均直径±标准误差来描述菌株抑菌能力的强弱。
取0.1 mL 乳杆菌菌液接种于5 mL MRS 培养液中,37 ℃培养18 h,连续传代2 次后于4 ℃保存待用。取0.1 mL 大肠杆菌、沙门氏菌、副溶血性弧菌、志贺氏菌属和金黄色葡萄球菌菌液接种于5 mL LB 肉汤培养基中,0.1 mL 单增李斯特菌接种于5 mL TSA-YE 培养基中,传两代后使用。
将活化的乳酸菌发酵液4℃、8000r/min 离心10min,弃沉淀(菌体)保留上清液,并过0.22 μm 滤膜除菌,收集滤液即为乳杆菌上清液,置4 ℃冰箱中保存备用。
以大肠杆菌为指示菌,采用牛津杯琼脂扩散法研究乳杆菌上清液的抑菌性能,从中初筛选出抑菌活性较强的几株乳杆菌株。
同样采用牛津杯琼脂扩散法研究初筛乳杆菌对金黄色葡萄球菌、单增李斯特菌、志贺氏菌、副溶血性弧菌和沙门氏菌的抑菌效果。
1.3.3 乳杆菌代谢产物中抑菌物质的确定
1.3.3.1 排除有机酸试验
选取革兰氏阴性大肠杆菌和革兰氏阳性金黄色葡萄球菌来作为指示菌,筛选出具有抑菌活性的乳杆菌所产生的抑菌物质。首先排除有机酸的干扰,用1 mol/L 的NaOH 中和菌株上清液中的有机酸,将pH值调至空白MRS 的pH值,并采用牛津杯琼脂扩散法进行抑菌试验,1 号孔加入正常的发酵上清液,剩下3 个孔加入中和酸后的上清液。
1.3.3.2 排除过氧化氢试验
若证明了乳杆菌代谢产物不完全是有机酸在起作用,则需要进行过氧化氢作用的排除试验,试验中将离心获得的乳杆菌发酵上清液在80 ℃水浴锅中加热10 min 使过氧化氢充分分解后进行抑菌试验[9]。试验中以未经处理的发酵上清液作为对照。
1.3.3.3 蛋白酶敏感性试验
分别用中性蛋白酶和胃蛋白酶处理发酵上清液[10]。用1 mol/L NaOH 调上清液pH值至中性蛋白酶最适pH 7.0,控制加酶量0.5 mg/mL,37 ℃水浴2 h 后,再用1 mol/L HCl 调pH值至发酵液原pH值进行抑菌试验,而胃蛋白酶处理的样品不需要调整pH值。试验过程中以未经蛋白酶处理的乳杆菌上清液作对照。如果仅为验证在酸性条件下才起作用的细菌素,则只需要将上清液用胃蛋白酶进行处理。
1.3.4 统计分析
所有试验均进行了重复试验,试验结果采用IBM SPSS 22.0 软件进行统计分析,比较所得数据之间的显著差异性(P<0.05)。
2 结果与讨论
2.1 海鱼肠道菌株的筛选
海鱼肠道菌株的镜检及过氧化氢酶试验结果见表1。
由表1可知从黄鱼、鸦片鱼、鲅鱼和梭鱼4种海鱼肠道中筛选出的41 株菌株全部为革兰氏阳性菌,其中包括21 株杆菌和20 株球菌,通过过氧化氢酶试验发现21 株杆菌全部为过氧化氢酶试验阴性菌,因此初步认定乳杆菌属细菌,在剩下的20 株球菌中,菌株B2-11 为过氧化氢酶试验阳性菌株,因此可以排除其为乳酸菌属细菌的可能,其余的球菌则可能是乳酸球菌属、链球菌属或肠球菌属细菌。通过对21 株杆菌菌落形态以及其在显微镜下染色后形态的观察,最终筛选了16株杆菌作为后续的研究菌株,部分杆菌在显微镜下的菌体形态见图1。
表1 海鱼肠道菌株的镜检及过氧化氢酶试验结果
Table 1 Microscopic examination of intestinal strains of sea fish and results of catalase test

试验 编号 G+/G- 接触酶试验B1-1 G+ 阴性(-) S3-1 G+ 阴性(-)B1-2 G+ 阴性(-) S3-2 G+ 阴性(-)B2-3 G+ 阴性(-) S2-3 G+ 阴性(-)B2-4 G+ 阴性(-) S2-4 G+ 阴性(-)B2-5 G+ 阴性(-) S2-5 G+ 阴性(-)B2-6 G+ 阴性(-) S2-6 G+ 阴性(-)B2-7 G+ 阴性(-) S2-7 G+ 阴性(-)B2-8 G+ 阴性(-) S2-8 G+ 阴性(-)B2-9 G+ 阴性(-) S2-9 G+ 阴性(-)B2-10 G+ 阴性(-) S2-10 G+ 阴性(-)B2-11 G+ 阳性(+) Y3-1 G+ 阴性(-)H3-1 G+ 阴性(-) Y3-2 G+ 阴性(-)H2-2 G+ 阴性(-) Y2-3 G+ 阴性(-)H2-3 G+ 阴性(-) Y2-4 G+ 阴性(-)H2-4 G+ 阴性(-) Y2-5 G+ 阴性(-)H2-5 G+ 阴性(-) Y2-6 G+ 阴性(-)H2-6 G+ 阴性(-) Y2-7 G+ 阴性(-)H2-7 G+ 阴性(-) Y2-8 G+ 阴性(-)H2-8 G+ 阴性(-) Y2-9 G+ 阴性(-)H2-9 G+ 阴性(-) Y2-10 G+ 阴性(-)H2-10 G+ 阴性(-)编号 G+/G- 接触酶
2.2 高抑菌性乳杆菌的筛选乳杆菌发酵液对大肠杆菌的抑菌效果见表2。
由表2可看出,从梭鱼肠道中分离得到的菌株S2-6 抑菌作用最为明显,抑菌圈直径达到了14.77 mm,而菌株S3-2 拮抗作用较弱,抑菌圈直径只有8.64 mm,而菌株S2-4,Y3-1,B2-3,B2-4,B2-10 和H2-4 也表现出较强的抑菌效果,其余菌株的抑菌直径则没有超过12.50 mm。整个试验过程均以无细胞发酵上清液来作为抑菌物质,结果表现出了一定程度的抑菌性,表明抑菌物质主要存在于菌株的无细胞代谢产物中,这一结果与苟小兰等[11]的研究结果相类似,都表明乳酸菌的抑菌物质主要存在于代谢产物中,菌体本身并没有抑菌作用。从梭鱼中选出的S2-4,S2-6,鸦片鱼中选出Y3-1,鲅鱼中选出B2-4,B2-10 和海鱼H2-4 作为抑菌性较强的高抑菌性乳杆菌菌株,进行后续的研究菌株。
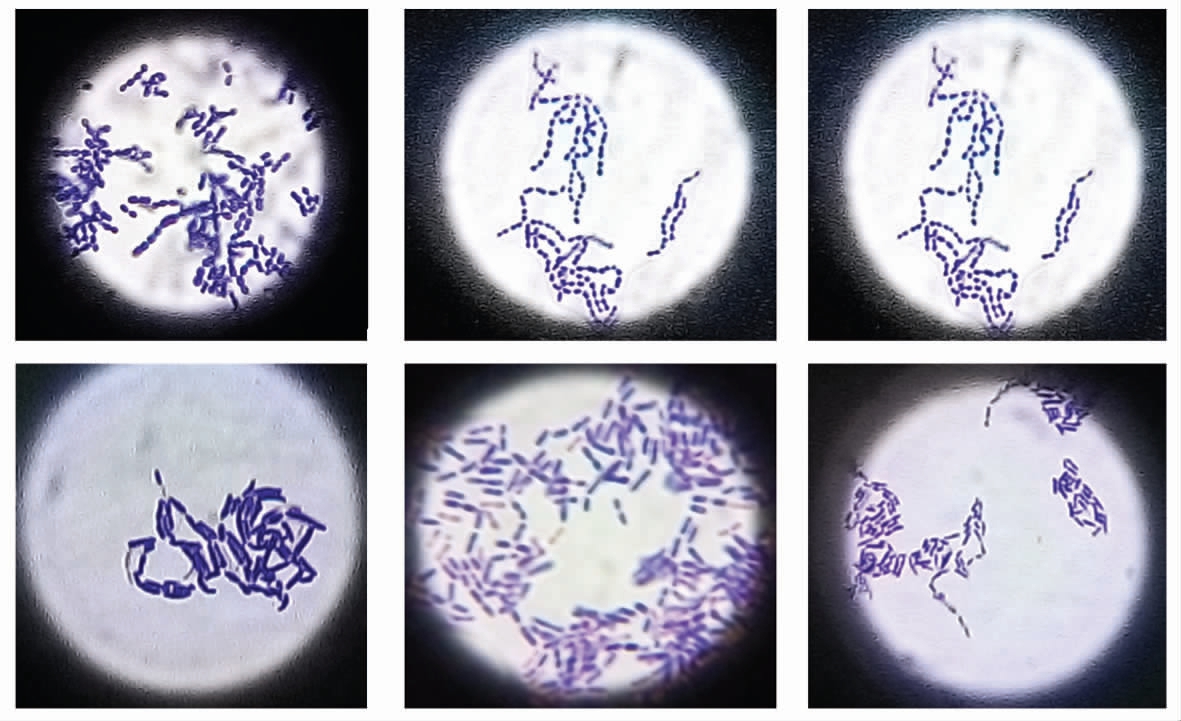
图1 几株杆菌在显微镜下的菌体状态
Fig.1 The bacterial status of several strains of bacteria under the microscope
表2 16株乳杆菌发酵液对大肠杆菌的抑菌效果
Table 2 Antibacterial effect of 16 Lactobacillus fermentation broth on Escherichia coli
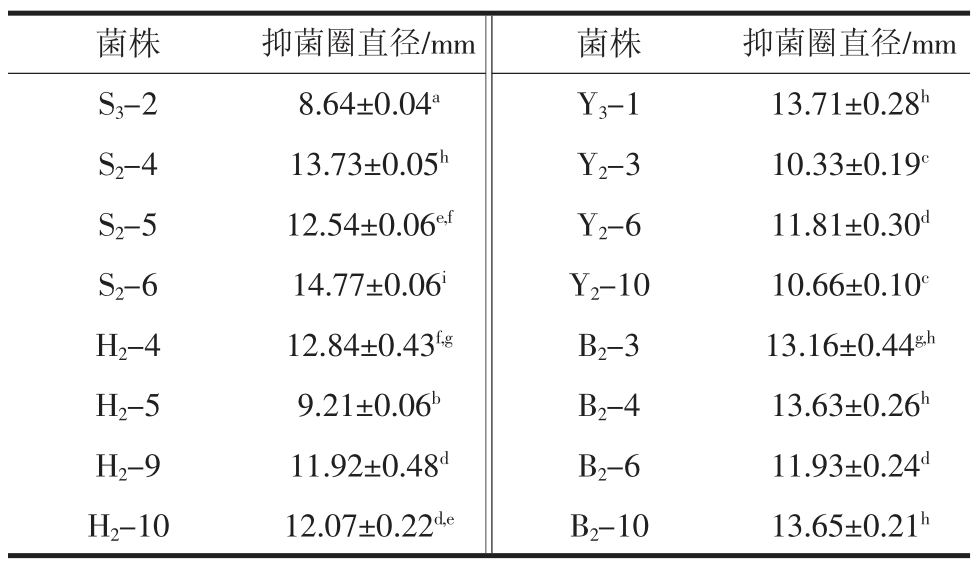
注:表内抑菌圈直径为3 次试验的平均值±标准误差且包括牛津杯外直径(8 mm);不同字母代表数据间差异显著(P<0.05)。
菌株 抑菌圈直径/mm 菌株 抑菌圈直径/mm S3-2 8.64±0.04a Y3-1 13.71±0.28h S2-4 13.73±0.05h Y2-3 10.33±0.19c S2-5 12.54±0.06e,f Y2-6 11.81±0.30d S2-6 14.77±0.06i Y2-10 10.66±0.10c H2-4 12.84±0.43f,g B2-3 13.16±0.44g,h H2-5 9.21±0.06b B2-4 13.63±0.26h H2-9 11.92±0.48d B2-6 11.93±0.24d H2-10 12.07±0.22d,e B2-10 13.65±0.21h
2.3 高抑菌性乳杆菌的抑菌试验
采用同样的方法研究了筛选出的6株乳杆菌对金黄色葡萄球菌、志贺氏菌、单增李斯特菌、副溶血性弧菌和沙门氏菌这五种指示菌的拮抗效果。试验中同样将指示菌的菌密度控制为OD600=0.4±0.05,结果发现这6株乳杆菌对所有选取的食品腐败菌都有一定的拮抗作用,抑菌圈直径大小见表3。
表3 乳杆菌发酵液对拮抗菌株的抑菌效果
Table 3 Antibacterial effect of Lactobacillus fermentation broth on antagonistic strains
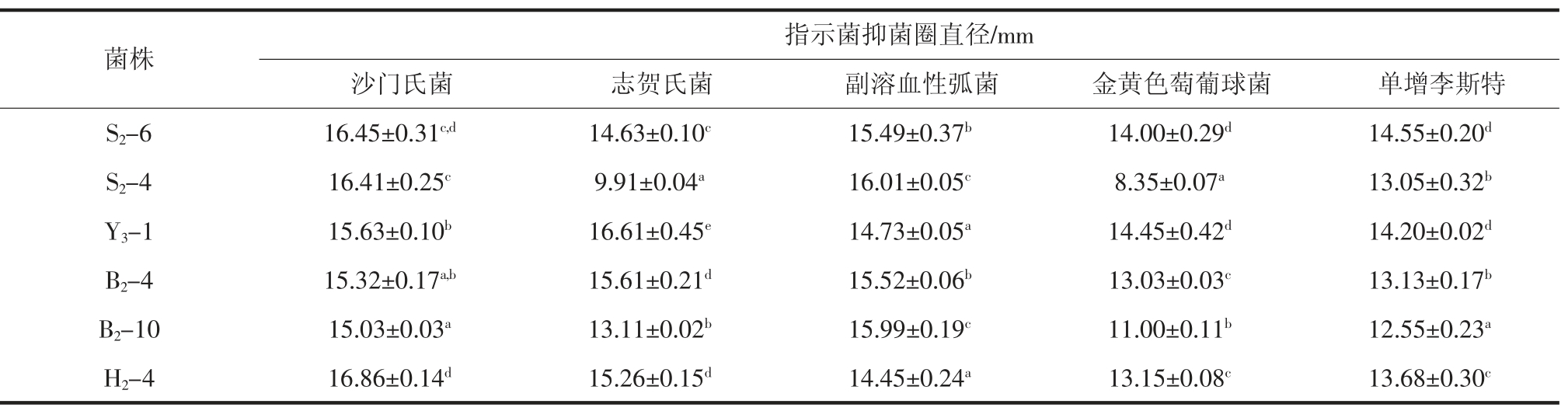
注:表内抑菌圈直径为3 次试验的平均值±标准误差且包括牛津杯外直径(8 mm);不同字母代表数据间差异显著(P<0.05)。
菌株 指示菌抑菌圈直径/mm沙门氏菌 志贺氏菌 副溶血性弧菌 金黄色萄葡球菌 单增李斯特S2-6 16.45±0.31c,d 14.63±0.10c 15.49±0.37b 14.00±0.29d 14.55±0.20d S2-4 16.41±0.25c 9.91±0.04a 16.01±0.05c 8.35±0.07a 13.05±0.32b Y3-1 15.63±0.10b 16.61±0.45e 14.73±0.05a 14.45±0.42d 14.20±0.02d B2-4 15.32±0.17a,b 15.61±0.21d 15.52±0.06b 13.03±0.03c 13.13±0.17b B2-10 15.03±0.03a 13.11±0.02b 15.99±0.19c 11.00±0.11b 12.55±0.23a H2-4 16.86±0.14d 15.26±0.15d 14.45±0.24a 13.15±0.08c 13.68±0.30c
从表3中可以看出菌株S2-6 和Y3-1 的抑菌效果最好,对金黄色葡萄球菌、志贺氏菌、单增李斯特菌、副溶血性弧菌和沙门氏菌这五种食品腐败菌均有较强的抑制效果且抑菌圈直径都大于14 mm,其中菌株S2-6对沙门氏菌的抑菌圈直径最大达到了16.45 mm,菌株Y3-1 对志贺氏菌的抑菌圈直径也达到了16.61 mm。此外菌株B2-4 对沙门氏菌,志贺氏菌和副溶血性弧菌3种革兰氏阴性菌抑菌效果较好,抑菌圈直径分别达到15.32、15.61、15.52 mm,对另外两株革兰氏阳性菌株的抑菌圈直径则在13.00 mm 左右,因此菌株B2-4 对革兰氏阴性菌的抑菌性能可能要强于革兰氏阳性菌。虽然每株杆菌产生的抑菌物质可能相同,对不同的指示菌,6株乳杆菌会表现出不同的抑制效果,6株乳杆菌都对沙门氏菌和副溶血性弧菌有较强的抑菌效果,其抑菌圈直径都较其它食品腐败指示菌大,平均直径都在15.00 mm 左右。但是菌株S2-4 对志贺氏菌和金黄色葡萄球菌的抑菌作用却不是很明显,抑菌圈直径只有9.91 mm 和8.35 mm,都没有超过10 mm。
2.4 乳杆菌代谢产物抑菌物质的研究
2.4.1 排除有机酸试验
乳杆菌在代谢过程中可产生有机酸,有机酸可能是抑菌的主要物质,试验中将6株杆菌传代培养并离心获得上清后,测得其上清液pH值均在3.5~4.0 之间,之后用1 mol/L 的NaOH 中和上清液代谢产物中的有机酸,将pH值调至空白MRS 的pH值,同时用未调pH值的上清液作为对照,进行抑菌试验,如表4。
表4 排除有机酸试验的抑菌效果
Table 4 Eliminate the antibacterial effect of organic acid test

注:+表示出现抑菌圈;-表示未出现抑菌圈。
大肠杆菌抑菌圈试验S2-6 上清液 + +S2-6 碱中和上清液--S2-4 上清液 + +S2-4 碱中和上清液--Y3-1 上清液 + +Y3-1 碱中和上清液--B2-4 上清液 + +B2-4 碱中和上清液--B2-10 上清液 + +B2-10 碱中和上清液--H 2-4 上清液 + +H 2-4 碱中和上清液--抑菌物质 金黄色葡萄球菌抑菌圈试验
表4表明,所有经过中和有机酸后的试验组,无论对大肠杆菌还是金黄色葡萄球菌均未产生明显的抑菌圈,而未经中和的上清液均显示出抑菌圈。这说明乳杆菌发酵上清液中可能是代谢产生的有机酸在充当抑菌物质,Vazquez 等研究9 株不同来源的乳酸菌对致病菌有抑制作用,认为乳酸菌主要通过分泌乳酸、乙酸等有机酸来抑制病原菌的生长[21]。上清液中还可能存在一些特殊细菌素,它们只在酸性条件下发挥抑菌作用,因而未能在上述试验条件下表现出抑菌效果,所以要用能在酸性条件下发挥作用的胃蛋白酶处理上清液以验证是否有细菌素的存在。
2.4.2 蛋白酶敏感性试验
试验过程中通过对乳杆菌发酵上清液进行蛋白酶处理,来验证上清液抑菌物质中是否含有蛋白类细菌素。排除有机酸试验已经说明本试验只需要使用胃蛋白酶对发酵上清液进行酶解,检测酶处理后的上清液是否还有抑菌能力,蛋白酶敏感性试验结果见表5。
表5 排除乳杆菌发酵液中蛋白后的抑菌效果
Table 5 Antibacterial effect of removing protein from Lactobacillus fermentation broth
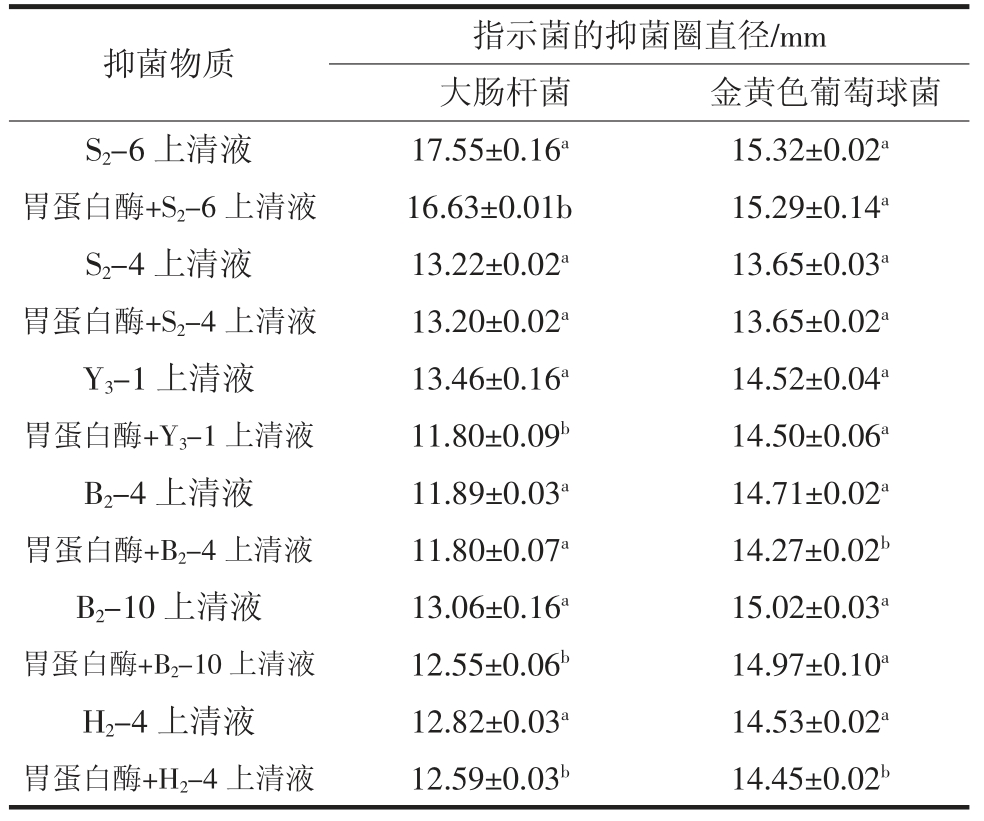
注:表内抑菌圈直径为3 次试验的平均值±标准误差且包括牛津杯外直径(8 mm);不同字母代表数据间差异显著(P<0.05)。
抑菌物质 指示菌的抑菌圈直径/mm大肠杆菌 金黄色葡萄球菌S2-6 上清液 17.55±0.16a 15.32±0.02a胃蛋白酶+S2-6 上清液 16.63±0.01b 15.29±0.14a S2-4 上清液 13.22±0.02a 13.65±0.03a胃蛋白酶+S2-4 上清液 13.20±0.02a 13.65±0.02a Y3-1 上清液 13.46±0.16a 14.52±0.04a胃蛋白酶+Y3-1 上清液 11.80±0.09b 14.50±0.06a B2-4 上清液 11.89±0.03a 14.71±0.02a胃蛋白酶+B2-4 上清液 11.80±0.07a 14.27±0.02b B2-10 上清液 13.06±0.16a 15.02±0.03a胃蛋白酶+B2-10 上清液 12.55±0.06b 14.97±0.10a H2-4 上清液 12.82±0.03a 14.53±0.02a胃蛋白酶+H2-4 上清液 12.59±0.03b 14.45±0.02b
由表5可以看出菌株S2-6、Y3-1 和B2-10 经胃蛋白酶处理后的发酵上清液对大肠杆菌的抑菌圈显著变小(P<0.05),对金黄色葡萄球菌抑菌效果不明显,而菌株S2-4 在处理前后对两种致病菌的抑菌效果均不明显;经蛋白酶处理后的菌株H2-4 对两种致病菌均有显著的抑菌效果(P<0.05),推测H2-4 可能为一种产广谱蛋白类抑菌物质的乳酸菌株,其抑菌结果如图2.5所示。虽然初步判定出了这几株杆菌产生抑菌物质,但是菌株产生的蛋白类抑菌物质需要进一步的分离纯化,其结构及理化性质也有待于进一步深入的研究,以方便人们对海洋源乳酸菌蛋白类抑菌物质的开发和利用,推动细菌素在食品保鲜方面的应用。
2.5 乳杆菌菌株的鉴定
本试验所分离的乳杆菌株均委托上海生工生物工程技术服务有限公司进行细菌的16S rDNA 序列测定。6株菌株的相似性及NCBI 登录号如表6所示。
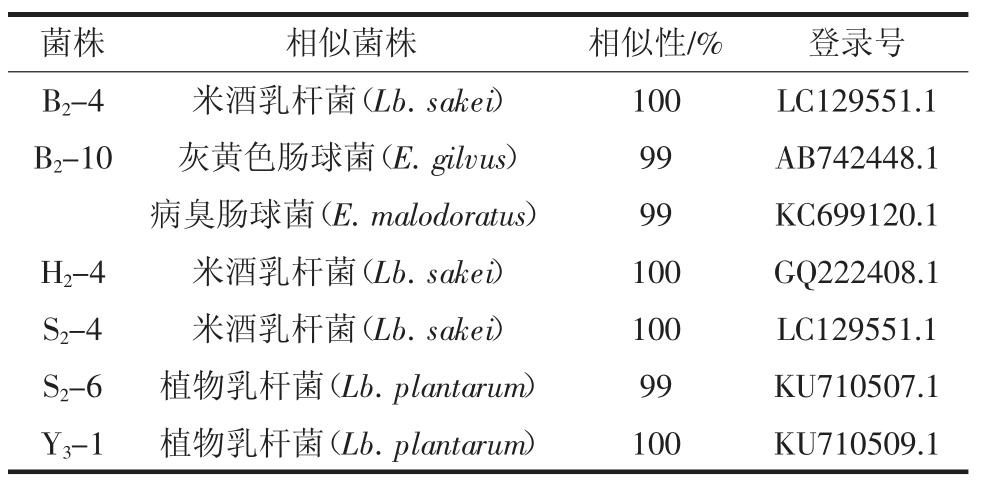
表6 6株乳杆菌株的NCBI 参考结果
Table 6 NCBI reference results of 6 strains of Lactobacillus
菌株 相似菌株 相似性/% 登录号B2-4 米酒乳杆菌(Lb. sakei) 100 LC129551.1 B2-10 灰黄色肠球菌(E. gilvus) 99 AB742448.1病臭肠球菌(E. malodoratus) 99 KC699120.1 H2-4 米酒乳杆菌(Lb. sakei) 100 GQ222408.1 S2-4 米酒乳杆菌(Lb. sakei) 100 LC129551.1 S2-6 植物乳杆菌(Lb. plantarum) 99 KU710507.1 Y3-1 植物乳杆菌(Lb. plantarum) 100 KU710509.1
由表6可知,菌株B2-4、H2-4、S2-4 被鉴定为米酒乳杆菌(Lactobacillus sakei),菌株S2-6 和Y3-1 被鉴定为植物乳杆菌(Lactobacillus plantarum)。但是从鲅鱼肠道分离的B2-10 却被鉴定为灰黄色肠球菌(Enterococcus gilvus)或 病 臭 肠 球 菌(Enterococcus malodoratus),这两株菌都属于同种的鸟肠球菌群。
现筛选的菌株B2-10 被鉴定为肠球菌属(Enterococcus)细菌,该属细菌也是革兰氏阳性、无芽孢的过氧化氢酶试验阴性菌,但是肠球菌不属于本试验旨在筛选的乳杆菌属细菌,造成这一结果的主要原因是由于肠球菌属细菌多为圆形或椭圆形,成对或短链状排列,并且一些细菌可能处于分裂状态,其形态易与短杆菌相混淆,以致镜检时将其误认为是乳杆菌属细菌,现将其纠正为肠球菌属细菌。
周伟等[12]发现植物乳杆菌素L-1 能抑制单增李斯特菌的生长,不过近几年发现一些植物乳杆菌素也能抑制革兰氏阴性菌的生长。这和本试验发现的S2-6 和Y3-1 两株植物乳杆菌对革兰氏阴性菌大肠杆菌有抑制作用结果相一致,洪伟等[13]也曾从腌菜中分离出一株能拮抗大肠杆菌的植物乳杆菌,董雪凤等[20]也认为乳酸菌对大肠杆菌有明显的抑制作用,其抑制作用的强弱与乳酸菌活力和大肠杆菌的浓度有关,这些结果为今后深入的研究和利用植物乳杆菌素奠定了一定的基础。此外本试验还从鲅鱼、黄鱼和梭鱼肠道中各分离出了一株米酒乳杆菌,编号依次为B2-4、H2-4 和S2-4。米酒乳杆菌主要分布在酸泡菜[14]、发酵面团、发酵香肠[15]等发酵食品中,本试验从海鱼肠道中分离出米酒乳杆菌实在为少见。但是关于米酒乳杆菌素C2 的研究却很多[12,16],刘晓燕等[17]研究发现米酒乳杆菌素C2除了具有很好的稳定性外,还能对金黄色葡萄球菌起到抑制作用,这与本试验分离得到米酒乳杆菌B2-4 性质极为相似。
3 结论
本试验从梭鱼和鸦片鱼肠道中各分离出一株植物乳杆菌S2-6 和Y3-1,能够在代谢中产生蛋白类抑菌物质,可抑制大肠杆菌的生长;从海鱼中获得的米酒乳杆菌H2-4 产生的细菌素对大肠杆菌和金黄色葡萄球菌均产生抑制效果,因此推测其可能是一株产广谱细菌素的米酒乳杆菌,而这些细菌素也需要于进一步深入的研究和纯化。从海鱼中分离具有广谱抑菌性能的乳酸菌,可作为潜在的生物保鲜剂应用于海洋鱼类的保鲜。
[1]高彦祥.食品添加剂[M].北京:中国轻工业出版社,2011:34-50
[2]Harris L J,Daeschel M A,Stiles M E,et al.Antimicrobial activity of lactic acid bacteria against Listeria monocytogenes[J].J Food Prot,1989,52(6):384-387
[3]李平兰,张篪,江汉湖.乳酸菌细菌素研究进展[J].微生物学通报,1998,25(5):295-298
[4]李晓婷,陈忠军.具有抑霉菌作用乳杆菌抑菌物质特性研究[J].食品科技,2017(1):18-22
[5]杜琨.青海牧民酸奶中乳酸菌产抑菌物质对冷却猪肉保鲜效果研究[J].东北农业科学,2018,43(1):41-44
[6]马欢欢,林洋,吕欣然,等.96 孔板法筛选抗黑曲霉性乳酸菌及抑菌机理研究[J].食品工业科技,2017,38(12):171-175
[7]杜连祥,路福平.微生物学实验技术[M].北京: 中国轻工业出版社,2011:160-161
[8]刘冬梅,李理,杨晓泉,等.用牛津杯法测定益生菌的抑菌活力[J].食品研究与开发,2006(3):110-111
[9]张子健,刘玉恩,赵谦,等.植物乳杆菌C8—1 产类细菌素的初步研究[J].中国乳品工业,2010,38(1):15-18
[10]武运,李远,王冰峰,等.新疆酸驼乳中细菌素乳酸菌的筛选及其抑菌性[J].食品与机械,2011,27(3):25-28
[11]苟小兰,苏艳秋,石锐,等.鱼源乳酸菌对水产病原菌的抑制作用研究[J].水产科学,2015,34(9):575-579
[12]周伟,刘国荣,李平兰,等.植物乳杆菌素L-1 对单核细胞增生李斯特氏菌作用机理的研究[J].微生物学报,2007(2):260-264
[13]洪伟,薛正莲.1 株植物乳杆菌的抑菌作用及其生物学特性的研究[J].生物学杂志,2014(6):51-54
[14]顾双,王向阳,俞兴伟,等.泡菜中产气乳酸菌分离鉴定研究[J].中国调味品,2016(1):1-2
[15]林伟涛,徐世明,刘蓉宏,等.中式发酵香肠菌种的分离筛选和初步鉴定[J].烟台大学学报(自然科学与工程版), 2008(2): 99-104
[16]盛艳,高玉荣.产广谱细菌素米酒乳杆菌C2 发酵培养基的研究[J].黑龙江八一农垦大学学报,2009,21(4):76-80
[17]刘晓燕,李大鹏.米酒乳杆菌素C2 生物稳定性的研究[J].中国食品添加剂,2010(4):66-70
[18]赵耀,李玲,刘飞扬,等.产广谱乳酸菌素乳酸菌的选育[J].安徽农学通报,2017,23(11):58-59,91
[19]刘君,林俊芳,郭丽琼,等.水产源乳酸菌的多样性及抑菌活性研究[J].水产科学,2015,34(6):351-357
[20]董雪凤,杨子彪,任发政.乳酸菌与大肠杆菌相互作用的研究[J].中国乳业,2013(3):54-56
[21]Vázquez J A,González M P,Murado M A. Effects of lactic acid bacteria cultures on pathogenic microbiota from fish [J]. Aquaculture,2005,245(1):149-161
[22]刘佳秀,查振兴,于文溪,等.海洋源乳酸菌在黄花鱼肉保鲜中的应用研究[J].食品科学技术学报,2018,36(6):1-9