辣椒是世界上仅次于豆类、番茄的第三大蔬菜作物,在我国种植规模大、产品类别多样、市场需求高,是我国最大的蔬菜产业。辣椒中含有丰富的辣椒红素、辣椒素、维生素、矿物质等,具有很高的保健功能和营养价值,有抗菌消炎、抗氧化、降低胆固醇、溶解血栓等方面的功效能增,为重要的蔬菜和调味品[1-2]。
咪鲜胺是一种咪唑类广谱高效杀菌剂,其作用机理主要通过抑制麦角甾醇的生物合成,破坏细胞膜结构功能,从而达到杀菌目的,对辣椒枯萎病菌引起病害具有很好的保护和治疗作用,用于防治辣椒的枯萎病[3-4]。咪鲜胺在环境中首先降解为N-丙基-N-[2-(2,4,6-trichlorophenol,2,4,6-三氯苯氧基)乙基]脲(BTS44595)和 N-醛基-N-丙基-N-[2-(2,4,6-三氯苯氧基)乙基]脲(BTS44596),后降解为 BTS45186[5-6],即 2,4,6-三氯苯酚(2,4,6-TCP)。根据国内外研究咪鲜胺的毒性[7],咪鲜胺毒性较低,在推荐使用剂量范围内,其对哺乳动物的致突变作用、致癌作用以及致畸作用的危害较小。但2,4,6-TCP 作为咪鲜胺的最终降解物,已经被确定为我国水体中的优先污染物,是一种具有毒性、致突变性和致癌性的环境污染物,会对人类的健康造成潜在威胁[8],其残留问题受到越来越多的关注。
国内外对于咪鲜胺和2,4,6-TCP 检测的前处理,样品提取液在210 ℃~240 ℃条件下与吡啶盐酸盐发生水解反应,将咪鲜胺及其代谢物全部转化为2,4,6-TCP,经石油醚提取后采用磺化法净化,检测2,4,6-TCP 的含量[9-11]。该方法操作复杂费时,且吡啶盐酸盐毒性较大,对试验人员的健康和环境安全造成威胁。QuEChERS(quick、easy、cheap、effective、rugged、safe)为这一问题提供了新的解决途径,该方法利用N-丙基乙二胺(primary secondary amine,PSA)去除组份中的色素和油脂,以无水硫酸镁去除水分,适用于辣椒中咪鲜胺和2,4,6-TCP 农药残留的提取和净化,是一种快速、简单、便宜、可靠和安全的样品前处理方法[12]。目前,对咪鲜胺和2,4,6-TCP 的检测方法有气相色谱法(gas chromatography,GC)[13],液相色谱法(lliquid chromatography,LC)[14],气相色谱-质谱联用法(gas chromatogarphy-mass spectrometry,GC-MS)[15],液相色谱-质谱联用法(liquid chromatography-mass spectrometry,LC-MS)[16-17]等,主要涉及到样品有水果[18]、谷物[19]、油料作物[20]、中药材[21]和土壤[22]等,而对辣椒中咪鲜胺和2,4,6-TCP 残留的研究尚无报道。
本文建立了QuEChERS-气相色谱-质谱连用测定辣椒中咪鲜胺和2,4,6-TCP 残留的方法,具有对咪鲜胺和2,4,6-TCP 精密度好、准确度高、溶剂使用量少、样品制备过程简单和分析成本廉价的优点。能够对低浓度的咪鲜胺和2,4,6-TCP 进行定性与定量分析,填补了辣椒中咪鲜胺和2,4,6-TCP 残留检测研究中的空白。
1 材料与方法
1.1 材料与试剂
无水硫酸镁(分析纯,使用前650 ℃下灼烧4 h,备用):天津市凯信化学工业有限公司;乙酸钠(分析纯):天津市光复精细化工研究院;PSA:天津博纳艾杰尔科技有限公司;冰乙酸(分析纯):国药集团化学试剂有限公司;甲醇、乙腈(色谱纯):北京百灵威科技有限公司;甲醇中咪鲜胺溶液标准物质(25165XM,纯度98.4%,浓度为 100 μg/mL)、甲醇中 2,4,6-TCP 溶液标准物质(26233XM,纯度 99.5 %,浓度为 100 μg/mL):北京振翔科技有限公司。
1.2 仪器与设备
7890A-5975C 气相色谱-质谱联用仪:美国安捷伦科技有限公司;VORTEX genius3 涡旋混合器:艾卡(广州)仪器设备有限公司;RJ-TDL-60B 离心机:无锡市瑞江分析仪器有限公司;JJ500 电子天平:常熟市双杰测试仪器厂。
1.3 条件
1.3.1 气相色谱条件
DB-1701 石英毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度260℃;升温程序:初始温度60℃保持1 min,以 10 ℃/min 升至 280 ℃,保持 10 min;进样量 1.0 μL,不分流进样。
1.3.2 质谱条件
EI 电离源,电离电压70 eV;离子源温度280 ℃;传输线温度280 ℃;溶剂延迟:5 min;咪鲜胺选择监测离子:定量离子 m/z 180;定性离子 m/z 308、266。2,4,6-TCP 选择监测离子:定量离子 m/z 196;定性离子 m/z 198、132。
1.4 样品处理
称取10.00 g 样于50 mL 离心管,加10 mL 乙腈-乙酸(99 ∶1,体积比),摇匀,加 3.0 g 无水硫酸镁,1.0 g乙酸钠,涡旋1 min,4 000 r/min 离心5 min。取上清液5 mL 于15 mL 离心管,加1.0 g 无水硫酸镁PSA量(3 ∶1,质量比),涡旋 1 min,4 000 r/min 离心 5 min,取1 mL 上清液过膜,待测。
1.5 标准溶液的配制
分别准确移取 1 mL 100 μg/mL 的咪鲜胺和2,4,6-TCP 标准品溶液至10 mL 容量瓶中,用甲醇定容,配成两种10.0 μg/mL 的标准储备液,分别吸取以上两种标准储备液适量,并用样品提取液稀释至质量浓度为0.01、0.02、0.05、0.1、0.2、0.5、1.0 μg/mL 系列混合标准溶液。
2 结果与分析
2.1 提取溶剂的选择
选用丙酮、乙腈、乙腈-乙酸作为提取溶剂进行比较。在辣椒中添加 0.1 μg/mL 咪鲜胺和 2,4,6-TCP 标准溶液测定其回收率见表1。
表1 辣椒中咪鲜胺和2,4,6-TCP 在0.1 μg/mL 添加水平下的回收率及其相对标准偏差(relative standard deviation,RSD)
Table 1 Recoveries and the relative standard deviation(RSD)of prochloraz and 2,4,6-TCP at 0.1 μg/mL spiked in pepper

样品 溶剂回收率/% RSD/%1 2 3 4 5辣椒 丙酮 2,4,6-TCP 84.93 87.54 80.66 79.27 82.20 4.01咪鲜胺 94.55 100.26 98.31 95.78 102.79 3.39乙腈 2,4,6-TCP 86.20 81.47 83.94 87.72 82.51 3.06咪鲜胺 97.55 99.85 101.33 98.58 100.42 1.50乙腈-乙酸 2,4,6-TCP 96.92 103.36 99.17 105.25 97.99 3.77咪鲜胺 105.21 99.88 103.31 105.55 98.93 3.10
由表1可知,咪鲜胺在丙酮、乙腈、乙腈-乙酸中回收率在94.55%~105.55%之间,三者对咪鲜胺均有较好的提取效果。2,4,6-TCP 在丙酮和乙腈中回收率为79.27 %~87.72 %之间,在乙腈-乙酸中回收率为96.92%~105.25%,说明 2,4,6-TCP 在乙腈-乙酸提取效率比乙腈好。这是由于2,4,6-TCP 具有较强的极性和酸性,其羟基上的H+与环境中的Na+进行交换从而生成 2,4,6-三氯苯酚钠,而 2,4,6-三氯苯酚钠在水相中的溶解度大于在有机相中的溶解度,有机相无法对样品基质中的2,4,6-三氯苯酚钠进行有效提取,加入乙腈-乙酸,存在大量的H+,促进样品基质中2,4,6-三氯苯酚钠形成 2,4,6-TCP,从而提高提取效率,2,4,6-TCP 与 2,4,6-三氯苯酚钠的转化见图1。

图1 2,4,6-TCP 与 2,4,6-三氯苯酚钠的转化
Fig.1 The transformation of 2,4,6-TCP and 2,4,6-trichlorophenosodiumsalt
因此,本研究选择乙腈-乙酸作为咪鲜胺和2,4,6-TCP 的提取剂。
2.2 无水硫酸镁PSA用量的优化
本研究选用无水硫酸镁PSA 量净化提取液,PSA对多糖、肽类(包括氨基酸)和色素有强吸附作用,无水硫酸镁去除提取液中少量的水分,有助于加强PSA的净化效果。考察不同用量的无水硫酸镁PSA 量对净化效率的影响见表2,按1.4 过程在辣椒中添加0.10 μg/mL 咪鲜胺和 2,4,6-TCP 混合标准溶液,分别以 0.2、0.5、1.0、1.5、2.0 g 无水硫酸镁 PSA 量净化提取液,观察不同用量的无水硫酸镁PSA 对提取液的净化效果。试验结果显示,随3 ∶1 的无水硫酸镁PSA 用量增加对提取液净化效果越好。
表2 辣椒中在0.10 μg/mL 添加水平下不同量3 ∶1 的无水硫酸镁PSA 对平均回收率的影响(n=5)
Table 2 Effects of amount of anhydrous magnesium sulfate PSA(3 ∶1,m/m)on average recoveries of 0.10 μg/mL spiked in pepper(n=5)

无水硫酸镁PSA 量/g 平均回收率/%咪鲜胺 2,4,6-TCP 0.2 83.39 85.51 0.5 88.49 89.76 1.0 98.40 99.14 1.5 98.13 98.98 2.0 97.77 98.22
由表2可知,当无水硫酸镁和PSA 的量达到1.0 g后2,4,6-TCP 和咪鲜胺回收率基本不变。综合净化效果和回收率,本研究选择1.0 g 无水硫酸镁PSA 量净化提取液。
2.3 线性范围和检出限
取1.4 配制的咪鲜胺和2,4,6-TCP 标准混合工作液,在最佳的试验条件下检测咪鲜胺和2,4,6-TCP,以进样质量浓度为横坐标、峰面积为纵坐标见图2。

图2 咪鲜胺和2,4,6-TCP 标准曲线
Fig.2 The standard curve of the prochloraz and 2,4,6-TCP
得到咪鲜胺和2,4,6-TCP 的线性方程分别为Y=637 497.3X-8 786.1 和 Y=890 775.9X-3 978.6,其相关系数r 值分别为0.999 1 和0.999 2,表明咪鲜胺和2,4,6-TCP 在 0.01 μg/mL~1.0 μg/mL 范围内的线性关系均良好,以3 倍信噪比(S/N=3)确定咪鲜胺和2,4,6-TCP 检出限为 0.003 3 mg/kg,满足残留定量分析要求。
2.4 回收率和精密度
试验对辣椒进行了加标回收试验,考察该方法的回收率与精密度。按照1.5 步骤对辣椒添加0.02、0.10、0.50 μg/mL 3 个水平的咪鲜胺和 2,4,6-TCP 标准溶液,经前处理后GC-MS 分析,测定后计算回收率见表3。
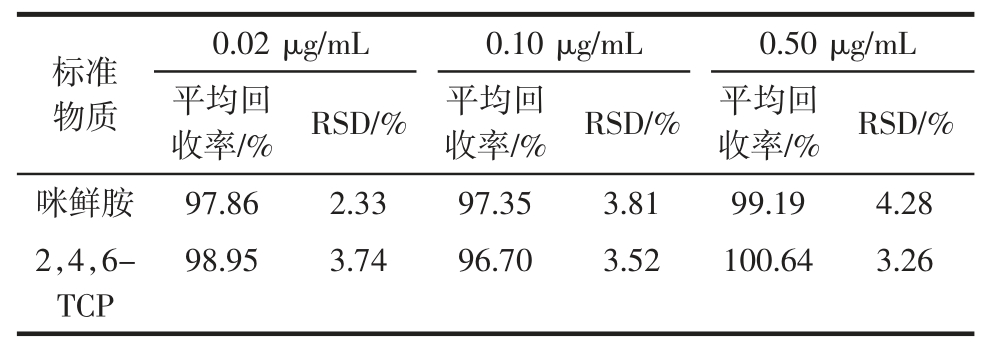
表3 辣椒中咪鲜胺和2,4,6-TCP 在3 个添加水平下的平均回收率及其相对标准偏差(n=7)
Table 3 Average recoveries and the RSD of prochloraz and 2,4,6-TCP at three spiked levels in pepper(n=7)
标准物质 收率/% RSD/% 平均回0.02 μg/mL 0.10 μg/mL 0.50 μg/mL平均回images/BZ_105_1662_1471_1684_1501.png收率/% RSD/% 平均回收率/% RSD/%images/BZ_105_1936_1471_1957_1501.png咪鲜胺 97.86 2.33 97.35 3.81 99.19 4.28 2,4,6-TCP 98.95 3.74 96.70 3.52 100.64 3.26
由表3可知,在3 个添加水平下咪鲜胺和2,4,6-TCP 的平均回收率在96.70%~100.64%的范围之间,相对标准偏差(relative standard deviation,RSD)介于2.33%~4.28%之间,表明此方法具有较高的准确度和精密度。因此,试验中开发的方法满足2,4,6-TCP 和咪鲜胺分析的要求,可用于辣椒样品中2,4,6-TCP 和咪鲜胺农药残留的检测。
2.5 实样分析
利用本试验方法按1.5 样品处理步骤,以市售的辣椒50 个样品进行定性定量分析见表4。
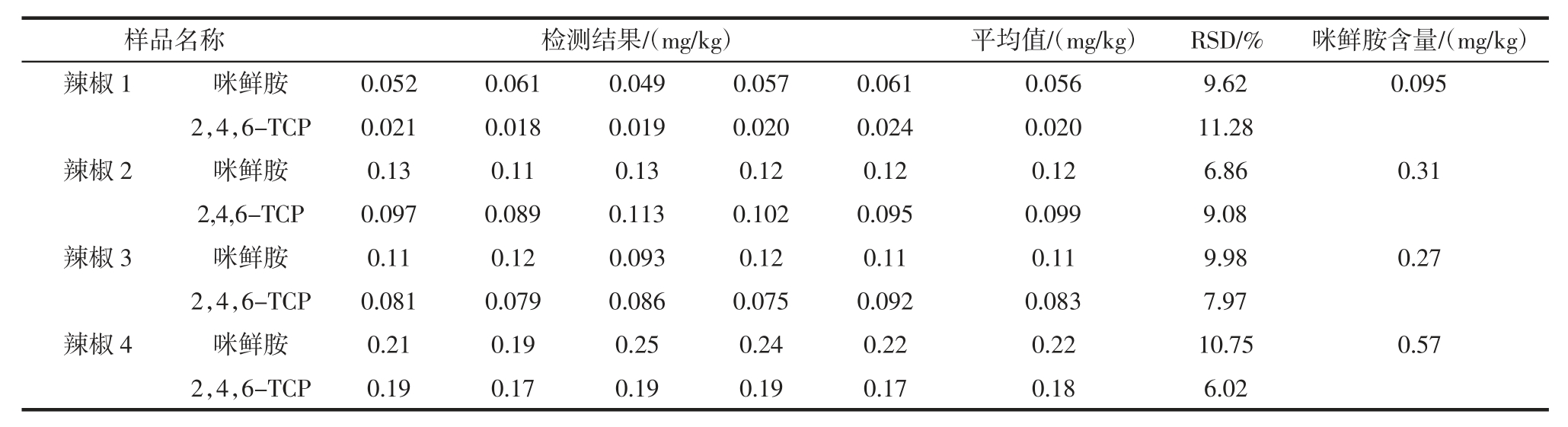
其中 4 个样品检出咪鲜胺和 2,4,6-TCP 残留,结果见表4,其余样品均未检出,对检出样品做5 次平行检测,咪鲜胺和2,4,6-TCP 分别在0.049 mg/kg~0.25 mg/kg 和 0.018 mg/kg~0.19 mg/kg 之间,相对标准偏差在6.02%~11.28%之间。
表4 实样检测结果
Table 4 Sample test results
样品名称检测结果/(mg/kg)平均值/(mg/kg)RSD/%咪鲜胺含量/(mg/kg)辣椒1 咪鲜胺 0.052 0.061 0.049 0.057 0.061 0.056 9.62 0.095 2,4,6-TCP 0.021 0.018 0.019 0.020 0.024 0.020 11.28辣椒2 咪鲜胺 0.13 0.11 0.13 0.12 0.12 0.12 6.86 0.31 2,4,6-TCP 0.097 0.089 0.113 0.102 0.095 0.099 9.08辣椒3 咪鲜胺 0.11 0.12 0.093 0.12 0.11 0.11 9.98 0.27 2,4,6-TCP 0.081 0.079 0.086 0.075 0.092 0.083 7.97辣椒4 咪鲜胺 0.21 0.19 0.25 0.24 0.22 0.22 10.75 0.57 2,4,6-TCP 0.19 0.17 0.19 0.19 0.17 0.18 6.02
由于咪鲜胺最终降解为2,4,6-TCP,根据水解反应的化学计量法,1 摩尔咪鲜胺(分子量为376.7)水解产生 1 摩尔的 2,4,6-TCP(分子量为 197.5),所以它们之间存在下一种转换关系[23-24]:
1(mg/kg)2,4,6-TCP=1.907(mg/kg)咪鲜胺
按照GB2763-2016《食品安全国家标准食品中农药最大残留限量规定》[25],咪鲜胺及其含有2,4,6-三氯苯酚部分的代谢产物之和,以咪鲜胺表示,根据转换关系计算4 个样品中咪鲜胺的含量在0.095 mg/kg~0.57 mg/kg 之间,在辣椒中的最终残留量均低于最大残留量2 mg/kg。
3 结论
采用QuEChERS-气相色谱-串联质谱法对蔬菜中咪鲜胺及其代谢物2,4,6-三氯苯酚残留量的检测技术进行了研究。该方法前处理简便快速、选择性好、灵敏度高、抗干扰能力强,具有良好的线性响应,且在0.02、0.10、0.50 μg/mL 添加水平下,两种农药均有较好的回收率。表明该方法符合农药残留分析的要求,适用于辣椒中咪鲜胺及其代谢物2,4,6-三氯苯酚残留检测的定性和定量分析。
[1]Mirmanto M,Syahrul S,Sulistyowati E D,et al.Effect of inlet temperature and ventilation on heat transfer rate and water content removal of red chilies[J].Journal of Mechanical Science & Technology,2017,31(3):1531-1537
[2]Shin Y H,Kim J M,Park K.The effect of capsaicin on salivary gland dysfunction[J].Molecules,2016,21(7):835-845
[3]卢俊文,李蓉,杨芳,等.气相色谱-串联质谱法快速测定水果中咪鲜胺及其代谢物2,4,6-三氯苯酚的残留量[J].食品科学,2015,36(12):213-217
[4]洪艳霞.咪鲜胺与异菌脲混配对辣椒枯萎病菌和西瓜枯萎病菌的增效作用[J].山西农业科学,2016,44(3):382-384
[5]龚道新,樊德方,杨仁斌,等.咪鲜安及其主要代谢物的紫外光谱吸收特性和对蝌蚪急性毒性的研究[J].农业环境科学学报,2003,22(6):749-753
[6]Höllrigl-Rosta A,Kreuzig R,Bahadir M.Investigations on the metabolic fate of prochloraz in soil under field and laboratory conditions[J].Pest Management Science,1999,55(5):531-538
[7]Vinggaard A M,Hass U,Dalgaard M,et al.Prochloraz:an imidazole fungicide with multiple mechanisms of action[J].International journal of andrology,2006,29(1):186-192
[8]Wiese F W,Chang H C,Lloyd R V,et al.Peroxidase-catalyzed oxidation of 2,4,6-trichlorophenol[J].Archives of environmental contamination and toxicology,1998,34(3):217-222
[9]李静,李红波,胡效亚.衍生电化学法测定橘皮中的咪酰胺[J].食品科学,2011,32(18):246-248
[10]Polese L,Jardim E F G,Navickiene S,et al.Prochloraz residue levels in ginger submitted to Sportak 450 CE postharvest treatment[J].Eclética Química,2006,31(2):59-62
[11]高洁,胡德禹,张钰萍,等.咪鲜胺及其代谢产物在橙汁中的残留检测方法研究[J].农药科学与管理,2011,32(6):35-39
[12]王建芳,李斌,赵彤,等.QuEChERS-高效液相色谱法同时检测茶鲜叶和乌龙茶中4 种农药残留[J].食品科技,2017(8):306-313
[13]Cengiz M F,Erler F,Bilgin A K,et al.Rapid and sensitive determination of the prochloraz residues in the cultivated mushroom,Agaricus bisporus (Lange) Imbach[J].Analytical Methods,2014,6(6):1970-1976
[14]贾巧莉,王明强.超高效液相色谱法测定水果中咪鲜胺残留量[J].中国酿造,2015,34(9):145-148
[15]吴琼,吕岱竹,韩丙军,等.咪鲜胺及2,4,6,-三氯苯酚在牛奶中的残留检测方法[J].山西农业科学,2017,45(6):937-939,948
[16]Blasco C,Picó Y,Manes J,et al.Determination of fungicide residues in fruits and vegetables by liquid chromatography-atmospheric pressure chemical ionization mass spectrometry[J].Journal of Chromatography A,2002,947(2):227-235
[17]Zhao P,Cao L,Ma D,et al.Translocation,distribution and degradation of prochloraz-loaded mesoporous silica nanoparticles in cucumber plants[J].Nanoscale,2018,41(10):1798-1806
[18]袁小雅,彭梓,周慧平,等.香蕉中咪鲜胺的消解动态及安全性评价[J].食品安全质量检测学报,2016,7(1):209-214
[19]程莉,董丰收,刘新刚,等.QuEChERS-超高效液相色谱-串联质谱方法快速测定小麦中的咪鲜胺残留[J].农药学学报,2009,11(3):357-361
[20]柳训才,陈平,程运斌,等.油菜体内及土壤中咪鲜胺的残留检测与消解动态[J].中国油料作物学报,2006,28(3):354-357
[21]虞淼,梁赤周,唐芬芬,等.HPLC/MS/MS 测定铁皮石斛中咪鲜胺残留[J].农药科学与管理,2016(7):34-37
[22]王燕,王春伟,高洁,等.咪鲜胺在人参和土壤中的残留动态及安全性评价[J].东北农业大学学报,2014,45(3):25-30
[23]De Paoli M,Barbina M T,Damiano V,et al.Simplified determination of combined residues of prochloraz and its metabolites in vegetable,fruit and wheat samples by gas chromatography[J].Journal of Chromatography A,1997,765(1):127-131
[24]郭筠,莫汉宏,安凤春,等.咪鲜胺及其代谢物在黄瓜和土壤中残留的分析方法[J].环境化学,2014,23(6):704-706
[25]中华人民共和国卫生和计划生育委员会,中华人民共和国农业部,国家食品药品监督管理总局.食品安全国家标准食品中农药最大残留限量:GB2763-2016[S].北京:中国标准出版社,2016