亚麻(linum usitatissimum linn)也称胡麻,是我国五大油料作物之一,我国油用亚麻(胡麻)主要分布在华北、西北等地,主产区是内蒙古、甘肃、宁夏、河北、山西、陕西和新疆,西南地区的云南等地也有种植[1-4]。亚麻饼粕属于亚麻籽榨油后的下脚料,其粗蛋白的含量高达43%左右,亚麻籽粕含有丰富的α-亚麻酸、木质素以及蛋白类等物质[5],同时也含有丰富的维生素A、维生素B、维生素E等维生素,具有很高的营养价值,可作为油料作物配合开发新营养主食品种的原料,但是亚麻饼粕通常作为动物饲料或肥料使用,存在着巨大的浪费。
植物蛋白质经蛋白酶部分水解后,可获得具有生物活性的多肽诸如抗氧化作用、降血脂、抗肿瘤、抗高血压、活化细胞免疫机能等多肽[6-9],是现代食品和医药领域最热门的研究方向,也是提升植物蛋白利用价值的主要方向。目前对于大豆、花生等原料多肽的制备工艺和功能性进行较多的研究,如周婷婷等[10]筛选制备抗氧化大豆多肽的水解酶及水解条件,从而得到高效的抗氧化大豆多肽制品;刘英丽等[11]研究确定了酶解花生粕制备抗氧化肽的最佳工艺参数。目前国内对于亚麻的研究主要集中在亚麻油脂的开发利用,而对亚麻蛋白质的研究关注较少,特别是对脱脂亚麻粉中蛋白肽的制备研究甚少。亚麻籽蛋白也是一种优良的植物蛋白[12],(以亚麻饼粕为原料,通过对不同蛋白酶的酶解效率比较,建立3.350酸性蛋白酶解亚麻籽粕制备多肽的实验室工艺,并对制备的亚麻多肽的还原能力和清除O2-·和DPPH·的能力,进行测定,显示其具有较好的体外抗氧化活性,为后续亚麻多肽饮料和功能性食品的开发提供了理论依据。
1 材料与方法
1.1 材料
胃蛋白酶(30U/mg)、胰蛋白酶(165 U/mg):Solarbio公司;木瓜蛋白酶(10万U/g)、菠萝蛋白酶(80万U/g)、537酸性蛋白酶(2.05万U/g):广西庞博生物工程有限公司;3.350黑曲酸性蛋白酶(35 000 U/g):天津市诺奥科技发展有限公司;其它试剂均为国产分析纯;亚麻籽粕:山西省农业科学院提供;苦肽(MLIPPFFVI):华大基因合成;亚麻胰蛋白酶抑制剂(LUTI)为山西大学生物技术研究所制备。
1.2 仪器与设备
QT2000自动液相色谱分离纯化层析仪:上海琪特分析仪器有限公司;Lambda 35双光束紫外可见光光度计:珀金埃尔默企业管理(上海)有限公司;D-37520高速冷冻离心机:美国Thermo Fisher Scientific公司;FD8-4T冷冻干燥仪:GOLD-SIM公司。
1.3 多肽含量和多肽得率的测定
亚麻多肽含量参照QB/T2879-2007《海洋鱼低聚肽粉测定》[13]中的三氯乙酸沉淀法测定,其中总氮采用半微量凯氏定氮法,氨基酸态氮按照GB 5009.235-2016《食品安全国家标准食品中氨基酸态氮的测定》中的甲醛滴定法测定。
多肽得率/%=(离心上清液中总氮量-离心上清液中氨基酸态氮含量)/样品中总氮量×100
1.4 亚麻蛋白粉的制备
取一定量烘干的亚麻饼粕粉按1∶30(g/mL)加入蒸馏水,用1 mol/L的氢氧化钠调pH值到9.5~10.0,在60℃的水浴中保温搅拌3 h,然后离心取上清液。沉淀物进行二次提取、离心。两次上清液合并后,用稀盐酸调pH值到4.0~4.5沉淀蛋白,并水洗两次;水洗蛋白用1 mol/L氢氧化钠调pH值到7.0,然后冷冻干燥,得到成品亚麻蛋白粉。
1.5 水解多肽蛋白酶的筛选
准确称取亚麻蛋白粉,按1∶20(g/mL)加入蒸馏水,按每克蛋白6 000 U的酶剂量分别加入木瓜蛋白酶、胰蛋白酶、胃蛋白酶、菠萝蛋白酶、537酸性蛋白酶和3.350酸性蛋白酶,在各种蛋白酶的适宜条件下水解2 h,沸水浴30 min灭酶活,离心分离(8 000 r/min,10 min),取上清液,测定多肽含量。以多肽得率为指标,筛选出最佳蛋白酶。
1.6 亚麻多肽制备工艺条件的优化
1.6.1 单因素试验
以亚麻多肽得率为评价指标,用筛选出的酶解多肽得率最高的蛋白酶做进一步的单因素试验。按料液比 1 ∶20(g/mL),考察该酶在不同酶解温度(30、40、50、60、70)、酶解 pH 值(2.0、2.5、3.0、3.5、4.0)、加酶量(3 000、4 000、5 000、6 000、7 000 U/g)和酶解时间(1、2、3、4、5 h)4个单因素条件下对多肽得率的影响。
1.6.2 正交试验
以单因素试验的试验结果为基础,在酶解温度、酶解pH值、加酶量和酶解时间,四因素三水平下做正交试验,确定多肽得率最佳的酶解条件。正交试验方案L9(34),见表1。
表1 正交试验因素水平表
Table 1 Orthogonal test factor level table
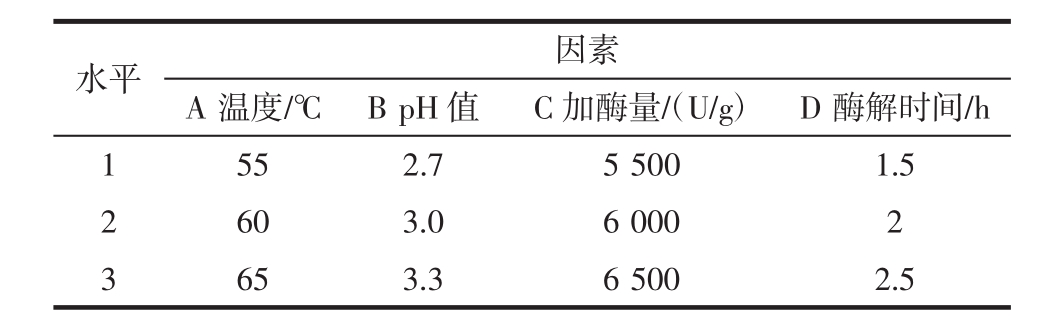
水平 因素A温度/℃B pH值C加酶量/(U/g)D酶解时间/h 1 55 2.7 5 500 1.5 2 60 3.0 6 000 2 3 65 3.3 6 500 2.5
1.7 抗氧化活性研究
还原能力的测定方法参照文献[14];DPPH·清除率的测定方法参照文献 [15-17];超氧阴离子自由基(O2-·)的清除率的测定方法参照文献[18-19]。
1.8 亚麻多肽分子量分析
利用Superdex 75 prep grade凝胶色谱法测定制备的亚麻多肽的相对分子量。以已知分子量的两种多肽,亚麻胰蛋白酶抑制剂(分子量7 612.71 Da)和化学合成的亚麻苦肽(分子量1 149.46 Da)作为参照,分别将上述标准样及制备的亚麻水解多肽,在相同条件下,上样Superdex 75 prep grade凝胶色谱柱,波长220 nm检测,绘制各自洗脱体积和A220nm吸收值关系曲线,通过与两个已知蛋白的洗脱图谱比对,粗略测定亚麻水解多肽分子量分布范围。
1.9 统计分析方法
试验数据采用Minitab15软件进行方差分析。
2 结果与分析
2.1 制备亚麻多肽的蛋白酶筛选
选取6种蛋白酶,在各种酶的最适条件下酶解2 h见表2。
表2 6种蛋白酶酶解亚麻蛋白溶液制备多肽效果的对比
Table 2 Comparison of the effect of six proteases on enzymatic hydrolysis of defatted flaxseed meal

酶解时间/h木瓜蛋白酶 60 6.0 6 000 2 9.14胰蛋白酶 37 7.0 6 000 2 8.87胃蛋白酶 37 2.0 6 000 2 8.25菠萝蛋白酶 50 5.5 6 000 2 7.97 537酸性蛋白酶 45 3.0 6 000 2 22.97 3.350酸性蛋白酶 45 2.5 6 000 2 28.52酶种类 温度/℃ pH 加酶量/(U/g)酶解条件 多肽得率/%
由表2可知,3.350酸性蛋白酶酶解亚麻蛋白得率(28.52%)最高,537酸性蛋白酶酶解亚麻蛋白得率(22.97%)次之,因此选用3.350酸性蛋白酶制备亚麻多肽。
2.2 3.350酸性蛋白酶制备亚麻多肽的单因素试验结果
2.2.1 酶解温度对亚麻多肽得率的影响
在酶解时间2 h,加酶量6 000 U/g,pH2.5的条件,酶解温度对亚麻多肽得率的影响见图1。

图1 温度对亚麻多肽得率的影响
Fig.1 Effect of temperature on the yield of flax polypeptide
由图1可知,当温度小于60℃时,多肽得率随着温度的升高而增大,温度为60℃时达到最大值,温度大于60℃时,多肽得率有所下降。可能是因为酶解温度较高时,蛋白酶容易变性,从而使酶活性减弱。所以选择60℃为下一步正交试验的酶解温度。
2.2.2 pH值对亚麻多肽得率的影响
pH值对亚麻多肽得率的影响见图2。

图2 pH值对亚麻多肽得率的影响
Fig.2 Effect of pH on the yield of flax polypeptides
由图2可知,pH值对水解效果的影响显著,3.350酸性蛋白酶酶解亚麻分离蛋白在加酶量6 000 U/g,酶解温度60℃,酶解时间2 h时,当pH值达到3.0时,多肽得率最大,当pH值大于3.0时,多肽得率略有下降。3.350酸性蛋白酶在pH值较低时酶活较高,所以选取pH3.0为下一步正交试验的酶解pH。
2.2.3 加酶量对亚麻多肽得率的影响
在酶解温度60℃,pH值3.0,酶解时间2 h的条件下,加酶量与多肽得率的关系见图3。
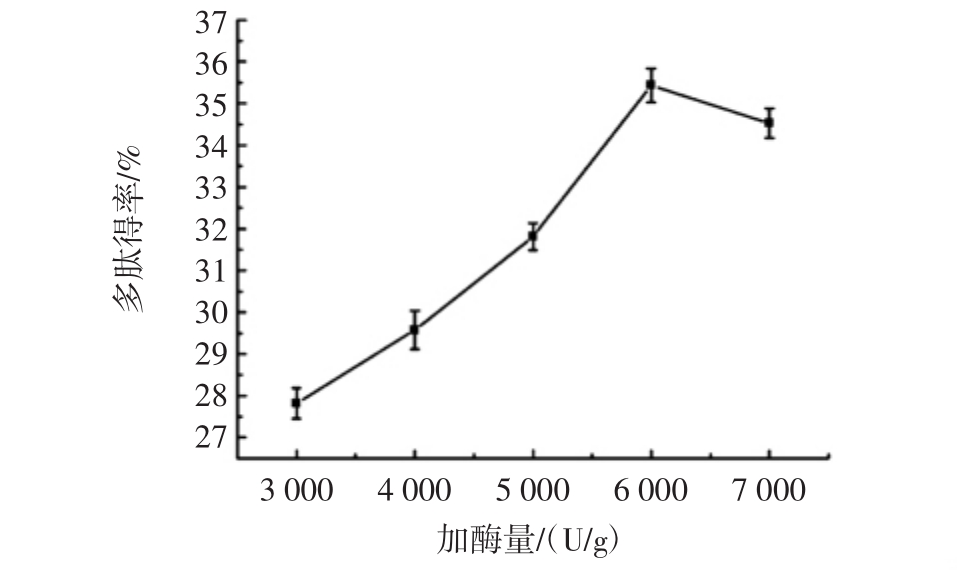
图3 加酶量对亚麻多肽得率的影响
Fig.3 Effect of enzyme addition on yield of flax polypeptides
从图3中可以看出,当加酶量为6 000 U/g时,亚麻多肽得率最大,即使增加酶的量也就不会对水解速度有明显的影响,多肽得率反而有所下降。因此,选择蛋白酶添加量为6 000 U/g,作为下一步正交试验的加酶量。
2.2.4 酶解时间对亚麻多肽得率的影响
当酶解温度60℃,pH值3.0,加酶量6 000 U/g时,酶解时间与多肽得率的关系表现为:当酶解时间小于2 h时,随着时间的延长,多肽得率快速上升,2 h时达到最大值,之后再延长酶解时间,多肽得率逐渐下降见图4,这可能是因为随着水解的进行,蛋白质底物逐渐减少,且酶解产物不断积累对蛋白酶本身造成抑制,或者多肽又被进一步酶解成为氨基酸。还可能是因为随着时间延长,多肽之间通过非共价键(如疏水基作用、氢键和配位键)相互聚集,产生了聚合反应,导致多肽减少。因此,选择酶解时间为2 h,作为下一步正交实验的蛋白酶解时间。

图4 酶解时间对亚麻多肽得率的影响
Fig.4 Effect of enzymolysis time on yield of flax polypeptide
2.3 3.350酸性蛋白酶制备亚麻多肽的正交试验结果
综合单因素试验结果,以亚麻多肽得率为指标,进行正交试验,结果见表3。
表3 正交试验设计与结果
Table 3 Orthogonal experimental design and results
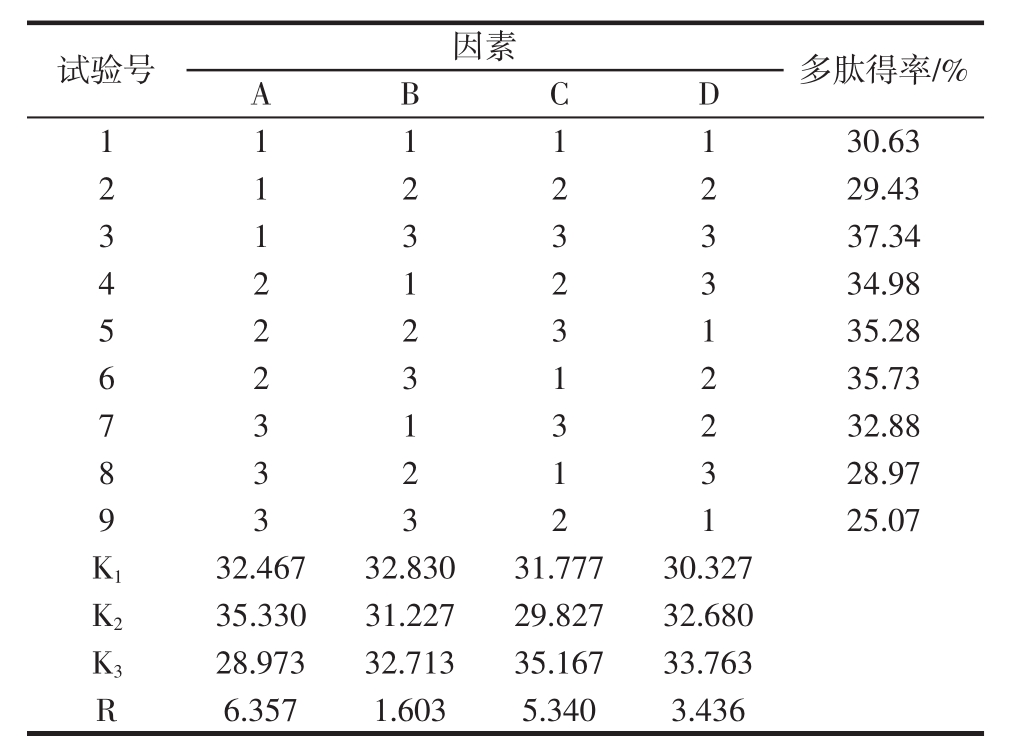
试验号 因素 多肽得率/%A B C D 1 1 1 1 1 30.63 2 1 2 2 2 29.43 3 1 3 3 3 37.34 4 2 1 2 3 34.98 5 2 2 3 1 35.28 6 2 3 1 2 35.73 7 3 1 3 2 32.88 8 3 2 1 3 28.97 9 3 3 2 1 25.07 K1 32.467 32.830 31.777 30.327 K2 35.330 31.227 29.827 32.680 K3 28.973 32.713 35.167 33.763 R 6.357 1.603 5.340 3.436
由表3可知,制备亚麻多肽的最佳工艺组合为A2B1C3D3,即温度 60 ℃、pH2.7、加酶量 6 500 U/g、酶解时间2.5 h,在此条件下进行验证试验,制备亚麻多肽得率的提取率为38.80%。又由极差分析可知,各因素对多肽得率的影响大小顺序为A>C>B>D,即酶解温度对亚麻多肽得率的影响最大,加酶量和pH值次之,酶解时间的影响最小。方差分析结果(表4)表明酶解温度和加酶量对制备亚麻多肽得率的影响显著,其他2个因素的影响均不显著。
表4 方差分析结果
Table 4 Analysis of variance

注:* 显著(P<0.05);** 极显著(P<0.01)。
因素 偏差平方和 自由度 F比 F临界值 显著性温度 60.809 2 12.684 9.000 *pH 4.794 2 1.000 9.000加酶量 43.810 2 9.139 9.000 *酶解时间 18.522 2 3.864 9.000误差 4.79 2
2.4 多肽抗氧化活性分析
2.4.1 亚麻多肽相对还原力的测定
亚麻多肽的还原能力见图5。

图5 亚麻多肽的还原能力
Fig.5 Reduction activity of flax polypeptides
由图5可知,在0.15 mg/mL~1.2 mg/mL有效质量浓度范围内,亚麻多肽的还原能力随着质量浓度的升高而增大,且增幅明显。此后,随着质量浓度增大,亚麻多肽的还原能力变化不明显,趋于稳定,逐步达到其最大还原能力。
2.4.2 亚麻多肽对DPPH自由基的清除作用
亚麻多肽对DPPH自由基的清除能力见图6。
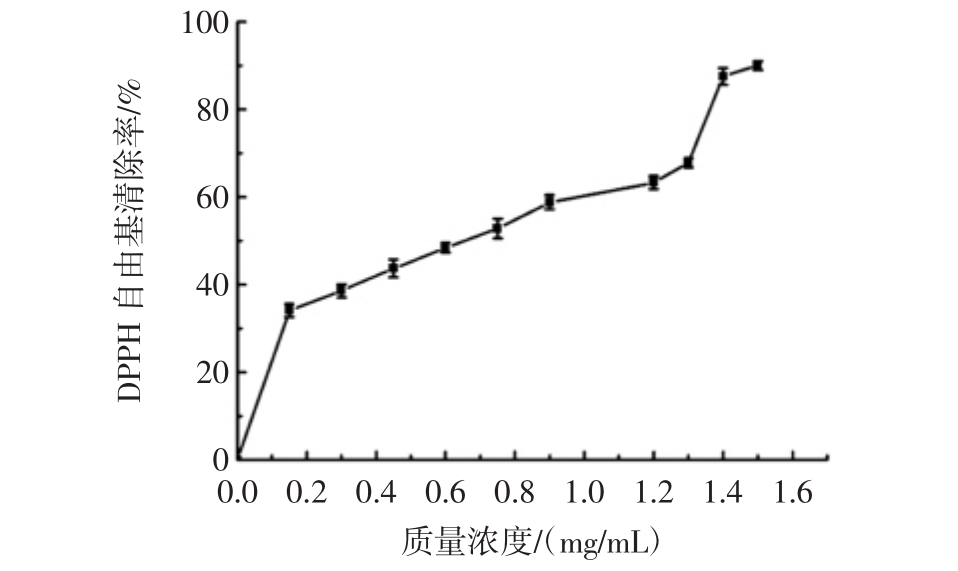
图6 亚麻多肽对DPPH自由基的清除能力
Fig.6 DPPH free radical scavenging ability of flax and polypeptide
由图6可知,亚麻多肽DPPH自由基清除率与浓度呈正比,可能是酶解过程产生了能有效清除DPPH·的小分子肽类,当酶解液质量浓度为1.5 mg/mL时,DPPH·清除率达到了最大值89.99%。
2.4.3 亚麻多肽对O2-·自由基的清除作用
亚麻多肽对O2-·自由基的清除能力见图7。

图7 亚麻多肽对O2-·自由基的清除能力
Fig.7 The scavenging ability of flax and polypeptide on O2-·free radicals
由图7可知,制备的亚麻多肽清除O2-·能力随质量浓度增加,有明显的增大趋势,当多肽质量浓度为0.6 mg/mL时,清除率可达85.57%;此后,随着质量浓度增大,亚麻多肽对O2-·清除效果变化不明显,趋于稳定,逐步达到其最大的清除O2-·效果。
2.5 亚麻水解多肽分子量的分布范围
亚麻水解多肽分子量分布范围见图8。
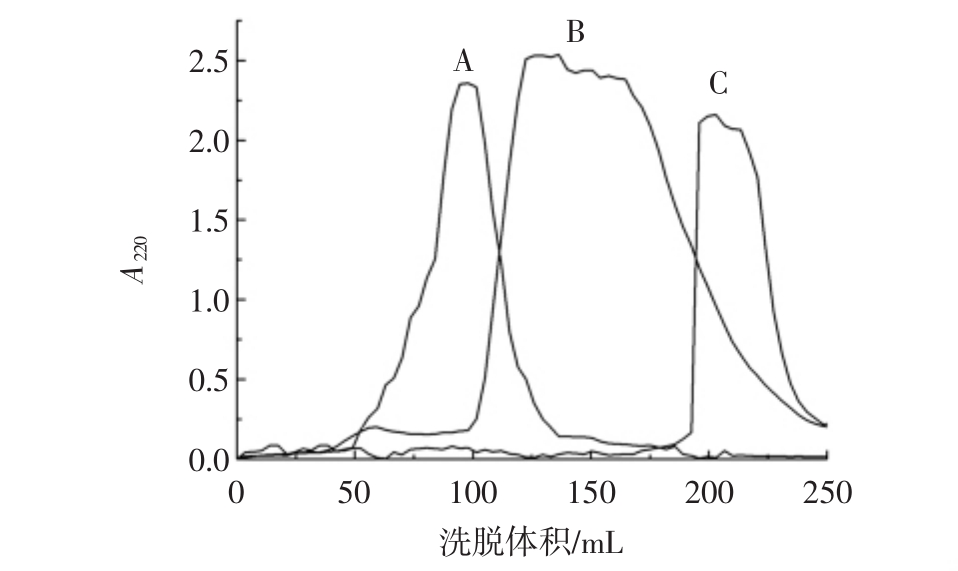
图8 亚麻水解多肽分子量分布范围
Fig.8 Molecular weight distribution of flax hydrolyzed peptides
A.亚麻胰蛋白酶抑制剂;B.亚麻多肽;C:亚麻苦肽。
通过Superdex 75 prep grade凝胶色谱法,对亚麻水解多肽分子量的分析,揭示亚麻水解多肽在凝胶层析的上洗脱的体积,介于亚麻胰蛋白酶抑制(7 612.71 Da)和亚麻苦肽(MLIPPFFVI,1 149.46 Da)的洗脱体积间,说明利用酸性蛋白酶3.350制备的亚麻水解多肽的分子量分布范围主要集中在1 000 Da~7 600 Da间。
3 结论
3.350 酸性蛋白酶制备亚麻多肽单因素和正交试验,表明制备亚麻多肽的最佳工艺条件为:酶解温度60 ℃、pH2.7、加酶量 6 500 U/g、酶解时间 2.5 h,此条件下亚麻多肽的得率为38.80%。对亚麻多肽得率的影响因素排序为酶解温度>加酶量>pH值>酶解时间,其中酶解温度和加酶量对亚麻多肽得率影响显著。亚麻多肽对DPPH自由基和超氧阴离子自由基有明显的清除作用,说明亚麻多肽具有良好的抗氧化活性,并随着多肽质量浓度的升高,其抗氧化活性不断增强,表现出良好的量效关系,这为亚麻多肽功能性食品开发提供理论依据。制备的亚麻多肽的分子量主要分布在1 000 Da~7 600 Da间的范围,但是亚麻多肽的组成及构效关系有待进一步研究。
[1]吴征镒,于锦秀,汤彦承.胡麻是亚麻,非脂麻辨[J].植物分类学报,2007(4):458-472
[2]张金.胡麻籽的营养保健价值与产业前景[J].中国食品工业,2006(3):32-32,34
[3]杨宏志.亚麻籽脱毒和木脂素提取工艺研究[D].北京:中国农业大学,2005
[4]史高峰,孙浩冉,陈学福,等.亚麻的开发利用研究[J].安徽农业科学,2006,34(10):2179-2181
[5]Bernacchia R,Preti R,Vinci G.Chemical composition and health benefits of flaxseed[J].Austin J Nutri Food Sci,2014,2(8):1045
[6]孔令明,李芳,陶永霞,等.多肽的功能活性与研究进展[J].中国食品添加剂,2009,71(3):71-73
[7]王树华,王树祥,王昀.抓紧发展生物活性肽[J].化工管理,2004(5):27
[8]Byun HG,Kim SK.Purificatio and characterization of angiotensin I converting enayme(ACE)inhibitory peptides from Alaska pollack(Theragra chalcogramma)skin[J].Process Biochemistry,2001(36):1155-1162
[9]Nooshin AP,Eunine CY,Li Chan.Comparison of protein surface hydrophobicity measured at various pH values us-ing three different fluorescent probes[J].Journal of Agricultural and Food Chemistry,2000(48):328-334
[10]周婷婷,李燕,宋斐.抗氧化大豆多肽制备的研究[J].食品工业科技,2010,31(3)281-284
[11]刘英丽,张慧娟,王静,等.酶解花生粕制备抗氧化肽工艺研究[J].中国食品学报,2014,14(8):62-68
[12]Moller Niels Peter,Scholz-Ahrens Katharina Elisabeth,Roos Nils,et al.Bioactive peptides and proteins from foods:indication for health effects[J].European Jjournal of nutrition,2008,47(4):171-182
[13]訾艳,王常青,陈晓萌,等.具有α-淀粉酶抑制活性的白芸豆多肽的制备及其热稳定性研究[J].食品科学,2015,36(13):190-195
[14]Kaur Rajbir,Arora Saroj,Singh Bikram.Antioxidant activity of the phenol rich fractions of leaves of Chukrasia tabularis A.Juss[J].Bioresource technology,2008,99(16):7692-7698
[15]陈金海,徐怀德,李艳伏,等.碱性蛋白酶酶解核桃粕蛋白产物抗氧化特性研究[J].广西植物,2014,13(2):183-188
[16]Bektas Tepe,Munevver Sokmen,H Askin Askin Akpulat,et al.In Vitor antioxidant activities of the methanol extracts offive Allium species from Turkey[J].Food Chemistry,2005,92:89-92
[17]陈永浩,王克建,郝艳宾,等.酶解方式对核桃蛋白肽及其抗氧化活性的影响[J].食品与机械,2011,27(5):63-67
[18]励建荣,齐旦旦,张蕾.蜂王浆水溶性蛋白质及其水解多肽对自由基的清除能力和对胰脂肪酶和α-葡萄糖苷酶的抑制活性[J].中国食品学报,2012(9):8-15
[19]LIU Q,KONG B H,XIONG Y L,et a1.Antioxidant activity and functional properties of porcine plasma protein hydrolysate as influenced by the degree of hydrolysis[J].Food Chemistry,2010,118(2):403-410