芒果(Mangifera indica L.)属于漆树科植物,主要分布在我国广西、海南、云南等地,其中芒果叶富含黄酮和酚酸类等,芒果果实富含糖类、有机酸类、类胡萝卜素等活性成分[1-2],具有多种药理作用,如芒果苷抗氧化与调节糖脂代谢、止咳平喘等[3-5]。现有研究主要针对芒果叶部位的有效成分,而对芒果果实、树皮等化学成分和药理作用的研究尚少。果皮是芒果食用及加工过程中的废弃物,研究发现芒果皮提取物可以改善高脂血症模型大鼠血脂水平和肝功能,并具有一定的抵抗脂质过氧化作用[6]。为提高芒果资源综合利用率及进一步了解芒果多糖的生物活性,本研究探讨纤维素酶提取芒果果皮多糖的最佳条件,并研究其体外抗氧化活性,为芒果果皮多糖开发利用提供一定的科学理论依据。
1 材料与方法
1.1 材料与仪器
芒果:品种为桂七芒,市售,本研究取其干燥果皮作为材料;纤维素酶(食品级,5万U/g)、维生素C、D-无水葡萄糖:北京索莱宝科技有限公司;1,1-二苯基-2-三硝基苯肼(1,1-Diphenyl-2-picrylhydrazyl,DPPH):日本TCI公司;其它试剂均为国产分析纯。
5810R型高速离心机:德国eppendorf公司;Alpha-1506型紫外分光光度计:上海谱元仪器有限公司;SHA-BA双功能水浴恒温振荡器:常州华普达教学仪器有限公司;PHS-25型pH计:上海仪电科学仪器股份有限公司;SHB-III型循环水真空泵、2L-ARE旋转蒸发器:上海皓庄仪器有限公司。
1.2 方法
1.2.1 芒果果皮多糖提取
多糖提取具体操作方法参照文献[7]进行,主要包括粉碎、特定酶解条件下提取、高温灭活、分离浓缩、乙醇沉淀、Sevage法脱蛋白、二次醇沉、真空冷冻干燥等系列步骤。
1.2.2 多糖含量测定
多糖测定采用苯酚-硫酸法,葡萄糖标准曲线方程为 y=8.498 6x-0.018 5,R2=0.990 3,式中 y为 490 nm条件下的吸光度值、x为葡萄糖质量浓度(mg/mL)。多糖得率/%=cnV/m×100。
式中:c为样品稀释液中多糖的浓度,mg/mL;n为稀释倍数;V为样品稀释液体积mL;m为芒果果皮粉末质量,mg。
1.2.3 多糖提取单因素试验
酶解时摇床转速固定为180 r/min,分别考察pH值(3.0、4.0、5.0、6.0、7.0)、液料比[4 ∶1、8 ∶1、12 ∶1、16 ∶1、20 ∶1(mL/g)]、酶添加量(2、6、10、14、18 mg/mL)、酶解时间(40、80、120、160、200 min) 和酶解温度(35、40、45、50、55、60 ℃)对芒果果皮多糖得率的影响,其中各因素固定水平为pH 5.0、液料比 8∶1(mL/g)、酶添加量10 mg/mL、酶解时间80 min、酶解温度45℃。
1.2.4 响应面试验
响应面因素水平设计见表1,自变量包括酶解pH值、酶解时间、酶添加量、液料比4个因素,以多糖得率为响应值。数据分析采用Design Expert 8.06软件。
表1 响应面因素设计及水平
Table 1 Factors and levels in response surface design
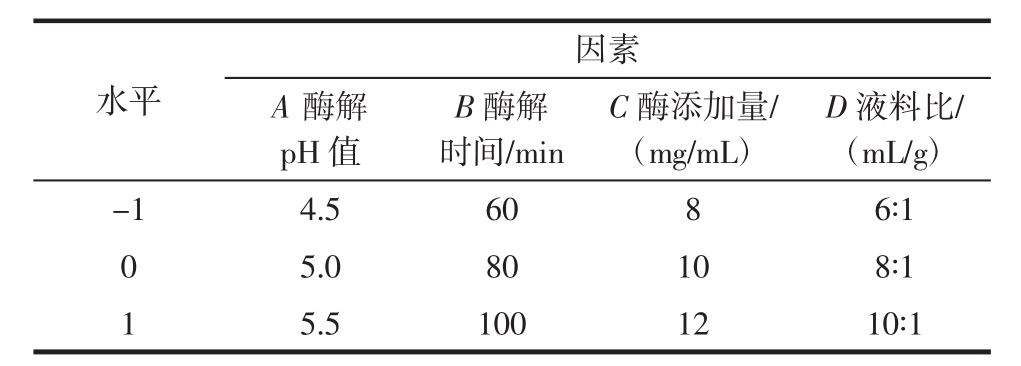
水平D液料比/(mL/g)-1 4.5 60 8 6∶1 0 5.0 80 10 8∶1 1 5.5 100 12 10∶1因素A酶解pH值B酶解时间/min C酶添加量/(mg/mL)
1.2.5 芒果果皮多糖体外抗氧化活性测定
1.2.5.1 DPPH自由基清除能力测定
取不同质量浓度的样品溶液2 mL和2 mL DPPH溶液(0.2 mmol/L)混匀,反应30 min后在517 nm处测定其吸光度A1,同法测定2.0 mL乙醇加样液的吸光度A2,以及2.0 mL DPPH溶液与2.0 mL蒸馏水的吸光度A0,以维生素C作为对照,样品对DPPH自由基的清除率 Y/%=[1-(A1-A2)/A0]×100[7]。
1.2.5.2 ·OH清除能力测定
取不同质量浓度的样品提取液2 mL,依次加入浓度均为5 mmol/L的FeSO4溶液、H2O2溶液各2 mL,混匀,静置10 min,再加入5 mmol/L的水杨酸溶液2 mL,混匀,37℃水浴30 min后,波长510 nm处测定吸光度B1,用蒸馏水代替水杨酸测定吸光度B2,以蒸馏水代替样品溶液测定吸光度B0,以维生素C作为对照,样品对·OH 的清除率 Y/%=[1-(B1-B2)/B0]×100[7-8]。
2 结果与分析
2.1 单因素对芒果果皮多糖得率的影响
纤维素酶添加量对多糖得率的影响见图1。
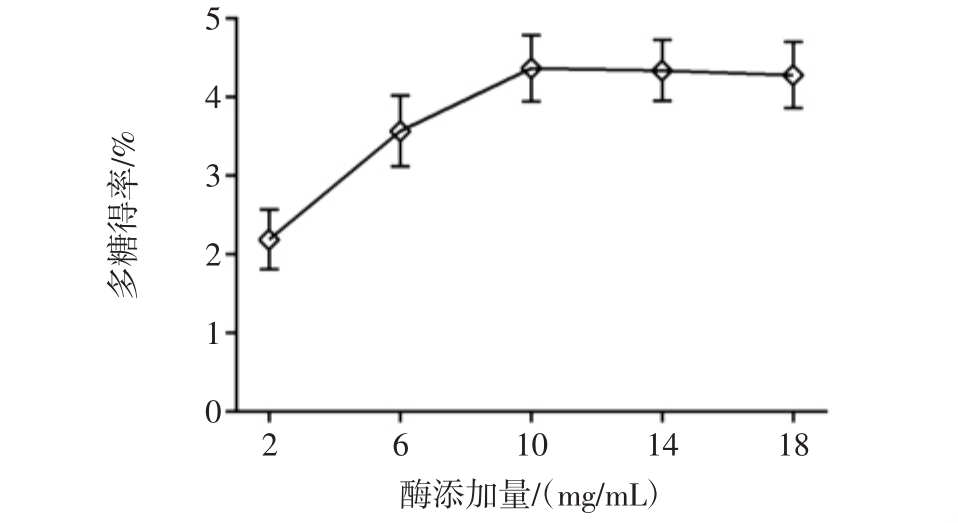
图1 纤维素酶添加量对多糖得率的影响
Fig.1 Influence of cellulase addition amount on the polysaccharide extraction rate
由图1可知,当酶添加量增加到10 mg/mL时,多糖得率可达4.37%,进一步加大酶用量,多糖得率没有显著变化,说明在该底物浓度下,酶浓度已经趋于饱和,继续增加纤维素酶用量,对多糖得率没有显著影响,选择10 mg/mL作为酶的最佳添加量。
pH值对多糖得率的影响见图2。
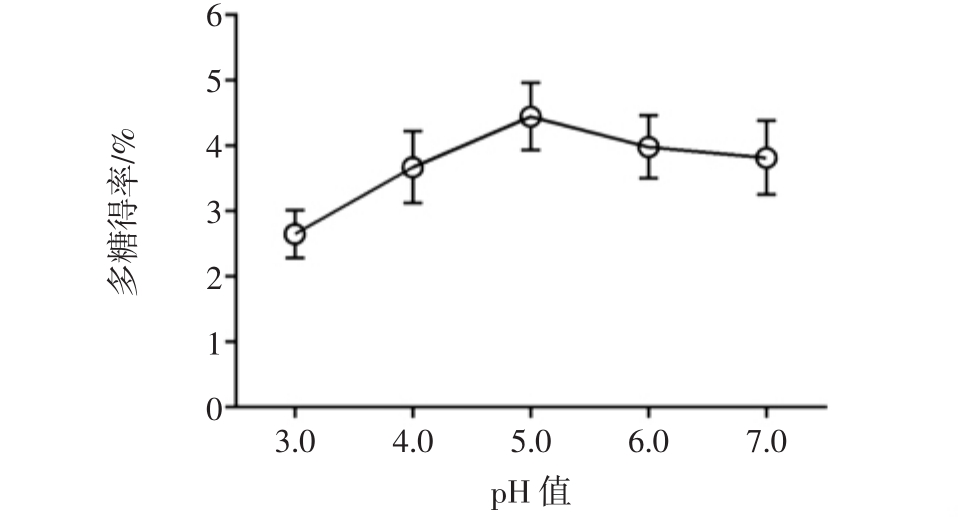
图2 pH值对多糖得率的影响
Fig.2 Influence of pH value on the polysaccharide extraction rate
由图2可知,当pH值增加到5.0时,多糖得率达到最大值4.45%,pH=7.0时多糖得率反而降低,酶解最佳pH值选定为5.0。
液料比对多糖得率的影响见图3。
由图3可知,当液料比增加到 8∶1(mL/g)时,多糖得率达到4.31%,之后,随着液料比增大,多糖得率反而减小,原因可能与过高液料比不利于多糖物质溶出有关,此外,水用量过大加重后续浓缩工作负担,不利于工业化实际生产,故液料比优化为8∶1(mL/g)。
酶解温度对多糖得率的影响见图4。
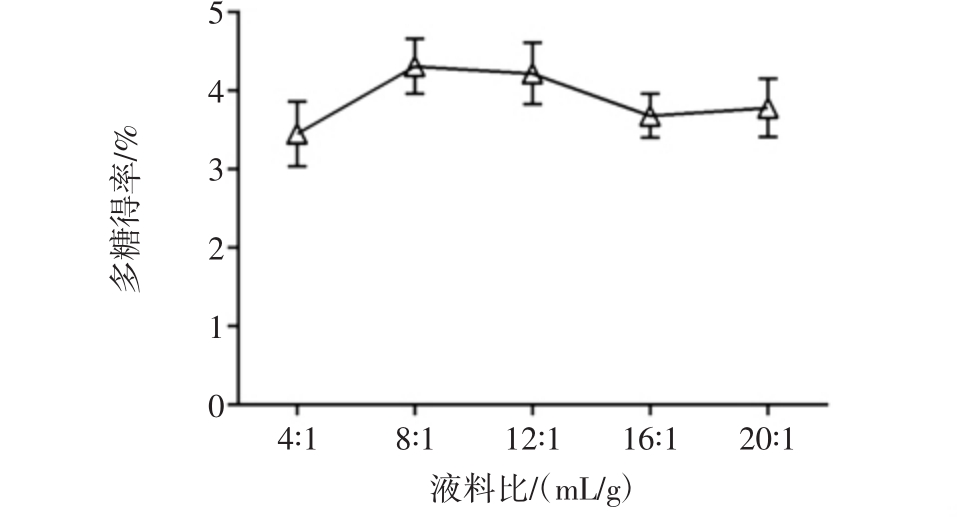
图3 液料比对多糖得率的影响
Fig.3 Influence of the ratio of water to material on the polysaccharide extraction rate

图4 酶解温度对多糖得率的影响
Fig.4 Influence of hydrolysis temperature on the polysaccharide extraction rate
由图4可知,随着温度的升高,多糖得率先提高后降低,这是由于温度过高导致酶活力减弱所致,选择45℃为本研究最佳酶解温度。
酶解时间对多糖得率的影响见图5。
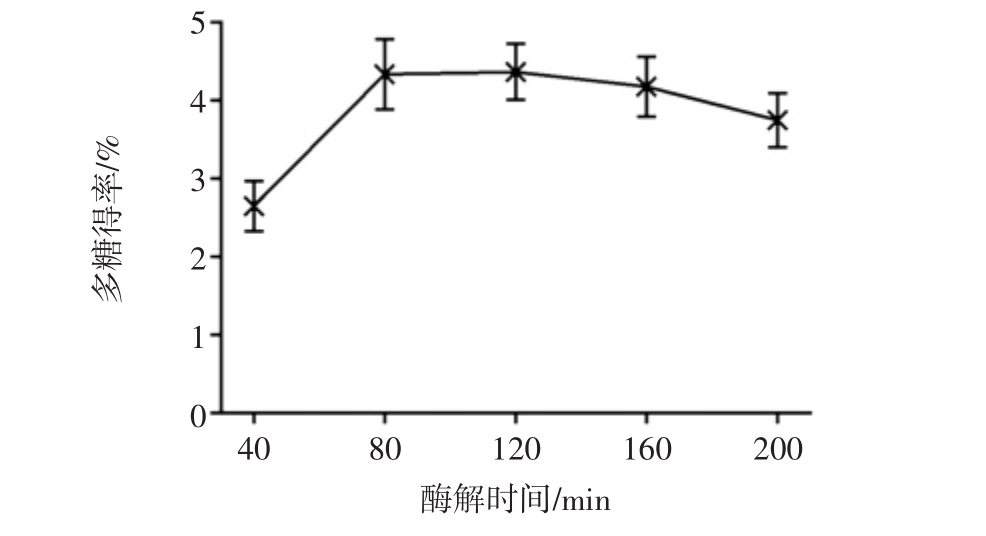
图5 酶解时间对多糖得率的影响
Fig.5 Influence of hydrolysis time on the polysaccharide extraction rate
由图5可知,当酶解时间为80 min时,多糖得率4.34%接近120 min时的最大值4.37%,本研究选择80 min为最佳酶解时间。
2.2 芒果果皮多糖纤维素酶提取的响应面优化试验
2.2.1 响应面试验结果与分析
试验设计及结果见表2,回归模型方差分析见表3。
表2 芒果果皮多糖提取的响应面试验结果
Table 2 Results of response surface design for Mangifera indica L.rind polysaccharides extraction
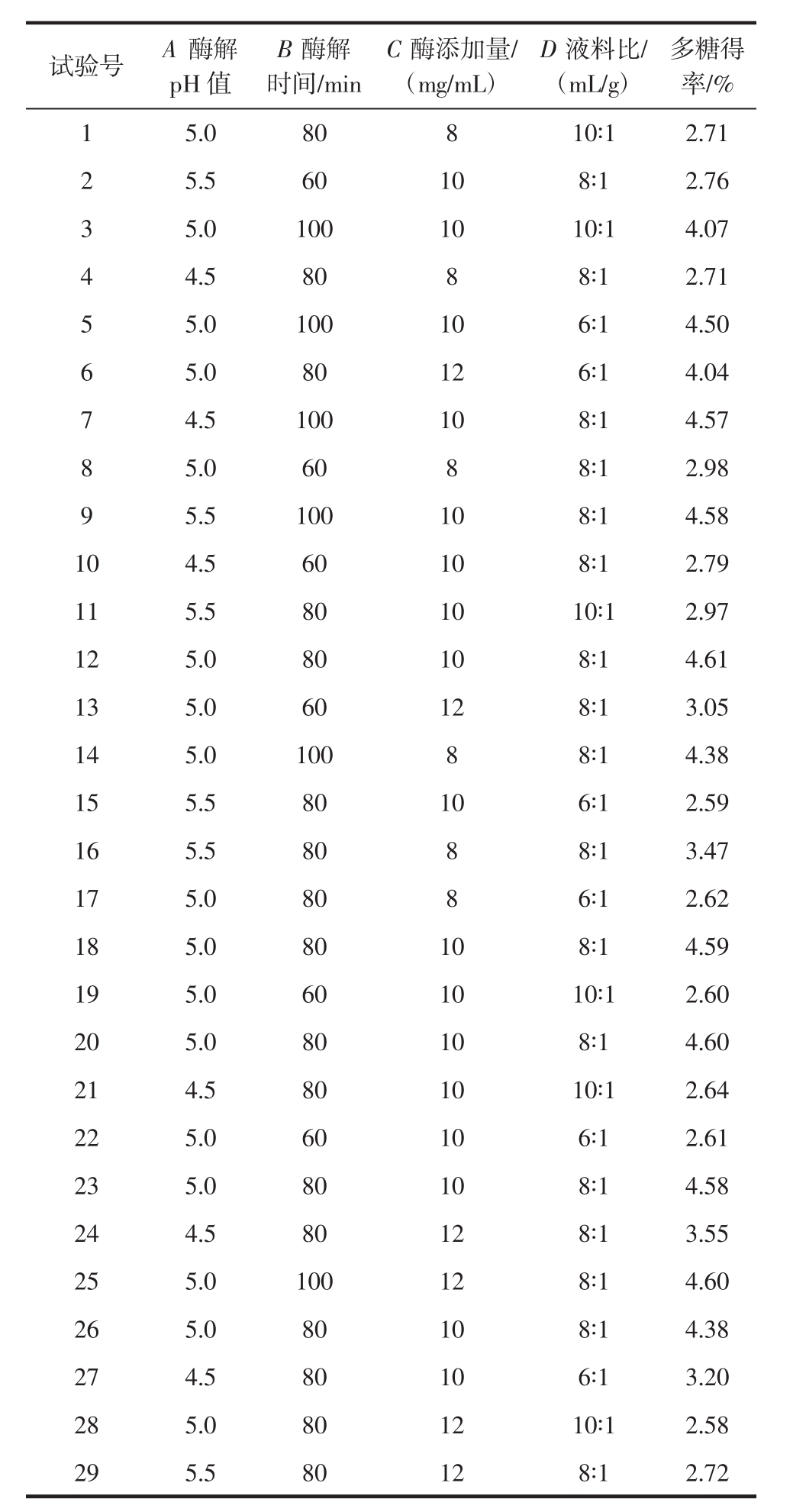
试验号 A酶解pH值多糖得率/%1 5.0 80 8 10∶1 2.71 2 5.5 60 10 8∶1 2.76 3 5.0 100 10 10∶1 4.07 4 4.5 80 8 8∶1 2.71 5 5.0 100 10 6∶1 4.50 6 5.0 80 12 6∶1 4.04 7 4.5 100 10 8∶1 4.57 8 5.0 60 8 8∶1 2.98 9 5.5 100 10 8∶1 4.58 10 4.5 60 10 8∶1 2.79 11 5.5 80 10 10∶1 2.97 12 5.0 80 10 8∶1 4.61 13 5.0 60 12 8∶1 3.05 14 5.0 100 8 8∶1 4.38 15 5.5 80 10 6∶1 2.59 16 5.5 80 8 8∶1 3.47 17 5.0 80 8 6∶1 2.62 18 5.0 80 10 8∶1 4.59 19 5.0 60 10 10∶1 2.60 20 5.0 80 10 8∶1 4.60 21 4.5 80 10 10∶1 2.64 22 5.0 60 10 6∶1 2.61 23 5.0 80 10 8∶1 4.58 24 4.5 80 12 8∶1 3.55 25 5.0 100 12 8∶1 4.60 26 5.0 80 10 8∶1 4.38 27 4.5 80 10 6∶1 3.20 28 5.0 80 12 10∶1 2.58 29 5.5 80 12 8∶1 2.72 B酶解时间/min C酶添加量/(mg/mL)D液料比/(mL/g)
表3 芒果果皮多糖提取响应面试验结果的方差分析
Table 3 Variance analysis of response surface design for Mangifera indica L.rind polysaccharides extraction
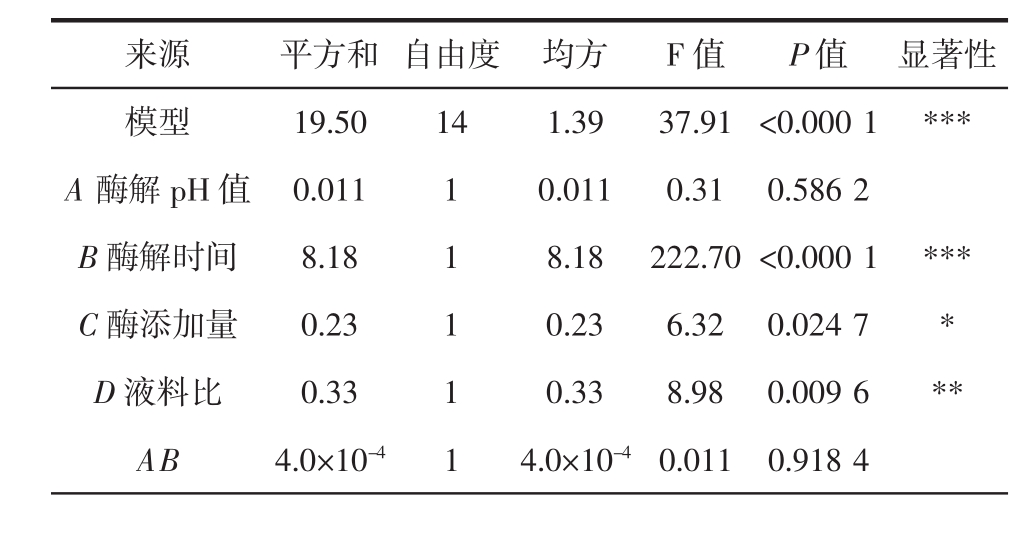
来源 平方和 自由度 均方 F值 P值 显著性模型 19.50 14 1.39 37.91 <0.000 1 ***A酶解pH值 0.011 1 0.011 0.31 0.586 2 B酶解时间 8.18 1 8.18 222.70<0.000 1 ***C酶添加量 0.23 1 0.23 6.32 0.024 7 *D液料比 0.33 1 0.33 8.98 0.009 6 **AB 4.0×10-4 1 4.0×10-40.011 0.918 4
续表3 芒果果皮多糖提取响应面试验结果的方差分析
Continue table 3 Variance analysis of response surface design for Mangifera indica L.rind polysaccharides extraction

注:差异显著(*P<0.05);差异非常显著(**P<0.01);差异极显著(***P<0.001)。
来源 平方和 自由度 均方 F值 P值 显著性AC 0.63 1 0.63 17.20 0.001 0 **AD 0.22 1 0.22 6.01 0.028 0 *BC 5.6×10-3 1 5.6×10-3 0.15 0.701 5 BD 0.044 1 0.044 1.20 0.291 8 CD 0.60 1 0.60 16.34 0.001 2 **A2 3.76 1 3.76 102.22<0.000 1 ***B2 0.13 1 0.13 3.63 0.077 3 C2 2.77 1 2.77 75.38 <0.000 1 ***D2 5.71 1 5.71 155.46<0.000 1 ***残差 0.51 14 0.037失拟性 0.48 10 0.048 5.09 0.065 4纯误差 0.037 4 9.4×10-3总和 20.02 28 R2=0.974 3 R2Adj=0.948 6
对表2中数据进行回归拟合,获得自变量(酶解pH值、酶解时间、酶添加量、液料比)与芒果果皮多糖得率(Y)的二次多项回归方程:
Y=4.55-0.031A+0.83B+0.14C-0.17D+0.01AB-0.40AC+0.24AD+0.037BC-0.10BD-0.39CD-0.76A2-0.14B2-0.65C2-0.94D2。由表3可知,回归方程模型P<0.000 1,达到极显著水平,失拟项P>0.05不显著(P=0.065 4),模型总决定系数R2=0.974 3,调整后R2Adj=0.948 6,以上参数均说明该模型与试验数据拟合程度好,试验误差小,可用于不同变量条件下的响应值预测。
由表3F值可知,芒果果皮多糖纤维素酶法提取影响因素的主次顺序为:酶解时间(B)>液料比(D)>酶添加量(C)>酶解pH值(A),其中A影响不显著,其它三因素均达到显著水平。因素间交互作用对芒果果皮多糖得率的影响如图6所示。
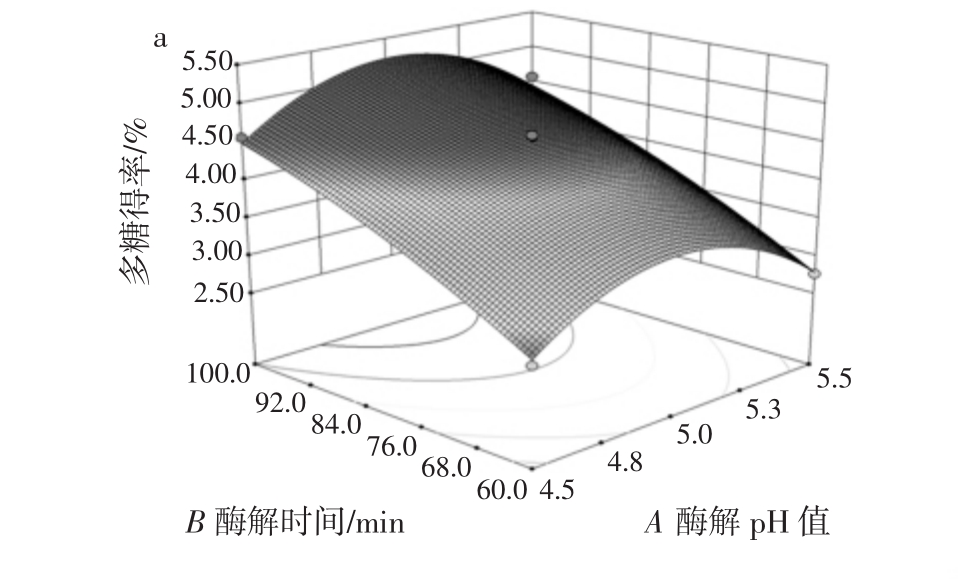

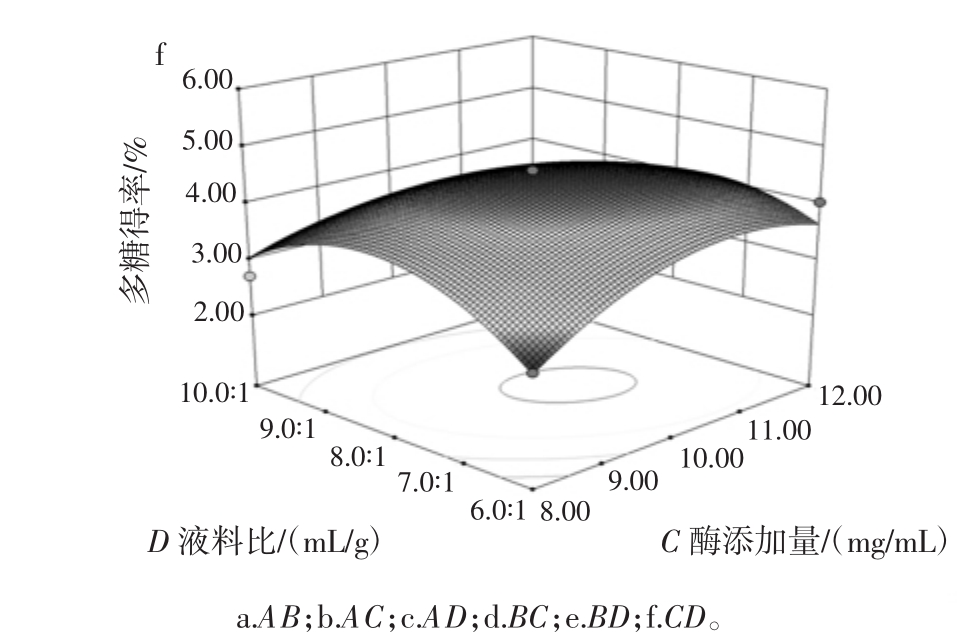
图6 各因素交互作用对多糖得率影响的响应面图
Fig.6 Response surface graphs showing the interactions of various factors on polysaccharide yield
由图6(b、c、f)和表3方差分析结果可知,AC、AD、CD交互作用显著影响芒果果皮多糖酶法提取的得率,其中AC、CD达到非常显著水平,AD达到显著水平,其它两因素间交互作用对多糖得率的影响均不显著(P>0.05)。
2.2.2 最佳提取条件预测及验证
对回归模型方程求解,获得芒果果皮多糖纤维素酶提取的最佳条件为酶解pH4.9,酶解时间100.0 min,酶添加量 10.46 mg/mL,液料比 7.6 ∶1(mL/g),此条件下多糖得率为5.28%。考虑实际操作方便,将上述最佳提取参数修改为酶解pH值5.0,酶解时间100.0 min,酶添加量 10.5 mg/mL,液料比 7.6 ∶1(mL/g),根据工艺条件进行3组平行试验,所得多糖得率平均值为(5.17±0.64)%,与回归方程理论多糖得率5.28%的相对误差为2.08%,提示本响应面法得到的回归模型有效、可靠,得到的纤维素酶提取芒果果皮多糖工艺条件具有实际应用价值。
2.3 芒果果皮多糖体外抗氧化活性
2.3.1 芒果果皮多糖对DPPH自由基清除作用
芒果果皮多糖对DPPH自由基的清除作用见图7。
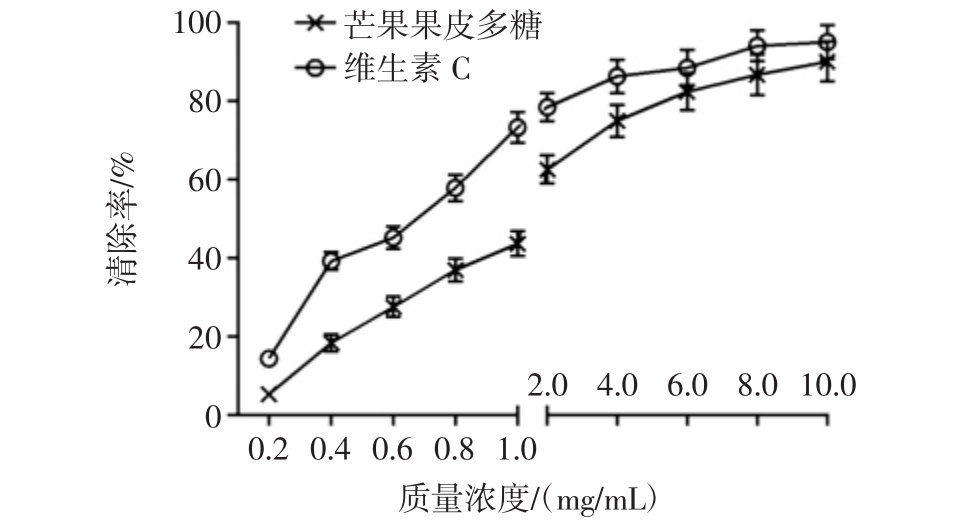
图7 芒果果皮多糖对DPPH自由基的清除作用
Fig.7 The scavenging effect of polysaccharide from Mangifera indica L.rind on DPPH radical
由图7可知,当芒果果皮多糖浓度在0.2 mg/mL~10 mg/mL时,对DPPH自由基清除率不断增大,当质量浓度为10 mg/mL时,芒果果皮多糖对DPPH自由基清除率为90.14%,而维生素C对DPPH自由基清除率可达95.13%,芒果果皮多糖清除DPPH自由基的半数抑制浓度IC50为1.385 mg/mL,维生素C的IC50为0.716 mg/mL,两者比较,芒果果皮多糖清除能力弱于维生素C。以上结果提示芒果果皮多糖具有较好的DPPH自由基清除作用。
2.3.2 芒果果皮多糖对·OH清除作用
芒果果皮多糖对·OH的清除作用见图8。
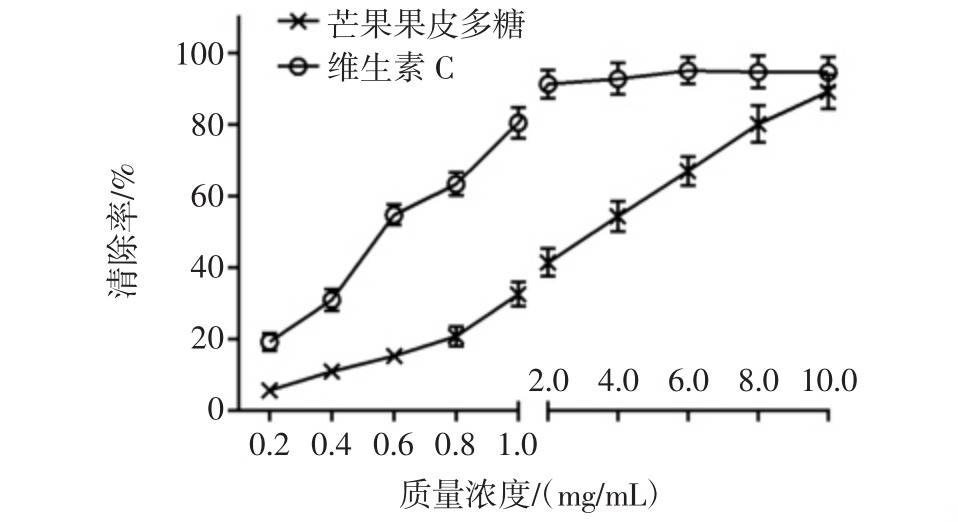
图8 芒果果皮多糖对·OH的清除作用
Fig.8 The scavenging effect of polysaccharide from Mangifera indica L.rind on hydroxyl radical
由图8可知,当芒果果皮多糖浓度在0.2 mg/mL~10 mg/mL时,对·OH清除率稳步提升,而维生素C在浓度6 mg/mL时对·OH清除率就已达到最大值95.08%,之后趋于稳定。当质量浓度为10 mg/mL时,芒果果皮多糖对·OH清除率为89.24%,维生素C对·OH清除率可达94.69%,芒果果皮多糖清除·OH的IC50为3.612 mg/mL,维生素C的IC50为0.587 mg/mL,两者比较,维生素C清除能力强于芒果果皮多糖。以上结果说明芒果果皮多糖具有较好的·OH清除作用。
3 结论讨论
天然植物多糖越来越受到学者的重视,主要因为其具有多种药理活性,如抗炎、抗氧化、提供免疫功能等,还具有毒副作用低等特点。天然产物多糖来自于植物细胞膜和微生物细胞壁的天然高分子化合物,可采用有机溶剂、酶解等方法提取,其中酶解提取操作简单、条件较温和,在多糖结构研究以及活性保持方面具有一定的优势[9]。植物多糖具有抗肿瘤、抗病毒、防衰老、降血糖等生物活性,可作为药物和保健品的有效成分,药食两用植物多糖系列产品的市场前景将非常广阔[10-11]。
芒果果皮约占整个鲜果的15%左右,果皮作为加工副产物,在企业生产中都作为废弃物丢弃,对环境造成污染还浪费资源。芒果果皮中富含多糖、膳食纤维、苷类、挥发油等功效成分[12-14],具有抗氧化、抑菌、调节脂代谢等作用[15-16]。研究表明,采用热水浸提、乙醇沉淀法提取芒果不同部位多糖,其中果实多糖含量达到4.6%[2],叶中多糖含量为1.5%[17]。林燕如等还使用超声波辅助乙醇沉淀法提取芒果叶中多糖,提取量为1.0%[18],对芒果有效成分多糖的研发将有助于提升其附加值。
本研究在单因素试验基础上,通过响应面设计优化了芒果果皮多糖纤维素酶提取的工艺。结果发现,纤维素酶酶解时间对芒果果皮多糖得率影响最显著,其次是液料比、酶添加量,而酶解pH值对其多糖提取影响最小;芒果果皮多糖最佳酶解提取条件为酶解pH5.0,酶解时间 100.0 min,酶添加量 10.5 mg/mL,液料比7.6∶1(mL/g)、酶解温度45℃,在此条件下芒果果皮多糖的得率为5.17%,与回归模型方程预测值5.28%相比,相对误差小于5%。张莉等采用超声波辅助乙醇沉淀法提取芒果皮渣中多糖,结果表明在提取温度80℃、超声功率160 W、提取时间90 min、料液比1∶2(g/mL)、提取次数2次的条件下,芒果皮渣多糖得率为0.81%[19],此外,王维民等研究表明芒果皮中粗多糖得率可达3.5%[20],均低于本研究中酶法提取的多糖得率。
通过体外抗氧化活性试验,芒果果皮多糖对DPPH自由基、·OH均具有较强的清除能力,在试验质量浓度下其对两种自由基的清除能力均呈现一定的正相关关系,与张莉等研究结果一致[19]。芒果果皮多糖清除DPPH自由基的IC50为1.385 mg/mL,清除·OH的IC50为3.612 mg/mL。但与维生素C比较,芒果果皮多糖清除两种自由基的能力较弱。以上研究结果可为芒果果皮多糖的研究开发提供一定的前期理论基础。
[1]陈仪新,卫智权,陆广利,等.芒果不同部位化学成分和药理作用的研究近况[J].广西中医药大学学报,2015,18(2):102-105
[2]孙延芳,梁宗锁,张欣.芒果多糖的纯化与光谱分析[J].食品科学,2012,33(7):93-95
[3]杨海光,方莲花,杜冠华.芒果苷的药理作用研究进展[J].中国药理学通报,2016,32(1):5-8
[4]闫文昊,林贺,律广富,等.芒果苷现代药理作用研究[J].吉林中医药,2017,37(3):288-290
[5]刘颖,王硕,周小雷,等.芒果叶药理作用研究进展[J].中华中医药杂志,2017,32(2):662-665
[6]张丽婧,张岭,李林子,等.芒果皮提取物对高脂血症大鼠血脂,肝功能及脂质过氧化的影响[J].毒理学杂志,2015,29(4):294-297
[7]蒋德旗,黄利敏,王艳,等.响应面优化纤维素酶法提取桂花多糖工艺及其抗氧活性研究[J].食品工业科技,2015,36(2):271-275
[8]郑林龙,蒋剑平,许海顺,等.响应面法优化土茯苓多糖的提取工艺及抗氧化活性研究[J].中华中医药杂志,2014,29(3):918-922
[9]李萍,李卫燕,曹蔚.酶解技术在多糖结构和活性研究中的应用进展[J].西北药学杂志,2015,30(4):433-436
[10]李雨虹,董文宾,付瑜,等.药食两用植物多糖的研究进展[J].食品研究与开发,2016,37(9):219-221
[11]陈阳,杨娟.响应面法优化仙茅多糖的酶解工艺及其抗氧化活性研究[J].食品科技,2016,41(9):209-215
[12]胡会刚,赵巧丽,庞振才,等.芒果皮渣多糖脱蛋白和脱色工艺研究[J].食品工业科技,2018,39(1):183-188
[13]梁秀媚,胡卓炎,赵雷,等.提取方法对芒果皮精油化学成分的影响[J].食品与机械,2017,33(3):155-159
[14]刘铭,李秀婷,潘凌风,等.芒果皮可溶性膳食纤维的提取及性质研究[J].中国食品添加剂,2014(1):81-87
[15]周毅刚,许文天,马小卫,等.芒果果皮和果肉的抗氧化能力分析[J].广东农业科学,2013,40(24):87-90
[16]黄春萍,罗群,李洁.芒果皮中芒果苷提取工艺优化及其抑菌性分析[J].南方农业学报,2014,45(8):1452-1456
[17]李金花,农石生,韦柳培,等.芒果叶多糖的提取及含量测定[J].食品研究与开发,2012,33(3):135-137
[18]林燕如,陈宜菲,陈樱.正交试验优化芒果叶多糖的提取工艺[J].韩山师范学院学报,2014,35(3):56-60
[19]张莉,赵巧丽,刘翠芳,等.芒果皮渣多糖的超声波辅助提取及其抗氧化活性研究[J].热带农业科学,2017,37(10):72-78
[20]王维民,汪敏.芒果皮粗多糖提取的影响因素及工艺的研究[J].农产品加工,2005,4(9):128-131